Готовят серию калибровочных растворов путем разбавления пополам предыдущего (например, к 3 мл исходного раствора прибавляется 3 мл дистиллированной воды, взбалтывается и т. д.) Получают серию растворов с разным содержанием нитратов: 3000, 1500, 750, 375, 188, 94, 47, 23 мг/кг.
Под предметное стекло подкладывается лист белой бумаги, на стекло капают две капли изучаемого раствора и две такие же капли дифениламина в трехкратной повторности. Описывают реакцию согласно следующей градации, которую можно использовать как для калибровочных растворов, так и для двух типов анализов (по Церлинг, 1965).
Баллы | Характер окраски | Содержание нитратов, мг/кг |
6 | Сок или срез окрашиваются быстро и интенсивно в иссиня-черный цвет. Окраска устойчива и не пропадает | >3000 |
5 | Сок или срез окрашиваются в темно-синий цвет. Окраска сохраняется некоторое время | 3000 |
4 | Сок или срез окрашиваются в синий цвет. Окраска наступает не сразу | 1000 |
3 | Окраска светло-синяя, исчезает через 2-3 минуты | 500 |
2 | Окраска быстро исчезает, окрашиваются главным образом проводящие пучки | 250 |
1 | Следы голубой, быстро исчезающей окраски | 100 |
0 | Нет ни голубой, ни синей окраски. На целых растениях возможно порозовение | 0 |
Следует отметить, что основой для определения содержания нитратов в соке должны быть собственные исследования, а не вышеприведенная таблица, т. к. окраска может варьироваться в зависимости от качества реактивов, срока их годности, температуры в помещении и др.
Овощи и плоды расчленяют на части: зона, примыкающая к плодоножке, кожура, периферийная часть, серединная часть, кочерыжка (у капусты), жилки, лист без жилок. Вырезанные части мелко режут ножом и быстро растирают в ступке, сок отжимают через 2-3 слоя марли. 2 капли сока капают на чистое предметное стекло, положенное на белую бумагу, добавляют 2 капли дифениламина. Быстро описывают все наблюдаемые реакции согласно схеме. Повторность опыта 3-кратная. В случае сомнений в содержании нитратов в той или иной части овощной продукции капают рядом калибровочный раствор с известной концентрацией вещества и повторяют реакцию с дифениламином.
Анализ начинают с сока капусты и картофеля, затем помещают эти овощи в термостойкий химический стакан с кипящей дистиллированной водой и кипятят 10-15 мин, после чего анализируют и отварные овощи, и отвар. За время варки делают анализ различных частей других овощей и плодов (не менее четырех видов за занятие). Записывают в общую таблицу на доске и в частную – в тетради.
Схема записи
Содержание нитратов в различных овощах и плодах
Исследуемое растение | Часть | Баллы | Содержание нитратов в мг/кг |
Картофель свежий | а) под кожурой б) серединная часть | ||
Картофель отварной | те же части | ||
Капуста | а) жилки б) кочерыжка в) лист | - | |
Капуста отварная | те же части | ||
Отвар |
Б. Определение нитратов в целых растениях
Отрезают у свежих растений части в виде толстых срезов: куски стеблей, черешков, плодов. Кладут их на полоску восковой бумаги. Капают на различные части среза по несколько капель 1 %-го раствора дифениламина в серной кислоте, отмечают окрашивание согласно вышеприведенной шкале. При этом в случае малых концентраций нитратов в продукции и при отсутствии синей окраски может наступить порозовение ткани, вследствие её обугливания от H2SO4 в реактиве дифениламина.
Указанный метод дает возможность оценить и сравнить разные ткани овощных и других растений прямо в поле. Он проверен и хорошо действует на хлебных злаках, картофеле, корнеплодах, овощах, бобовых, многолетних травах для оценки обеспеченности различных сельхозкультур азотом. Показано, что нитраты исчезают в фазе цветения, но их много в период вегетационного роста, который и должен быть использован для оценки. Нитраты сразу утилизируются (не проявляются в анализах) в меристимах и почках, бутонах и цветках различных сельхозкультур.
В. Определение нитратов методом ионоселективных электродов
На 10 г свежеразмолотых плодов или овощей наливают 50 мл 1 %-го раствора алюмокалиевых квасцов. Анализ проводят в стаканчиках на 100 мл, взбалтывают 3-5 мин. Определяют ионоселективными электродами на нитрат-ион с использованием потенциометра (рН-метра). Калибровку делают по KNO3.
Приготовление реактивов
1. 1 %-ый раствор дифениламина в серной кислоте 1 г дифениламина растворяют в 99 г концентрированной серной кислоты (плотностью 1,84). Это соответствует приблизительно 54 мл Н2SO4.
Расчет:
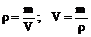 = 53,8мл,
= 53,8мл,
где r – плотность,
m – масса,
V – объем.
2. Исходный раствор NaNO3 для построения калибровочной кривой.
Если растворить 1 г NaNO3 в 1 л воды, то это будет соответствовать 729 мг/кг нитратов (по нитрат-иону):
85 – 1000 мг (1 г)
62 – Х
X =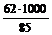 = 729 мг/кг,
= 729 мг/кг,
где 85 – молекулярный вес NaNO3,
62 – молекулярный вес нитрат-иона (NO3-).
Однако, согласно табл. 1, наибольшее содержание нитратов в распространенных видах овощей – 3000 мг/кг.
729 – 1000 мг (1 г)
3000 – X
Х=![]() = 4,11 г,
= 4,11 г,
то есть надо растворить 4,11 г соли в литре дистиллированной воды. Однако при небольшом количестве анализов в учебных целях достаточно и 100 мл, то есть 411 г NaNO3 нужно растворить в100 мл воды.
Работа № 13. Уменьшение содержания хлорофилла
в листьях растений – биоиндикационный признак
неблагоприятных условий среды. Определение
хлорофилла фотометрически
Сведения относительно использования содержания хлорофилла (и других пигментов) как биоиндикационных признаков в литературе противоречивы. Ряд немецких ученых считает этот признак недостаточно информативным и специфичным (Биоиндикация загрязнений… 1988), хотя первой стадией видимых хлорозов листьев как раз и является разрушение хлорофилла под влиянием неблагоприятных факторов. В то же время другие исследователи, в том числе русские и украинские, показали, что у чувствительных к загрязнению видов (липы, клена) наблюдается снижение содержания хлорофилла еще до появления видимых изменений и это может служить достаточно надежным неспецифическим биоиндикационным признаком.
Неспецифичность этого индикатора в том, что недостаток в почве азота, а также железа и других элементов, быстро сказывается на окраске листьев в результате разрушения хлорофилла в них и, этот признак очень часто используется для оценки низкого плодородия почв. Это надо учитывать и использовать этот показатель при биоиндикации в сочетании с другими признаками.
По нашим данным, для оценки степени загрязнения наземных экосистем или их составляющих листья следует собирать из средней части кроны в первой половине вегетации, учитывая условия произрастания (освещенность, минеральное питание, обводненность и др.). В качестве биоиндикаторов в городской среде рекомендуется использовать следующие газочувствительные виды: липу мелколистную, клен платанолистый, каштан конский, ель обыкновенную, сосну обыкновенную.
Метод основан на извлечении хлорофилла из листьев растворителями (спирт, ацетон) и определении его количества на фото-элекроколориметре или спектрофотометре.
Оборудование, реактивы, материалы
1) торзионные весы; 2) фотоэлектроколориметр – ФЭК; 3) насос Камовского или электрический; 4) колба Бунзена с пробкой и стеклянным фильтром № 2, № 3; 5) ступки малые с пестиками; 6) стеклянные палочки; 7) ножницы;
8) толченое и просеянное стекло; 9) мерные колбы на 100 и 50 мл; 10) калька; 11) вазелин; 12) фильтровальная бумага; 13) медный купорос CuSO4 • 5Н2О; 14) биохромат калия К2Сr2О7, 15) 7 %-ый раствор аммиака; 16) листья растений-индикаторов, собранные в «загрязненной» и «чистой» зонах.
Для учебной работы можно использовать и комнатные растения, выращенные специально в сосудах на гумусной почве с поливом водой и на малоплодородной почве с поливом раствором соли какого-либо тяжелого металла.
P. S. В случае отсутствия колбы Бунзена, стеклянных фильтров и насоса, их можно заменить центрифугированием вытяжки хлорофилла.
Ход работы
Определение хлорофилла в листьях можно проводить как на свежем, так и на фиксированном материале. Фиксацию осуществляют текучим паром (5 мин) или сухим жаром (при 105 °С в течение 5-10 мин).
(1963) предложил следующий способ фиксации для сохранения хлорофилла: листья нарезают мелкими кусочками, заворачивают в марлю и погружают в кипящий насыщенный раствор поваренной соли на
1-2 минуты. За это время материал обезвоживается и ферменты убиваются. Затем материал промывают проточной водой в течение 0,5 минуты, встряхивают для удаления влаги. Высушивают в тени не менее 2-х суток или в термостате при температуре не выше 40 °С. (1971) считал, что лучшие результаты дает сочетание фиксации материала горячим паром (2 мин) с проведением быстрой экстракции на холоде.
При работе с сухим материалом берут навеску 0,5-1 г, со свежим – 1-2 г. Предварительно определяют влажность листьев. Навеску растительного материала (исключая жилки) тщательно измельчают в фарфоровой ступке с битым стеклом, добавляя мел или углекислый магний. Извлечение хлорофилла из сухого материала можно производить 90 %-ым спиртом или 80-85 %-ым ацетоном, а из свежего – 96-98 %-ым спиртом или абсолютным ацетоном.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



