6. Реакция Фоля на серосодержащие аминокислоты
При нагревании растворов белка со щелочью и плюмбитом жидкость окрашивается в бурый или черный цвет.
|
Серосодержащая аминокислота метионин (метил-тио-аминомасляная кислота) более устойчива и при слабом щелочном гидролизе не разрушается. Реакция протекает по следующему уравнению:
|
Интенсивность окраски зависит от количества серосодержащих аминокислот в белке и от концентрации белка в растворе.
Ход работы. В пробирку налить 5 капель 1%-го раствора яичного белка, 5 капель 30%-го раствора едкого натра и одну каплю 5%-го раствора уксуснокислого свинца. При длительном нагревании жидкость буреет и выпадает черный осадок уксуснокислого свинца. То же проделать с 1%-м раствором желатина.
7. Реакция Сакагучи на аргинин
Производные хинониминов (в данном случае нафтохинониминов), у которых водород аминогруппы замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона. Оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина. Механизм реакции аргинина с α-нафтолом в присутствии окислителя можно представить следующим образом:
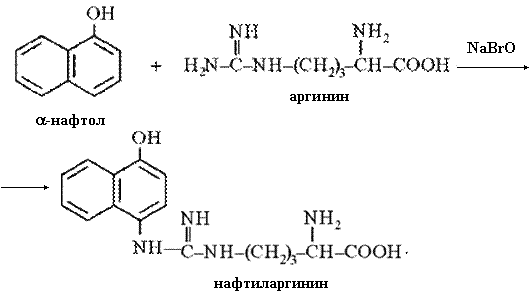 |
При дальнейшем окислении нафтиларгинина образуется соединение типа хинонимина:
 |
Ход работы. В пробирку налить 5 капель 0,01%-го раствора яичного белка, прибавляют 5 капель раствора гидроксида натрия и 1 – 2 капли 0,2%-го спиртового раствора α-нафтола. Хорошо перемешивают содержимое пробирки, приливают 1 – 2 капли раствора гипобромита и вновь перемешивают. Немедленно добавляют 2 капли 40%-го раствора мочевины для стабилизации быстроразвивающегося оранжево-красного окрашивания.
Контрольные вопросы
1. Перечислите цветные реакции на аминокислоты.
2. Как доказать присутствие аминокислот, имеющих в своем составе бензольное кольцо?
3. Назовите содержащие серу аминокислоты. С помощью какой реакции можно их открыть?
4. Что открывает нингидриновая реакция?
5. Какие аминокислоты можно обнаружить диазореакцией?
6. Какие реакции доказывают наличие белка в растворе?
7. Можно ли с помощью цветных реакций судить об аминокислотном составе белков?
8. Какую цветную реакцию можно использовать для количественного определения белков?
Задание на дом
1. Выучить формулы аминокислот, уметь составлять пептиды.
2. Первичная структура белков.
Занятие 2
Теоретическая часть
1. Контрольная работа по классификации аминокислот:
а) 1 и 3 классы аминокислот;
б) 2 и 4 классы аминокислот.
2. Написание полипептидов заданного аминокислотного состава.
Практическая часть
Исследование аминокислотного состава белков
С помощью цветных реакций на отдельные аминокислоты (занятие 1) сравнить аминокислотный состав двух неизвестных белков. Результаты работы оформить в таблицу и сделать выводы об аминокислотном составе белков.
Название реакции | Белок 1 | Белок 2 |
Задание на дом
1. Подготовка к контрольной работе по написанию полипептидов.
2. Методы изучения первичной структуры белков.
Занятие 3
Теоретическая часть
1. Контрольная работа по написанию пептидов.
Напишите формулы следующих пептидов:
а) вал-сер-про-глн-лей-три-лиз-асп-ала-иле;
б) гли-глу-цис-тре-асн-арг-тир-гис-мет-фен;
в) про-мет-асн-арг-тир-глу-лиз-гли-ала-цис;
г) глн-вал-три-асп-иле-сер-тре-гис-лей-фен.
Укажите:
а) гидрофобные радикалы;
б) гидрофильные радикалы;
в) кислотные радикалы;
г) основные радикалы.
2. Решение задач по методам изучения первичной структуры белка.
Задача 1.
Укажите, какие пептиды получаются при действии химотрипсина на полипептид, имеющий первичную структуру: сер-тир-мет-глу-гис-фен-арг-три-гли-лиз-вал-гли-лиз-лиз-вал-тир-асп-глн-ала-асп-лей-три-лиз-фен-иле-тре-сер-вал. На полученные пептиды воздействовали динитрофторбензолом, образовавшиеся ДНФ-пептиды гидролизовали 20%-м раствором соляной кислоты. Какие ДНФ-аминокислоты образуются в результате реакций?
Задача 2.
Согласно условиям, изложенным в задаче 1, на полипептид, имеющий первичную структуру, указанную выше, воздействовали трипсином. Какие ДНФ-производные образуются в этом случае?
Задача 3.
Тетрапептид содержит в своем составе аланин, лизин, пролин, валин. В результате реакций тетрапептида с динитрофторбензолом и последующего гидролиза ДНФ-пептида 20%-м раствором соляной кислоты был получен ДНФ-аланин. Гидролиз тетрапептида трипсином дает два соединения, одно из которых окрашивается нингидрином в сине-фиолетовый, а другое – в желтый цвет. Какова первичная структура тетрапептида?
Задача 4.
В гидролизате пептида найдены ала, вал, глу, фен, тир, гли, лиз, лей, мет, NH3. При обработке пептида по методу Сенгера выделен ДНФ-аланин, карбоксипептидазой – глицин. В триптическом гидролизате обнаружены два пептида: первый состоит из вал, ала, глн, лиз, фен; второй – из мет, гли, лей, тир и при обработке по Сенгеру дает ДНФ-лейцин. В химотриптическом гидролизате найдены три пептида: первый содержит мет и гли; второй – вал, ала, фен, глн; третий – лей, тир, лиз. Выведите на основании всей совокупности данных первичную структуру исходного пептида.
Задача 5.
При исследовании Ф. Сенгером первичной структуры цепи А инсулина быка было показано, что она содержит 21 аминокислотный остаток, а именно гли, ала, вал2, лей2, иле, цис4, асп2, глу4, сер2, тир2. Обработка полипептида динитрофторбензолом с последующим гидролизом привела к ДНФ-глицину, карбоксипептидазой – к аспарагиновой кислоте. При действии на цепь А инсулина быка пепсином, были получены пептиды: глу-цис-цис-ала-сер-вал-цис-сер-лей, гли-иле-вал-глу, асп-тир-цис-асп, тир-глу-лей-глу; химотрипсином – сер-лей-тир, глу-лей-глу-асп-тир, цис-асп, гли-иле-вал-глу-глу-цис-цис-ала-сер-вал-цис. Исходя из этих данных, выведите первичную структуру цепи А инсулина быка.
Задача 6.
Лей-энкефалин – это полипептид, выделенный из нормальной мозговой ткани. Он относится к группе опиоидов. Роль их в том, что они присоединяются к специфическим рецепторам, которые связывают опиаты, такие как морфин, налаксон.
Исследователи рассматривают эти полипептиды как содержащиеся в мозгу собственное средство анастезии. Наша задача определить аминокислотную последовательность этого полипептида, исходя из следующих данных о нем:
1. Полный гидролиз выявил присутствие гли, лей, фен и тир в молярном отношении 2:1:1:1.
2. После обработки ДНФБ с последующим гидролизом и хроматографическим разделением было выявлено присутствие 2,4-динитрофенильного производного тирозина.
3. Частичный гидролиз с использованием химотрипсина дал лей, тир, а также более короткий пептид.
4. Полный гидролиз короткого пептида выявил присутствие в нем гли, фен в отношении 2:1.
Какова первичная структура этого полипептида?
Задача 7.
Структура полипептидного антибиотика, выделенного из Bacillus brevis. Этот пептид образует комплексы с ионами металлов и, по-видимому, нарушает систему ионного транспорта через клеточную мембрану, убивая определенные виды бактерий. Структура полипептида была установлена на основе следующих наблюдений:
а) Полный кислотный гидролиз пептида, как показал последующий аминокислотный анализ, привел к образованию эквимолярных количеств лей, орн, фен, про и вал. Орн – сокращенное обозначение орнитина – аминокислоты, не встречающейся в белках, но присутствующей в некоторых пептидах. Он имеет следующее строение:
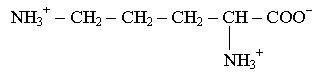 |
б) измерение молекулярной массы дали приблизительную величину 1200.
в) пептид не подвержен гидролизу под действием фермента карбоксипептидазы.
г) Обработка исходного пептида динитрофторбензолом с последующим полным гидролизом образовавшегося производного и хроматографирование полученных продуктов дает лишь свободные аминокислоты и производное следующего строения:
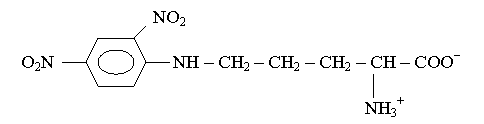 |
(Подсказка: учтите, что 2,4-динитрофенильная группа присоединилась не к α-азоту, как это обычно имеет место, а к аминогруппе боковой цепи).
д) Частичный гидролиз полипептида с последующим хроматографическим разделением полученных продуктов и определением в них аминокислотных последовательностей дал следующие ди - и трипептиды:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



