лей-фен вал-орн-лей орн-лей вал-орн
фен-про про-вал-орн фен-про-вал.
Определите первичную структуру этого полипептидного антибиотика.
Задача 8.
В химии белка часто используются следующие реактивы: CNBr, дансихлорид, 6N HCl, нингидрин, трипсин, фенилизотиоцианат, надмуравьиная кислота, химотрипсин. Какой из этих реактивов следует применить при решении следующих задач:
а) Расщепление пептидных связей по карбоксильной группе метионинов.
б) Гидролиз пептидных связей по карбоксильным группам остатков лизина и аргинина.
в) Определение последовательности аминокислот в небольшом пептиде.
г) Гидролиз пептидных связей по карбоксильной группе ароматических аминокислотных остатков.
д) Идентификация аминокислотного остатка в пептиде (количество которого составляет 10-7 г).
е) Определение свободных аминокислот.
Задание на дом
Подготовиться к семинару «Структурная организация белковой молекулы».
Занятие 4
Теоретическая часть
1. Семинарское занятие по теме «Структурная организация белковой молекулы».
2. Тестирование по теме «Уровни структурной организации белковой молекулы».
I. Выберите один правильный ответ:
1. Нейтральной аминокислотой является:
а) аргинин
б) лизин
в) валин
г) аспарагиновая кислота
д) гистидин
2. Впервые аминокислотная последовательность была расшифрована для:
а) рибонуклеазы
б) гемоглобина
в) цитохрома с
г) вазопрессина
д) инсулина
3. Первичная структура белка не характеризуется тем, что:
а) в ее формировании участвуют слабые связи
б) закодирована генетически
в) образована ковалентными связями
г) определяет последующие уровни структурной организации белка
4. Пептидная связь в белках является:
а) одинарной
б) двойной
в) частично одинарной и частично двойной
5. Водородные связи образуются между радикалами аминокислот:
а) Сер, Асн
б) Ала, Вал
в) Глу, Асп
г) Цис, Три
д) Асп, Арг
6. В α-спирали белка связи:
а) перпендикулярны оси спирали
б) параллельны оси спирали
в) водородная связь замыкается через три аминокислотных остатка
г) водородная связь замыкается через четыре аминокислотных остатка
7. Вторичная структура белка открыта:
а) Д. Уотсоном и Ф. Криком
б) Э. Фишером
в) Л. Полингом
г) Ф. Сэнгером
д) Д. Эдманом
8. Препятствует образованию α-спирали аминокислотный остаток:
а) аланина
б) серина
в) валина
г) пролина
д) глутамина
9. Вторичная структура природных белков представлена:
а) только α-спиралью
б) только β-спиралью
в) участками аморфными, α-спирали, β-структуры
г) участками α-спирали и β-структуры
10. В формировании третичной структуры белка не участвует связь:
а) водородная
б) пептидная
в) дисульфидная
г) гидрофобное взаимодействие
11. В стабилизации четвертичной структуры не участвует связь:
а) ионная
б) дисульфидная
в) водородная
г) гидрофобное взаимодействие
д) пептидная
12. Формирование четвертичной структуры белка является:
а) генетически закодированным
б) самопроизвольным, взаимодействие протомеров осуществляется любой частью их поверхности
в) самопроизвольным, протомеры взаимодействуют определенным участком
13. Белки выполняют различные функции, кроме:
а) структурной
б) каталитической
в) регуляторной
г) генетической
д) рецепторной
14. В процессе функционирования белковые молекулы:
а) сохраняют жестко зафиксированную пространственную конформацию
б) происходит существенное изменение пространственной структуры
в) претерпевают небольшие конфирмационные изменения (флуктуации)
П. Выберите правильные ответы:
1. Цветные реакции позволяют судить о:
а) присутствии белков в биологических жидкостях
б) первичной структуре белков
в) присутствии некоторых аминокислот в белке
г) количестве аминокислот в белке
д) функции белков
2. Олигомерный белок:
а) состоит из нескольких протомеров
б) имеет полипептидные цепи, связанные дисульфидными связями
в) содержит контактные поверхности протомеров, комплементарные друг другу
г) может связывать только один лиганд
д) формирует четвертичную структуру путем самосборки
3. Радикалы аминокислотных остатков полипептидной цепи не участвуют в формировании структур молекулы белка:
а) первичной
б) вторичной
в) третичной
г) четвертичной
III. Выберите один неправильный ответ:
1. Водородные связи могут образовываться между радикалами аминокислот:
а) Сер, Глн
б) Три, Асп
в) Тре, Лиз
г) Глу, Цис
д) Асп, Сер
2. Гидрофобные связи могут образовываться между радикалами аминокислот:
а) Лей, Мет
б) Три, Иле
в) Ала, Тре
г) Вал, Фен
д) Мет, Про
3. К слабым связям, участвующим в образовании нативных белков, относятся:
а) пептидные
б) водородные
в) гидрофобные
г) ионные
д) ван-дер-ваальсовы взаимодействия
4. Гидрофобные радикалы аминокислот чаще всего располагаются:
а) внутри глобулярных цитозольных белков
б) в местах контактов протомеров олигомерных белков
в) на поверхности цитозольных белков
г) на поверхности интегральных мембранных белков
д) в активном центре белков
IV. Установите соответствие:
1) А. Первичная структура
Б. Вторичная структура
В. Третичная структура
Г. Супервторичная структура
Д. Конформация
1. Стабилизируется водородными связями между атомами пептидного остова
2. В ее формировании принимают участие гидрофобные взаимодействия радикалов аминокислот
3. Фиксируется ковалентными связями между α-амино - и α-карбоксильными группами аминокислот
2) А. Асн
Б. Гли
В. Ала
Г. Глу
Д. Лиз
1. Аминокислота, образующая ионную связь с Асп
2. Аминокислота, располагающаяся внутри цитозольного глобулярного белка
3. Аминокислота, не имеющая радикала
3) А. Первичная структура
Б. Вторичная структура
В. Третичная структура
Г. Супервторичная структура
Д. Четвертичная структура
1. Порядок чередования аминокислот, соединенных пептидной связью
2. Пространственная структура, образованная водородными связями, возникающими между атомами пептидного остова
3. Специфический порядок чередования вторичных структур
V. Выберите один наиболее полный ответ:
1. В белках водородные, ионные и гидрофобные связи участвуют в формировании:
а) вторичной структуры
б) третичной структуры
в) супервторичной структуры
г) первичной структуры
д) конформации
2. Конформация белка:
а) аминокислотная последовательность полипептидной цепи
б) число полипептидных цепей в олигомерном белке
в) укладка α-спиралей и β-структур в полипептидной цепи
г) характерное строение супервторичной структуры
д) пространственная структура белка
3. Четвертичная структура белка - это:
а) способ укладки полипептидной цепи в виде α-спирали
б) способ укладки полипептидной цепи в виде β-структуры
в) количество протомеров, их расположение относительно друг друга и характер связей между ними в олигомерном белке
г) порядок чередования аминокислот в полипептидной цепи
д) фрагмент пептидного остова
е) способ укладки полипептидной цепи в пространстве
Задание на дом
Физико-химические свойства белков.
Занятие 5
Теоретическая часть
1. Физико-химические свойства белков.
2. Решение задач по физико-химическим свойствам белков.
Задача 1.
Укажите, в каком направлении будут передвигаться в электрическом поле (т. е. будут ли они двигаться к аноду или к катоду или будут оставаться на старте) следующие белки: 1) яичный альбумин при рН 3,0 и 5,0; 2) рибонуклеаза рН 4,2; 9,45 и 11,3. Изоэлектрическая точка яичного альбумина – 4,6; рибонуклеазы – 9,45.
Задача 2.
При каких значениях рН наиболее целесообразно электрофоретическое фракционирование нижеперечисленных белковых смесей: 1) миозина и гемоглобина; 2) цитохрома С и гемоглобина; 3) сывороточного альбумина, уреазы и гемоглобина? Изоэлектрическая точка миозина 5,4; гемоглобина – 6,8; цитохрома С – 10,65; уреазы – 5,0; сывороточного альбумина – 4,9.
Задача 3.
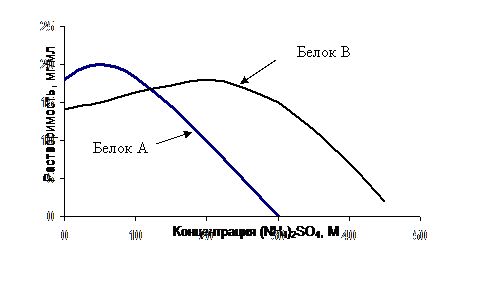
Чистые белки большей частью нерастворимы в дистиллированной воде, но растворяются в разбавленных солевых растворах. Однако при добавлении к водному раствору белка нейтральных солей в высокой концентрации белок выпадает в осадок. Это явление называют высаливанием. Например, большая часть белков растворяется в 0,1 М (NH4)2SO4, но выпадает в осадок если концентрация (NH4)2SO4 повышается до 3 М. После удаления избытка (NH4)2SO4 путем диализа белки снова растворяются. Попытайтесь объяснить на молекулярном уровне, почему добавление солей в высоких концентрациях приводит к понижению растворимости белка.
На графике показана зависимость растворимости двух белков от концентрации (NH4)2SO4. Как можно использовать эти данные для разделения белков А и В?
3. Тестирование по теме «Физико-химические свойства белков».
I. Выберите один правильный ответ:
1. Что общего между нативной и денатурированной рибонуклеазой:
а) первичная структура
б) конформация
в) строение активного центра
г) межрадикальные связи
д) функция
2. Пептид, плохо растворимый в воде:
а) Глу - Цис - Лиз
б) Глн - Асп - Фен
в) Арг - Сер - Про
г) Мет - Ала - Лей
д) Асн - Лиз - Гис
3. Пептид, лучше других растворимый в воде при рН 7,0:
а) Асп - Тре - Лиз
б) Асн - Мет - Фен
в) Про - Сер - Ала
г) Цис - Гли - Три
д) Лей - Про - Глн
4. Пептид, изоэлектрическая точка которого находится в кислой среде:
а) Гли - Тре - Лиз
б) Глу - Сер - Арг
в) Мет - Асп - Тир
г) Асн - Лиз - Гис
д) Ала - Про – Лей
5. Что происходит с белковой молекулой при проведении электрофореза в условиях, когда рН буферного раствора выше, чем изоэлектрическая точка белка:
а) мигрирует к аноду
б) мигрирует к катоду
в) остается на линии старта
г) подвергается гидролизу
6. Белки характеризуются:
а) отсутствием способности кристаллизоваться
б) сохранением нативной структуры молекулы при нагревании до 100°С

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



