ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ПОУ ВПО «ИРКУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Биолого-почвенный факультет
Малый практикум по биохимии
Часть I

Иркутск, 2008
Печатается по решению научно-методического совета
Иркутского государственного университета
Рецензент:
д. б.н., гл. н.с. лаборатории физиологической генетики СИФИБР СО РАН
Методические указания по биохимии предназначены для студентов 2 курса специальностей «Биология» и «Микробиология» очного обучения и студентов 3 курса специальности «Микробиология» очно-заочного обучения и включают лабораторные работы, задачи, контрольные вопросы и итоговые тесты по двум основным темам курса - «Структура, свойства и функции белков» и «Структура и функции нуклеиновых кислот» к общепрофессиональной дисциплине "Биохимия".
Составители:
к. б.н., доцент кафедры физиологии растений и клеточной биологии
к. б.н., доцент кафедры физиологии растений и клеточной биологии
к. б.н., доцент кафедры физиологии растений и клеточной биологии
Биология 020201
Микробиология 020209
СТРУКТУРА, СВОЙСТВА И ФУНКЦИИ БЕЛКОВ
Занятие 1
Теоретическая часть
1. Правила работы в лаборатории, техника безопасности. Зачет по технике безопасности.
2. Программа практикума по биохимии и форма отчетности.
3. Аминокислоты – структурные элементы белковой молекулы. Структурные особенности аминокислот, образующих белковую молекулу.
Практическая часть
Цветные реакции на отдельные аминокислоты,
входящие в состав белковых молекул
Значение цветных реакций состоит в том, что они дают возможность обнаружить присутствие белка в биологических жидкостях, растворах и установить аминокислотный состав различных природных белков. Эти реакции применяются как для качественного, так и для количественного определения белка и содержащихся в нем аминокислот. Некоторые реакции присущи не только белкам, но и другим веществам, поэтому недостаточно проведения одной какой-либо реакции для установления наличия белка.
Существует два типа цветных реакций:
1. универсальные – биуретовая (на все белки) и нингидриновая (на все аминокислоты и белки);
2. специфические – только на определенные аминокислоты как в молекуле белка, так и в растворах отдельных кислот, например, реакция Фоля (аминокислоты, содержащие слабосвязанную серу).
Цветные реакции на белки проводят с 1% раствором яичного белка и 1% раствором желатина.
1. Биуретовая реакция (Пиотровского) на пептидную
связь в белковой молекуле
При добавлении к щелочному раствору белка раствора сернокислой меди жидкость приобретает красно-фиолетовое или сине-фиолетовое окрашивание. Реакция обусловлена присутствием в белке пептидных связей, которые с ионами меди образуют окрашенные солеобразные комплексные соединения. Схематично полипептид изображают следующим образом:
|
Реакцию можно представить в следующем виде:

Окраска биуретового комплекса зависит от количества медной соли в растворе и от структуры вещества, с которым координирован ион меди. Продукты распада белка – пептоны и полипептиды – дают биуретовую реакцию с красным оттенком.
Ход работы. В пробирку налить 5 капель 1%-го раствора яичного белка, во вторую пробирку то же количество 1%-го раствора желатина, в обе пробирки добавить 5 капель 10%-го раствора едкого натра и 1 каплю 1%-го раствора сернокислой меди. Появляется красно-фиолетовое (или сине-фиолетовое) окрашивание.
При малой концентрации белка в растворе биуретовую реакцию проводят следующим образом. В пробирку наливают 20 капель 10%-го раствора едкого натра, добавляют 1 – 2 капли 1%-го раствора сернокислой меди и перемешивают. Затем набирают в пипетку разбавленный раствор белка и осторожно спускают его по стенке пробирки так, чтобы он наслаивался сверху и не смешивался со щелочным раствором сернокислой меди. На границе двух слоев жидкости образуется фиолетовое кольцо.
2. Нингидриновая реакция на α-аминокислоты
При нагревании α-аминокислот с нингидрином появляется синее окрашивание. Это объясняется тем, что при взаимодействии с нингидрином α-аминокислоты окисляются и распадаются с образованием аммиака, альдегида и угольной кислоты. Нингидрин восстанавливается и конденсируется с другой частицей нингидрина и аммиаком. В результате образуется сложное соединение мурексидного строения, окрашенное в синий цвет. Реакция может быть представлена в следующем виде:
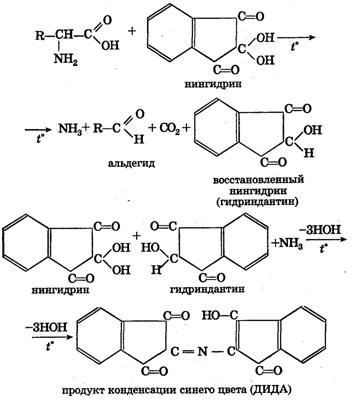 |
Ход работы. Налить в одну пробирку 5 капель 1%-го раствора желатина, в другую – 5 капель 1%-го раствора яичного белка. В обе пробирки добавить 2 – 3 капли 0,1%-го раствора нингидрина. Содержимое обеих пробирок нагреть до кипения. Через 1 – 2 минуты появляется розовое, красное, а затем и синее окрашивание. При стоянии интенсивность окраски увеличивается.
3. Ксантопротеиновая реакция на циклические
аминокислоты (Мульдера)
При нагревании растворов большинства белков с концентрированной азотной кислотой жидкость окрашивается в лимонно-желтый цвет, переходящий при подщелачивании в оранжевый. Реакция обусловлена присутствием в белке циклических аминокислот – фенилаланина, тирозина (п-оксифенилаланина) и триптофана (индолилаланина), которые при взаимодействии с концентрированной азотной кислотой образуют нитропроизводные желтого цвета (реакция нитрования):
 |
фенилаланин тирозин триптофан
Последние при добавлении щелочи превращаются в соли хиноидной структуры, окрашенные в оранжевый цвет. Белки, в которых циклические аминокислоты отсутствуют, не дают ксантопротеиновой реакции. К таким белкам относятся: желатин, клупеин, сальмин и др. Реакция нитрования тирозина может быть изображена следующим образом:
![]()

Аналогично протекает реакция нитрования триптофана и фенилаланина (последний нитруется труднее).
Ход работы. В одну пробирку налить 5 капель 1%-го раствора яичного белка, в другую – 5 капель 1%-го раствора желатина. В обе пробирки добавить 2 – 3 капли концентрированной азотной кислоты и нагреть. Жидкость окрашивается в лимонно-желтый цвет. После охлаждения добавить 10 капель концентрированного раствора аммиака или 30%-го раствора едкого натра. Окраска жидкости переходит в оранжевую.
4. Диазореакция на гистидин и тирозин (Паули)
При добавлении диазореактива к щелочному раствору гистидина или тирозина раствор приобретает оранжево-красное окрашивание.
 Реакция обусловлена тем, что гистидин и тирозин, реагируя с диазобензосульфокислотой, образует азокраситель красного цвета. Реакция может быть представлена в следующем виде:
Реакция обусловлена тем, что гистидин и тирозин, реагируя с диазобензосульфокислотой, образует азокраситель красного цвета. Реакция может быть представлена в следующем виде:
Интенсивность получаемой окраски зависит от количества гистидина и тирозина. Реакция Паули не является строго специфичной для гистидина и тирозина. Ее дают вещества, имеющие в своей структуре фенольное, имидазольное, пиррольное или тиазоловое кольцо (адреналин, тиамин, карнозин, желчные пигменты, гистамин и др.).
Диазобензосульфокислота – очень неустойчивое соединение, с течением времени разрушается, поэтому диазотирование сульфаниловой кислоты лучше проводить ex tempore и на холоде. Реакция диазотирования протекает по уравнению:
 |
Ход работы. В две пробирки налить по 3 капли раствора сульфаниловой кислоты в 2%-й соляной кислоте и 3 капли 5%-го раствора азотистокислого натрия. Содержимое пробирок перемешать. К полученному диазореактиву прибавить: в одну пробирку – 5 капель 1%-го раствора яичного белка, в другую – 5 капель 1%-го раствора желатина. В обе пробирки прилить по 5 капель 10%-го раствора соды. Жидкость в обеих пробирках окрашивается в красный цвет.
5. Реакция на триптофан Шульца-Распайля
Если к раствору триптофана добавить концентрированную уксусную кислоту или тростниковый сахар, а затем осторожно по стенке пробирки спускать из пипетки концентрированную серную кислоту, то на границе двух жидкостей образуется красно-фиолетовое кольцо.
Реакция обусловлена тем, что триптофан, реагируя с глиоксилевой кислотой, присутствующей в виде примесей в концентрированной уксусной кислоте, или с оксиметилфурфуролом, образующимся из фруктозы, дает окрашенные продукты конденсации. Концентрированная серная кислота принимает участие в реакции в качестве водоотнимающего вещества. Ход превращения триптофана может быть представлен в следующем виде:
 |
продукт конденсации триптофана с глиоксилевой кислотой
Ход работы. Налить в пробирку 5 капель 1%-го раствора яичного белка, добавить каплю 10%-го раствора сахарозы и подслоить равным объемом концентрированной серной кислоты. На границе двух жидкостей образуется красно-фиолетовое кольцо. В кипящей водяной бане окраска развивается быстрее. То же самое проделать, взяв вместо яичного белка 1%-й раствор желатина.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



