В зависимости от тяжести клинических проявлений, пациенты распределялись по пятибалльной шкале, согласно Международной клинической классификации MGFA (Barohn R. J. et al., 1998):
1 – изолированная слабость только окулярных мышц;
2 – легкая слабость мышц туловища, проксимальных отделов конечностей, а также вовлечение в процесс орофарингеальных мышц;
3 – умеренная слабость мышц туловища, проксимальных отделов конечностей, а также вовлечение в процесс орофарингеальных или дыхательных мышц;
4 – выраженная слабость мышц туловища, проксимальных отделов конечностей, а также вовлечение в процесс орофарингеальных или дыхательных мышц;
5 – интубация, или нахождение пациента на искусственной вентиляции легких.
А – бульбарные нарушения отсутствовали; В – присутствовали бульбарные нарушения.
Электромиографические методы
Как один из методов электромиографии использовался стандартный метод непрямой ритмической супрамаксимальной стимуляции мышцы с регистрацией М-ответа поверхностными электродами (декремент-тест). Учитывая то, что в исследовании, как правило, принимали участие пациенты с генерализованной формой заболевания, тест проводился на дельтовидной мышце (Рис. 1). У больных с выраженными бульбарными расстройствами дополнительно исследовалась двубрюшная мышца. Во всех случаях за 12-24 часа до исследования отменялись ингибиторы ацетилхолинэстеразы. При изучении функционального состояния нервно-мышечной передачи оценивали следующие параметры: амплитуду негативной фазы М-ответа в ответ на одиночный супрамаксимальный стимул (в мВ); величину декремента амплитуды М-ответа при стимуляции мышцы частотой 3 имп/с по отношению 5-го М-ответа к 1-му (в %).
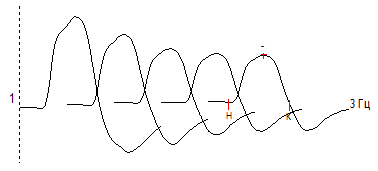
Рисунок 1. Декремент М-ответа -43% при миастении у больного К, 35 лет. Стимуляция подмышечного нерва с частотой 3 Гц; отведение с дельтовидной мышцы. Исследование нервно-мышечной передачи у пациентов проводилось на электромиографе «Нейро-МВП-Микро» фирмы «Нейрософт».
Фармакологические пробы
Для объективизации обратимости блока нервно-мышечной передачи миастенического типа проводилась проба с введением прозерина. По истечении 12- 24 часов после отмены ингибиторов ацетилхолинэстеразы проводится клиническое и ЭМГ обследования, после чего вводится 0,05% раствор прозерина. Через 40-50 минут после инъекции процедуру клинического осмотра и ЭМГ обследования повторяют по тому же протоколу. Проба считалась положительной в случае нарастания мышечной силы и уменьшения выраженности декремента М-ответа при повторном ЭМГ тестировании через 40-50 минут. Для уменьшения возможных побочных явлений в ответ на стимуляцию мускариновых холинорецепторов после введения прозерина, при необходимости вводилось подкожно 0,2-0,3 мл 0,1% раствора атропина.
Иммунологические методы
Иммунологическое исследование выполнялось в лаборатории полисистемных исследований (руководитель – доктор биологических наук, профессор ) НИИ общей патологии и патофизиологии РАМН.
Концентрацию антител к ацетилхолиновым рецепторам определяют радиоиммунологическим методом с помощью коммерческой тест-системы (DLD Diagnostika GMBH, Германия). Образцы сыворотки крови хранят при -200С. Перед проведением анализа сыворотки размораживают, отбирают аликвоты по 5 мкл и помещают в пробирки. К пробам добавляют по 100 мкл 125 I-рецептора ацетилхолина, 50 мкл антител к IgG человека, перемешивают и инкубируют в течение 30 мин при комнатной температуре. Затем добавляют по 1 мл промывочного буфера, центрифугируют (3000 g 20 минут), надосадочную жидкость удаляют декантацией. Осадок ресуспензируют и повторяют процедуру промывки. Определяют радиоактивность проб и вычисляют концентрацию антител в нмоль/л по формуле. Повышенной концентрацией антител к АХР считается значение, превышающее 0,50 Нмоль/л.
Статистическая обработка материала
Все данные были обработаны на персональном компьютере с помощью пакета программ STATISTICA 6.0 (Stastistica Inc., USA). Для проверки нормальности распределения полученных данных использовался метод Колмогорова – Смирнова. Учитывая нормальное распределение показателей при обработке результатов, приведенных в настоящей работе, использовались параметрические методы, такие как критерий Стьюдента и дисперсионный анализ с вычислением вероятности ошибки «р». Уровень доверительной вероятности во всех типах анализа р<0,05 рассматривали как статически значимый.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Данные, полученные в результате настоящего исследования, позволяют обсудить ряд вопросов связанных с патогенезом миастении и, в частности, роли аутоантител к АХР, как критерия оценки эффективности патогенетической терапии.
Благодаря возросшим методологическим возможностям экспериментальных и клинических иммунологических исследований осуществлен прорыв в понимании патогенеза целого ряда аутоиммунных заболеваний, среди которых оказалась и миастения. Методы, основанные на выявлении иммунного субстрата болезни в виде аутоантител к разным структурам нервно-мышечного соединения и, прежде всего, к субъединицам АХР, сегодня являются золотым стандартом при диагностике миастении, т. к. повышение концентрации этих антител наблюдается в 80-85% случаев. Вместе с тем, несмотря на высокую диагностическую значимость повышения концентрации антител к АХР, в подавляющем большинстве исследований не выявлено корреляции между выраженностью клинических проявлений миастении и концентрацией аутоантител к АХР ( и др., 2006; , 2012; Lindstrom J., 1997; Aurangzeb S. et al., 2009).
Результаты нашего исследования по определению содержания антител к АХР при миастении выявили ассоциацию клинического улучшения и снижения их концентрации при проведении патогенетического лечения глюкокортикоидными препаратами и после тимэктомии с предшествующей терапией глюкокортикоидными препаратами. Полученные данные позволяют рекомендовать использование факта изменения концентрации антител, как еще одного критерия оценки эффективности проводимого лечения.
Проведенное исследование было разделено на 2 основных этапа. Первый этап - определение клинической эффективности разных методов патогенетического лечения - терапии глюкокортикоидными препаратами и тим(тимомтим)эктомии. Второй этап - сопоставление полученного эффекта с изменением концентрации сывороточных антител к АХР.
Определение клинической эффективности проведенного лечения.
История применения глюкокортикоидных препаратов при миастении берет свое начало с 1970-х годов, однако, несмотря на большой опыт применения и бесспорно высокую эффективность, механизм их действия при этом заболевании остается до конца не изученным. Согласно современным представлениям, эффект глюкокортикоидных препаратов на иммунную систему реализуется несколькими путями, включающими угнетение процесса миграции лейкоцитов, ингибирование ряда функций Т-клеток, уменьшение продукции и секреции цитокинов рядом клеток и угнетение созревания дендритических клеток (Diaz-Manera J. et al., 2009). Первоначально проводились попытки назначения глюкокортикоидных препаратов в больших дозах на относительно короткое время с быстрой отменой. Это приводило в большинстве случаев к выраженному улучшению состояния, за которым часто следовала экзацербация заболевания (Mann J. D. et al., 1976). В дальнейшем было доказано, что продолжительный прием поддерживающих доз глюкокортикоидных препаратов позволяет добиваться длительной и устойчивой ремиссии в течение продолжительного времени (, , 1996). Сегодня глюкокортикоиды используются как препараты первого ряда в терапии миастении (Jee Y. K. et al., 2011; Gilhus N. E. et al., 2011).
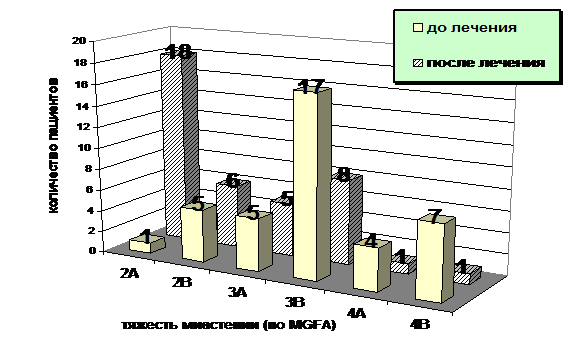
Рисунок 2. Распределение 39 больных в зависимости от тяжести состояния до и на фоне лечения глюкокортикоидными препаратами. Ось абсцисс – степень выраженности клинических проявлений миастении по шкале (согласно MGFA), ось ординат – число пациентов.
Согласно данным, полученным в ходе нашего исследования, клиническое улучшение на фоне приема глюкокортикоидных препаратов при оценке через 2-4 месяца после начала лечения наблюдалось у 28 из 39 пациентов (72%). При этом, выраженный эффект, подразумевавший изменение степени тяжести с 4 (А/В) до 2 (А/В) по MGFA, имел место только у 4 пациентов. У остальных 24 пациентов имелась умеренно выраженная положительная динамика в виде снижения степени тяжести заболевания на 1 градацию по MGFA. Полученные данные представлены на рис. 2.
Аналогичные результаты были получены и другими авторами (Evoli A. et al., 1992; Gajdos P. et al., 1999; Schneider-Gold C. et al., 2005), по результатам работ которых, эффект от применения глюкокортикоидных препаратов наблюдался у 70-80% больных с миастенией.
Тимус при миастении играет важную роль в индуцировании первичной иммуногенности, в основе которой лежит нарушение механизмов формирования толерантности Т-лимфоцитов к собственным антигенным белкам тимуса. В их число входят белки субъединиц АХР, а также титин и рианодиновые рецепторы ( и др., 2003; Kaminski H. J. et al., 1993; Mygland A. et al., 1995; Romi F. et al., 2000). Таким образом, вилочковая железа по современным представлениям является источником провоцирования и поддержания патологического аутоиммунного ответа при миастении (Cavalcante P. et al., 2011).
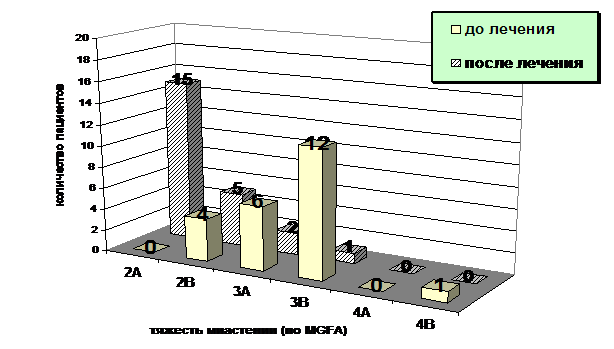
Рисунок 3. Распределение 23 больных в зависимости от тяжести состояния до и после проведения тим(тимомтим)эктомии. Обозначения: ось абсцисс – степень выраженности клинических проявлений миастении (согласно MGFA), ось ординат – количество пациентов.
По данным литературы клиническое улучшение при тимэктомии наблюдается в 60-80% случаев, чего не отмечается больше ни при одном другом аутоиммунном заболевании человека (Busch C. et al., 1996; Venuta F. et al., 1999; Popescu I. et al., 2002; Romi F. et al., 2006).
В настоящем исследовании положительный клинический эффект от тимэктомии при оценке через 9-12 месяцев после операции (рис. 3) наблюдался у 21 из 23 пациентов (91%), что в целом несколько больше, чем по данным ряда других авторов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


