Некоторые авторы указывают на то, что при комбинации тимэктомии и гормональной терапии антитела снижаются более существенно, чем при проведении операции без предварительной медикаментозной иммуносупрессии. Более того, есть данные, что при лечении только глюкокортикоидными препаратами антитела к АХР снижаются больше, чем при проведении только тимэктомии без применения других методов иммуносупрессивной терапии (Seybold M. E., Lindstrom J. M., 1981; Oosterhuis H. J. et al., 1983).
В наше исследование было включено 7 пациентов, у которых хирургическое лечение осуществлялось без предварительной глюкокортикоидной терапии. При этом не выявлено достоверного различия эффекта вмешательства у лиц с изолированным хирургическим лечением и тимэктомией в рамках комбинированной предварительной терапии глюкокортикоидными препаратами (табл. 6, А и В).
Таблица 6
А. Изменение клинико-иммунологических параметров у пациентов после тимэктомии.
Тяжесть заболевания | Число пациентов (n=7) | QMGS до и после лечения (среднее значение в баллах) | Содержание антител к АХР до и после лечения (среднее значение и d в нмоль/л) |
3В-2В | 1 | 21 – 9 | 21,8 - 21,2 |
3В-2А | 1 | 16 – 4 | 21,9 – 10,3 |
3А-2А | 2 | 18 - 4,5 | 18,8 (4,5) – 7,7 (5,1) |
2В-2А | 2 | 8,5 -5 | 17,3 (3,1) – 13,0 (3,6) |
3А-3А | 1 | 19-21 | 27,0 – 19,4 |
В. Изменение клинико-иммунологических параметров у пациентов после комбинированного лечения (глюкокортикоиды+тимэктомия).
Тяжесть заболевания | Число пациентов (n=16) | QMGS до и после лечения (среднее значение в баллах) | Содержание антител к АХР до и после лечения (среднее значение и d в нмоль/л) |
4В-3В | 1 | 28 – 20 | 7,2 – 5,0 |
3В-2В | 4 | 19 – 7,7 | 12,9(7,3) – 9,3(5,7) |
3В-2А | 6 | 17,5 – 8 | 13,3(8,0) – 10,3(8,6) |
3А-2А | 2 | 22 – 5,5 | 22,4(10,3) – 14,8(5,1) |
2В-2А | 2 | 11 – 6,5 | 16,4(6,9) – 10,1(5,5) |
3А-3А | 1 | 22 - 20 | 21,2 – 23,9 |
В целом, полученные в настоящем исследовании результаты показали (рис. 4), что у большинства больных при применении патогенетических методов лечения миастении, таких как терапия глюкокортикоидными препаратами или проведения тим(тимомтим)эктомии, положительный клинический эффект сопровождается уменьшением уровня антител к АХР (p<0,05).
Также как и другие исследователи, мы выявили группу больных, у которых улучшение состояния не ассоциировалось с уменьшением концентрации антител. Отсутствие клинического улучшения могло сопровождаться уменьшением уровня антител к АХР, но это уменьшение носило, как правило, невыраженный характер.
Проведенное нами исследование выявило несколько большую эффективность хирургического лечения по сравнению с глюкокортикоидной терапией. Аналогичные данные приводят Kuкs J. B. et al. (1991) на основании наблюдения 25 больных на сроках от 1 года до 3.5 лет. Необходимо отметить, что другие исследователи отмечали большую эффективность терапии глюкокортикоидными препаратами или их комбинации с азатиоприном (Schumm F. et al., 1984).
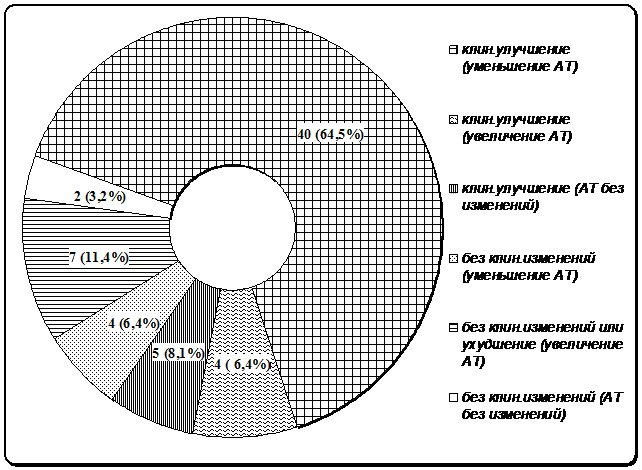
Рисунок 4. Варианты изменения клинического статуса и динамика уровня антител к АХР у 62 пациентов с миастенией на фоне патогенетического лечения. Для каждой группы указано число и (%) больных.
Известно, что при миастении использование других методов патогенетического лечения также приводит к уменьшению концентрации аутоантител к АХР. Так, при проведении плазмафереза и иммуносорбции на фоне клинического улучшения наблюдается снижение уровня антител в среднем на 21.0 ± 5.0% (Dau P. C. et al., 1993). Отмечен драматический клинический эффект ритуксимаба, сопровождавшийся достоверным снижением концентрации антител к АХР (Nowak R. J. et al., 2011). Однако введение человеческого иммуноглобулина несмотря на клинический эффект не сопровождается достоверным уменьшением концентрации антител к АХР в интервале от 2 до 4 недель после окончания курса лечения (, 2011).
Совокупность собственных данных и результатов, приведенных в литературе, позволяет считать, что границей ожидаемого улучшения является снижение уровня антител более чем на 20% (Schumm F. et al., 1984). Уменьшение концентрации антител на 50% и более, как правило, ассоциируется с достоверным клиническим улучшением.
Таким образом, исследование концентрации антител к АХР до и после использования разных видов патогенетического лечения является важной составляющей объективной оценки эффективности проводимых мероприятий. Выявление группы больных, у которых клиническое улучшение ассоциируется с незначительным менее 20% снижением уровня антител, с отсутствием изменения или даже увеличением уровня антител к АХР может указывать на неблагополучный прогноз течения болезни с возможным возникновением рецидива или экзацербации миастении.
ВЫВОДЫ
1. Патофизиологической основой нарушения нервно-мышечной передачи при миастении является появление антител к АХР, что позволяет использовать мониторинг их концентрации в оценке эффективности патогенетического лечения и прогноза неблагоприятного течения болезни. Обязательным является определение уровня антител к АХР на сроках 2-4 месяца после начала глюкокортикоидной терапии и 9-12 месяцев после проведения тим(тимомтим)эктомии.
2. Подавление патофизиологических механизмов аутоиммунной агрессии при адекватной патогенетической терапии приводит к ассоциации выраженного положительного клинического эффекта с уменьшением концентрации антител к АХР на 40% и более.
3. Отсутствие снижения концентрации антител к АХР при патогенетическом лечении, несмотря на клиническое улучшение, является признаком сохранения активности патофизиологического процесса и обуславливает высокую вероятность экзацербации болезни. Стабильность или повышение содержания антител к АХР на фоне лечения является неблагоприятным прогностическим фактором.
4. Клиническое улучшение, объективизируемое изменениями класса по шкале MGFA и количественной оценкой выраженности двигательных расстройств по шкале QMGS, наблюдается у 72% пациентов с миастенией на фоне лечения препаратами глюкокортикоидного ряда и у 90% пациентов при комбинированном лечении с предварительным назначением глюкокортикоидных препаратов и хирургическим удалением тимуса или тимомы.
5. В 80% случаев положительный клинический эффект глюкокортикоидной терапии и комбинированного лечения с использованием глюкокортикоидных препаратов и хирургического удаления тимуса или тимомы сопровождается уменьшением концентрации антител к АХР в среднем на 45%.
6. Изменение концентрации антител к АХР при патогенетическом лечении не зависит от возраста и пола больных, наличия или отсутствия тимомы, а также проведения фоновой терапии глюкокортикоидными препаратами в случае хирургического лечения.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. При оценке эффективности терапии глюкокортикоидными препаратами и тимом(тимомтим)эктомии у больных с миастенией, а также при прогнозировании дальнейшего течения болезни, целесообразно проведение мониторинга изменения концентрации антител к ацетилхолиновым рецепторам.
2. Оценку клинического эффекта и изменения уровня антител к ацетилхолиновым рецепторам на фоне лечения необходимо проводить через 2-4 месяца после начала терапии глюкокортикоидными препаратами и через 9-12 месяцев после проведения тим(тимомтим)эктомии.
3. Шкала количественной оценки тяжести клинических проявлений миастении (QMGS) является важным инструментом определения тяжести заболевания у пациентов с миастенией. Использование этой шкалы в совокупности с общепринятой шкалой оценки мышечной силы MRC позволяет повысить объективность оценки и учесть патогномоничный для миастении симптом патологической мышечной утомляемости.
Список работ, опубликованных по теме диссертации
1. , , , Карганов миастения: клинические, иммунологические и электрофизиологические характеристики // Клиническая неврология. – 2008. – №1. – С.3-10.
2. , , , Карганов и миастения у больного с тимомой // Журнал неврологии и психиатрии имени . – 2010. – Т.110. – №5. – С.101-103.
3. , , , , Алчинова к ацетилхолиновому рецептору в оценке эффективности патогенетической терапии у больных с миастенией // Журнал неврологии и психиатрии имени . – 2010. – Т.110. – №11. – С.37-40.
4. , , Дедаев С. И., Магомедов к ацетилхолиновому рецептору в оценке эффективности тимэктомии у больных с генерализованной миастенией // Вестник Национального медико-хирургического центра им. . – 2011. – Т.6. – №4. – С.15-19.
5. Sidnev D. V., Sanadze A. G., Dedaev S. I., Karganov M. Yu., Alchinova I. B. Antibodies to acetilcholine receptors in assessment of the efficacy of pathogenetic treatment patient with myasthenia // Neuroscience and Behavioural Phisiology. – 2011. – V.41. – №9. – Р.889-893.
6. , , Сиднев шкалы QMGS для количественной оценки тяжести двигательных расстройств у больных миастенией // Журнал неврологии и психиатрии имени . – 2012. – Т.112. – №7. – С.32-35.
7. , , , Кондратьев и антитела к ацетилхолиновому рецептору у больных миастенией: особенности раннего послеоперационного периода // Журнал неврологии и психиатрии имени . – 2012. – Т.112. – №9. – С.65-69.
Dedaev Sergey Igorevich
Pathogenetic role of antibodies against acetylcholine receptors in assessment of myasthenia gravis treatment efficacy.
Myasthenia gravis (MG) is an autoimmune neuromuscular disease with a confirmed pathophysiological role of circulating antibodies against acetylcholine receptors (anti-AChR) at the postsynaptic neuromuscular junction. The test of anti-AchR has a reasonable sensitivity of 80-95%, and is usually positive in up to 85% of cases. The absence of correlation between anti-AchR level and patient’s gender, age, severity and clinical course limits the usefulness of immunological test only to diagnostics purposes in MG.
The aim of the study was to analyze the pathophysiological mechanisms and relationship between clinical status and immunological changes in 62 patients with confirmed generalized MG taking pathogenic treatment. In 39 patients (group 1) the treatment was limited with high dosage of glucocorticoids (GL), and in 23 patients (group 2) the surgical removal of the thymus was done. In every patient the severity of symptoms with scales MRC and QMGS and anti-AChR concentration were tested before and 2-4 month after beginning of GL and 9-12 months after thymectomy.
It was shown that in group 1 the clinical improvement was associated with decreased anti-AChR concentration in 80% of cases. The positive clinical dynamics but without significant changes of anti-AChR concentration was associated with high risk of future exacerbation. The evaluation of anti-AChR concentration with obliged simultaneous complex MRC and QMGS clinical assessment may be used for predicting of course of the disease in MG patients. The absence lowering of anti-AChR concentration in comparison with the initial pretreatment level (before GL or thymectomy) is considered as a poor prognostic factor in disease course and reflect the resistance towards both types of treatment and possible activity of main pathophysiological mechanism of anti-AChR production and anti-AChR dependant damage of postsynaptic structures of neuron-muscular junction.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


