9.1. Основная литература
п/№ | Наименование | Автор (ы) | Год, место издания | Кол-во экземпляров | |
в библиотеке | на кафедре | ||||
1 | 2 | 3 | 4 | 7 | 8 |
1. | «Биохимия» | под редакцией чл.-корр. РАН, проф. | М., 2008 | 99 | 3 |
2. | «Биохимия с упражнениями и задачами» | под редакцией чл.-корр. РАН, проф. | М., 2008 | - | 3 |
3. | Биологическая химия. Учебник для студентов медицинских институтов. 3-е изд. | , | М., 2004 | 5 | - |
9.2. Дополнительная литература
п/№ | Наименование | Автор (ы) | Год, место издания | Кол-во экземпляров | |
в библиотеке | на кафедре | ||||
1 | 2 | 3 | 4 | 7 | 8 |
1. | Биохимия: химические реакции в живой клетке (в трех томах). | М., 1980 | - | 3 | |
2. | Основы биохимии (в трех томах). |
| М., 1981 | - | 3 |
3. | Биохимия (в трех томах). | М., 1985 | 1 | 3 | |
4. | Основы биохимии (в трех томах). | М., 1985 | 1 | 3 | |
5. | Биохимия человека (в двух томах). | , , | М., 2004. | 2 | 2 |
6. | Возрастная биохимия. Учебное пособие для мед. ВУЗов. | под редакцией проф. | СПб, 2007 | - | 1 |
9.3. Программное обеспечение:
Интернет-ресурсы.
1. MedLine.
2. PubMed.
9.4. Базы данных, информационно-справочные и поисковые системы:
Электронная база данных «Консультант студента». Элнетронная библиотека медицинского вуза. Компьютеры кафедры имеют логин и пароль для входа.
10. Материально-техническое обеспечение дисциплины
Аудитории, оснащённые лабораторными столами, вытяжными шкафами. Водяные
бани, фотоэлектроколориметры, лабораторные центрифуги, термостаты, спектрофотометры, иономеры, лабораторная посуда, штативы, наборы соответствующих реактивов, лабораторные животные (белые крысы), скальпели, лезвия, пинцеты, чашки Петри, колбы, пробирки, склянки для реактивов; фильтровальная бумага;
ноутбук с мультимедийной приставкой (для чтения лекций), компьютеры, принтеры, сканнеры.
11. Методические рекомендации по организации изучения дисциплины
1. Руководство к практическим занятиям по биохимии / под ред. .-Н. Новгород : НижГМА, 2010.- 107 с.
2. Сборник задач по биохимии / под ред. .-Н. Новгород : НижГМА, 2009.- 28 с.
3. Сборник тестов и упражнений по биохимии / под ред. .-Н. Новгород НижГМА, 2009.- 124 с.
4. Методические указания для проведения практических занятий по биохимии (Паспорта готовности практических занятий. Руководства для преподавателей).
12.1. Использование современных образовательных технологий
- № | - Наименование раздела (перечислить те разделы, в которых используются активные и/или интерактивные образовательные технологии) | - Формы занятий с использованием активных и интерактивных образовательных технологий | - Трудоемкость (час.) |
1. 1. | 2. 1-4, 6-13, 15 | 3. Лекции-визуализации | 4. 40 |
5. 2. | 6. 1-15 | 7. Информационные проекты | 8. 20 |
- 3. | - 1-11 | - Кэйс-методики | - 32 |
12.2. Оценочные средства для текущего контроля успеваемости
ТЕКУЩИЙ ТЕСТОВЫЙ КОНТРОЛЬ ПО ТЕМЕ ДМ №1 «ФЕРМЕНТЫ»
Инструкция. Без дополнительных указаний в задании теста выберите один наиболее правильный ответ. Вариант
1. Какова химическая природа ферментов?
1 - сложные белки 2 - производные витаминов
3 - производные аминокислот 4 - простые и сложные белки
2. Дайте определение понятию апофермент:
1 - комплекс белка и кофермента 2 - белковая часть сложного фермента
3 - не белковая часть сложного фермента 4 - простой фермент
3. Какова физиологическая роль кофактора в катализе? (2 ответа)
1 – определяет субстратную и каталитическую специфичность
2 – стабилизирует структуру фермента
3 – принимает непосредственное участие в катализе
4 - принимает опосредованное участие в катализе
4. Выберите коферменты участвующие в окислительно-восстановительных реакциях:
1 – АТФ 2 – НАД; НАДФ; ФАД; ФМН; Q; ГЕМ; Г-SН. 3 – НSКоА 4 - УДФГК
5 – перидоксальфосфат 6 – S-аденозалметионин (SАМ) 7 – ТПФ 8 – ФАФС
5. Выберите физико-химические свойства присущие активному центру фермента: (3 ответа)
1 – дестабилизирует межатомные связи в молекуле субстрата
2 – использует разнообразные физико-химические механизмы катализа
3 – максимально сближает и ориентирует соответствующие реагенты по отношению друг-другу
4 – снижает свободную энергию реагирующих веществ
5 – катализирует реакции энергетически не возможные в отсутствие ферментов
6. Какой механизм ферментативного катализа реализуется при переносе протона от
функциональной группы активного центра на субстрат?
1 – электрофильный 2 – нуклеофильный 3 – радикальный 4 – кислотно-основной
7. Выберите название участка на ферменте, к которому присоединяется регуляторный модулятор
активности фермента:
1 - активный центр 2 - аллостерический центр 3 - каталитический центр
4 - субстратный центр 5 - кофактор 6 - апофермент
8. Результатом регуляции активности ферментов по механизму ограниченного протеолиза
является:
1 - отщепление короткого пептида от профермента
2 - присоединение пептида к проферменту
3 - отщепление протомера от профермента
4 - отщепление кофермента от фермента
5 - нарушение комплементарности между активным центром и субстратом
9. Каким биохимическим методом можно обнаружить наличие фермента в биологическом материале:
1 - центрифугированием 2 – хроматографированием 3 - электрофорезом
4 - цветной реакцией на пептидную связь 5 - цветной реакцией на продукт реакции
10. Из приведённого перечня выберите кофермент, в состав которого входит витамин В2 :
1 - НАД 2 - НАДФ 3 - ФАД 4 - ТПФ 5 - НS-КоА 6 - перидоксальфосфат
11. Как изменится скорость химической реакции при ферментативном катализе если Км
с 10 мммоль/л уменьшится до 0,1 ммоль/л?
1 - уменьшится 2 - увеличится 3 - не изменится
12. К какому классу относятся ферменты, используемые для ингаляционной энзимотерапии?
1 - оксидоредуктазы 2 - трансферазы 3 - гидролазы
4 - лиазы 5 - изомеразы 6 - лигазы
13. Существование множественных форм фермента (изоферментов) возможно только для следующих
ферментов:
1 - состоящих из 2-х и более различных субъединиц
2 - состоящих из нескольких идентичных субъединиц
3 - всех сложных ферментов
4 - всех простых и сложных ферментов
14. Выберите один из ниже приведённых признаков положенных в основу современной
международной классификации ферментов:
1 - строение субстрата 3 - тип химической связи
2 - строение продукта 4 - тип химической реакции
15.
1 - оксидоредуктазы 2 - трансферазы 3 - гидролазы
4 - лиазы 5 - изомеразы 6 - лигазы
Из приведенной выше классификации выберите класс фермента для каждой из ниже приведённой реакции (А-Д).
А - гистидин → гистамин + CO2
Б - лактат + НАД+ ↔ ПВК + НАДН2
В - ала + 2-оксоглутарат ↔ ПВК + Глу
Г - лактоза + Н2О → Д-глюкоза + Д-галактоза
Д - глюкозо-6-фосфат ↔ фруктозо-6-фосфат
16. Какому из приведенного набора субъединиц соответствует изофермент ЛДГ2 ?
1 - НННН 2 - НННМ 3 - ННММ 4 - НМММ 5 - ММММ
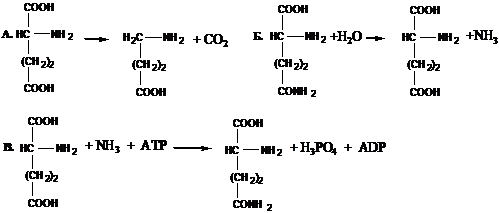
17.
1 - оксидоредуктазы 2 - трансферазы 3 - гидролазы
4 - лиазы 5 - изомеразы 6 - лигазы
Из приведенной выше классификации выберите класс фермента для каждой из ниже приведённой
реакции (А-В).
ТЕКУЩИЙ ЗАЧЕТНЫЙ КОНТРОЛЬ ПО ТЕМЕ БЕЛКИ, ФЕРМЕНТЫ
1. Принципы классификации аминокислот. Привести примеры. Основные свойства аминокислот. Их роль в формировании структуры белка и образовании внутримолекулярных связей. Аминокислоты как лекарственные препараты.
2. Белок-лигандные взаимодействия. Избирательность взаимодействия с лигандами ("узнавание лиганда"). Типы природных лигандов и особенности их взаимодействия с белками (кофакторы, простетические группы, субстраты, транспортируемые вещества, аллостерические эффекторы).
3. Белок-белковые взаимодействия, связи их образующие. Привести примеры. Роль в образовании межмолекулярных комплексов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |




