Повторяют высушивание при тех же условиях в течение 30 мин. Затем бюкс охлаждают в эксикаторе и снова взвешивают. Эту операцию повторяют до тех пор, пока масса бюкса с хлоридом бария не станет постоянной (разница не более 0,0002 г).
Пример записи результатов опыта
Дата.
Название работы: «Определение содержания кристаллизационной воды в кристаллогидрате хлорида бария».
Масса бюкса после первого взвешивания 20,2330 г
Масса бюкса после второго взвешивания 20,2328 г
Окончательная масса бюкса 20,2328 г
Масса бюкса с навеской 23,6508 г
Масса хлорида бария 3,1480 г
Масса бюкса с навеской после первого высушивания 23,1468 г
Масса бюкса с навеской после второго высушивания 23,1463 г
Масса бюкса с навеской после третьего высушивания 23,1462 г
Окончательная масса бюкса с хлоридом бария 23,1462 г
3.2.Расчет
Масса кристаллизационной воды в навеске хлорида бария: 23,6508- 23,1462=0,5046 г. Для вычисления содержания кристаллизационной воды (х) в процентах составим пропорцию:
В 3,4180г навески содержится 0,5046г воды
В 100г навески содержится x г воды.
Отсюда X=
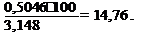
Полученный результат сравнивают с теоретическим содержанием кристаллизационной воды, рассчитанной по химической формуле BaCl2*Н2 0.
Молекулярная масса BaCl2* H2 0 244,2
Молекулярная масса Н2 0 18,015
Для вычисления составляют пропорцию:
В 244,28 г х. ч. ВаСl2*2H2 O содержится 36,03 г Н2 О
В 100 г х. ч. ВаСl2*2Н2 О содержится х г Н2 О
Отсюда
X=![]()
Если результаты анализа сравнить с теоретически вычисленным количеством воды для BaCl2*2Н2 О, то можно посчитать абсолютную ошибку определения:
D = 14,76 - 14,75 = 0,01%.
Относительную ошибку (D0) в процентах вычисляют из следующей пропорции:
14,75 - 0,01
100 – D0
Отсюда
D0=![]()
1.8 Учебно-методическое обеспечение дисциплины.
1.8.1 Рекомендуемая литература учебные издания
ОСНОВНАЯ ЛИТЕРАТУРА
Лурье по аналитической химии. – М.: Химия, 1971. , Мень химия. Качественный анализ катионов и анионов. Мурманск: МГПИ, 2001. , Мень в растворах электролитов. Мурманск: МГПИ, 2000. Пономарев химия. Книги 1 и 2. – М.: Химия, 1982. Харитонов химия. Книги 1 и 2. – М.: Химия, 2001.ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
Алексеев анализ. – М.: Химия, 1972. Алексеев качественного химического полумикроанализа. – М.: Химия, 1979. Алексеева анионов. Методические указания. - СПб.: СПХФА, 1995. Задачник по аналитической химии. – М.: Химия, 1993. Крешков аналитической химии. Книги 1,2,3. – М.: Химия, 1976. , , и др. Качественный химический анализ катионов: Методические указания. - СПб.: СПХФА, 1998.1.9 Материально-техническое обеспечение дисциплины
1.9.1 Перечень используемых технических средств:
Лабораторная посуда: пробирки, мерные цилиндры, бюретки, колбы конические, круглодонные, химические стаканы, воронки, водяная баня, плитка, пипетки, тигли, предметные стекла.
Лабораторное оборудование: спиртовки, лабораторные штативы, штативы для пробирок, планшетки для капельных реакций, подносы, зажимы-пробиркодержатели, шпатели - ложечки, подставки для реактивов, приборы для получения газов, прибор для измерения скорости химических реакций.
Наборы химических реактивов реактивы для количественного и качественного анализа (определение анионов и катионов)
1.9.2. Перечень используемых пособий:
Периодическая система химических элементов .
Ряд активности металлов.
Таблица «Растворимость солей, кислот и оснований в воде»
Таблица «Плотность растворов щелочей и кислот»
Таблица «Относительная электроотрицательность атомов элементов»
Плакаты.
Видеофильмы.
1.10 Примерные зачетные тестовые задания.
I. Равновесие в растворах электролитов, концентрации, гидролиз.
Вариант 1.
Определить константу диссоциации кислоты, если в 0,1 М растворе степень ее диссоциации 25%.а) 8,33 ×10-3; б) 5,2 ×10-3; в) 3,33 × 10-1; г) 5,2 × 10-2.
Какова молярность 20%-ой азотной кислоты? (ρ = 1,115 г/мл).а) 1,72 моль/л; б) 3,54 моль/л; в) 2,48 моль/л; г) 2,04 моль/л.
В 0,5 л раствора содержится 4,1 г СН3СОONa. Вычислить рН и степень гидролиза соли.а) 9,98; h = 6,78 × 10-3%; б) 7,6; h = 1,8%; в) 10,95; h = 7,6 × 10-2%; г) 8,88; h = 7,6 × 10-3%.
Вычислить рН раствора, полученного смешением 50 мл 0,1 М раствора КН2РО4 и 25 мл 0,2М К2НРО4.а) 6,98; б) 7,50; в) 7,20; г) 6,50.
Вариант 2.
Вычислить рН раствора, полученного смешением 70 мл 0,2 М КН2Cit и 30 мл 0,1М К2НCit (Cit3- - анион лимонной кислоты).а) 4,00; б) 5,77; в) 4,09; г) 3,65.
Определить Ка, если в 0,01М растворе кислота диссоциирована на 30%.а) 2,85 × 10-3; б) 1,32 × 10-2; в) 2,85 × 10-2; г) 1,28 × 10-3.
а) 0,65М; б) 1,76М; в) 2,56М; г) 1,63М.
К 30 мл воды прибавили 5 мл 3М раствора КNO2. Вычислить рН раствора.а) 8,46; б) 9,53; в) 10,80; г) 8,63.
Вариант 3.
Вычислить рН и степень гидролиза соли в 0,05М Na2СО3. Чему будет равен рН, если раствор разбавить водой в 5 раз?а) 10,67; 5,5%; 11,51; б) 11,51; 6,42%; 11,16;
в) 11,16; 3,34%; 10.67; г) 11,16; 4,42%; 9,78.
Вычислить рН раствора, полученного смешением 210 мл 0,1М Na2СО3 и 90 мл 0,М НСl.а) 10,45; б) 9,88; в) 11,9; г) 9,05.
Определить концентрацию раствора уксусной кислоты, если α = 2%.Ка=1,75 × 10-5.
а) 0,032; б) 0,022; в) 0,044; г) 0,014.
В 0,5 л соляной кислоты содержится 0,1 моль НСl. Определить массовую долю кислоты в растворе.а) 0,245%; б) 0,322%; в) 0,567%; г) 0,728%.
Вариант 4.
К 250 мл 10%-ой НNO3 (ρ = 1,054 г/мл) добавили 200 мл 50%-ой азотной кислоты (ρ = 1,310 г/мл). Какова массовая доля кислоты в растворе?а) 28,32%; б) 22,45%; в) 42,56%; г) 29,94%.
К 100 мл 0,2М НСООН прибавили 100 мл 0,2М КОН. Вычислить рН раствора.а) 7,38; б) 8,98; в) 8,37; г) 8,65.
Вычислить рН раствора, полученного смешением 30 мл 0,1М КН2РО4 и 25 мл 0,2М КОН.а) 11,3; б) 12,2; в) 9,88; г) 8,76.
Определить степень диссоциации кислоты в растворе с концентрацией 10-3 моль/л. Ка = 1,75 × 10-4.а) 0,418; б) 13,2%; в) 1,32; г) 4,18%.
Вариант 5.
Определить рН в 0,01 М растворе бензойной кислоты, если Ка = 6,1 × 10-5.а) рН - 5,3; б) рН - 6,7; в) рН - 4,6; г) рН - 3,1.
Сколько мл 96%-ой H2SO4 (ρ = 1,835 г/мл) нужно взять, чтобы приготовить 1 л 0,5М раствора кислоты?а) 27,81 мл; б) 22,45 мл; в) 14,87 мл; г) 16,34 мл.
В 200 мл раствора содержится 0,65 г KCN. Определить рН и степень гидролиза соли.а) 8,88; h = 7,6 × 10-3%; б) 10,95; h = 1,6%;
в) 8,46; h = 6,8%; г) 9,8; h = 2,7%.
Вычислить рН раствора, полученного при смешении 30 мл 0,1М Na2СО3 и 15 мл 0,1М NaHCO3.а) 9,88; б) 8,88; в) 10,63; г) 11,90.
Вариант 6.
Вычислить рН раствора, полученного смешением 30 мл 0,2М KH2PO4 и 10 мл 0,1М HCl.а) 2,82; б) 3,24; в) 5,67; г) 7,20.
Определить рН в 0,1М растворе валерьяновой кислоты, если рК = 4,842.а) 3,80; б) 4,6; в) 3,92; г) 2,92.
Сколько мл 30%-ой соляной кислоты (ρ = 1,089 г/мл) надо взять, чтобы приготовить 0,5 л кислоты с плотностью 1,098 г/мл?а) 234 мл; б) 332 мл; в) 318 мл; г) 255 мл.
В 500 мл раствора содержится 2,52 г Na2СО3. Определить рН раствора.а) 10,87; б) 11,50; в) 10,66; г) 11,23.
Вариант 7.
1. Вычислить рН и степень гидролиза соли в 0,05Na2С2О4. Чему будет равен рН, если раствор разбавить в 10 раз?
а) 10,96; 4,5%; 8,97; б) 8,48; 6,1 × 10-3%; 7,98;
в) 8,66; 7,8 × 10-4%; 9,77; г) 7,67; 8 × 10-2; 11,2.
2. Вычислить рН раствора, полученного смешением 50 мл 0,15М К2НРО4 и 45 мл 0,3М НСl.
а) 2,64; б) 3,97; в) 2,22; г) 4,66.
3. Определить степень диссоциации в 0,1 М растворе уксусной кислоты, если к ней добавили равный объём 0,1М соляной кислоты.
а) 3,5 × 10-2; б) 0,875 × 10-2; в) 2,5 × 10-3; г) 1,75 × 10-2.
4. К 100 мл 0,5М раствора азотной кислоты добавили 100 мл 10%-го раствора этой же кислоты (ρ = 1,054 г/мл). Какова молярность полученного раствора?
а) 1,08М; б) 1,65М; в) 0,55М; г) 0,6М.
Вариант 8.
Определить массовую долю Н3РО4, если к 1 л 0,5М раствора добавили 50 мл 25%-го раствора кислоты (ρ = 1,145 г/мл).а) 6,66%; б) 5,47%; в) 5,86%; г) 7,45%.
К 250 мл 0,4М НСl прибавили 250 мл 0,4М NаОН. Вычислить рН и степень гидролиза соли.а) 10,80; 2%; б) 11,05; 0,9%; в) 8,46; 1,8%; г) 8,95; 2,9%.
Вычислить рН раствора, полученного смешением 40 мл 0,2М КН2РО4 и 10 мл 0,2М КОН.а) 6,72; б) 7,65; в) 9,87; г) 5,64.
Определить концентрацию [Н+], [Н2АsО4-], [НАsО42-] в 0,1М растворе мышьяковой кислоты. К1 = 5,89 × 10-3; К2 = 1,05 × 10-7; К3 = 3,89 × 10-13.а) [Н+] = [Н2АsО4-] = 1,17 × 10-3; [НАsO42-] = 6 × 10-7;
б) [Н+] = [Н2АsО4-] = 1,27 × 10-3; [НАsO42-] = 5 × 10-6;
в) [Н+]= [Н2АsО4-] = 0,17 × 10-2;
г) [Н+]= [Н2АsО4-] = 2,42 × 10-2; [НАsO42-] = 1,05 × 10-7.
Вариант 9.
1.Определить [Н+], [НS-], [S2-] в 0,1М растворе Н2S. рК1 = 6,96; рК2=14.а) [Н+] = [НS-] = 2 × 10-5; [S2-] = 10-7;
б) [Н+] = [НS-] = 1,05 × 10-4; [S2-] = 10-14;
в) [Н+] = [НS-] = 3 × 10-5; [S2-] = 10-5;
г) [Н+] = [НS-] = 4 × 10-7; [S2-] = 10-21.
Смешали 20 мл 10%-ой серной кислоты (ρ =1,066 г/мл) с 50 мл 20%-ой Н2SО4 (ρ = 1,139 г/мл). Какова массовая доля кислоты в растворе?а) 15,30%; б) 13,54%; в) 17,28%; г) 14,66%.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




