Влияние циклофосфана и лактулозы на поступление аммиака и веществ средней молярной массы из кишечника в кровь у крыс
В. Л. Рейнюк, Т. В. Шефер, , Ю. Ю. Ивницкий
(научный руководитель — Ю. Ю. Ивницкий)
ФГУН «Институт токсикологии» ФМБА России, Санкт-Петербург ____________________________________________________________________________
Изучали влияние лактулозы (Л) на поступление аммиака и веществ средней молярной массы (ВСММ) из кишечника в кровь, а также на тяжесть интоксикации циклофосфаном (Ц) у крыс. Л вводили в/ж в дозе 30 ммоль/кг за 3 ч до Ц (в/б 200, 600 или 1000 мг/кг). В течение 6 ч после введения Л, рН и зависимая от уреазы компонента аммиакпродуцирующей активности химуса слепой кишки снижались (на 1,0 и 35%), а содержание аммиака в химусе возрастало на 38%. Введение Ц повышало содержание аммиака и, в меньшей степени, глутамина в портальной крови и крови, полученной при декапитации (в 3,6 и 9,0 раз, соответственно), интенсифицировало поступление в портальную кровь метиленового синего, введённого в/ж, и эндогенных ВСММ. Л значимо не влияла на эти изменения, а также на неврологический статус, летальность и среднюю продолжительность жизни крыс. Таким образом, введение Л не препятствовало вызванной Ц интенсификации утечки аммиака и ВСММ из желудочно-кишечного тракта в кровь и не уменьшало тяжести интоксикации.
Ключевые слова: лактулоза; циклофосфан; аммиак; метиленовый синий; вещества средней молярной массы
Миелоабляционные режимы применения циклофосфана (Ц) при подготовке к трансплантации стволовых кроветворных клеток сопряжены с острыми нейротоксическими эффектами [7]. Ввиду энтеротоксичности Ц [6], в формирование таких эффектов могут быть вовлечены вещества, образующиеся в кишечном химусе — в том числе соединения малой (<300 г/моль) и средней (300—5000 г/моль) молярной массы. Ранее мы показали, что эта гипотеза справедлива в отношении одного из веществ малой молярной массы — аммиака [4, 5]. При печёночной энцефалопатии, для подавления токсигенной и аммиакпродуцирующей микрофлоры в просвете кишечника, назначают лактулозу (Л), [2]. Однако вызываемая Л ацидификация химуса может ускорить образование цитотоксичного бис-хлорэтиламина за счёт гидролиза амидных связей Ц, а также нарушить обезвреживание аммиака в энтероцитах глутаминсинтетазой, для которой оптимум рН составляет 7—8 [8]. В связи с этим, в настоящей работе оценивали влияние Л на поступление аммиака и (или) веществ средней молярной массы (ВСММ) из химуса в кровь при острой интоксикации Ц, а также на тяжесть этой интоксикации.
Методика исследования
В работе использовали самцов беспородных крыс-альбиносов массой 140—160 г, приобретённых в питомнике «Рапполово» АМН РФ. В течение суток перед экспериментом животных не кормили при неограниченном доступе к воде. Лапаротомию проводили под эфирным наркозом. Лактулозу (Л) вводили в/ж в виде 1,5 М раствора, приготовленного ex tempore из сиропа «Duphalac» (Solvay Biologicals, Нидерланды), в объёме 20 мл/кг. Раствор Ц («Компания Деко», Россия), вводили в/б в дозе 200, 600 или 1000 мг/кг, в объёме 10 мл/кг. Метиленовый синий (МС, чда, ЛенРеактив), который вводили в/ж (313 мкмоль/кг в объёме 10 мл/кг), рассматривали как модель ВCММ. Контрольные животные вместо растворов Л или Ц получали воду.
В 1-й серии опытов, через 3 или 6 ч после введения Л, содержимое слепой кишки суспендировали в четырёхкратном объёме 0,9% раствора хлорида натрия. Ионометром ЭВ-74 в центрифугате измеряли рН. Для определения аммиака в центральный стаканчик сосудика Варбурга помещали 0,1 мл 0,25 М H2SO4, в основной отсек — 1 мл суспензии, которую, после герметизации, смешивали с 1 мл насыщенного раствора поташа. Для оценки аммиакпродуцирующей активности химуса, поташ приливали после 30 мин. инкубации проб при 37ºС, которую проводили в отсутствие мочевины либо после внесения 400 мкмоль её в пробы. Через 18 ч аммиак определяли титрометрически.
Во 2-й серии, через 0,5, 1,0, или 3,0 ч после введения Ц в дозе 1000 мг/кг (т. е., 3,5; 4,0 или 6,0 ч после Л), отбирали 1 мл крови из v.0portae (краниальнее v. pylorica), после чего животных декапитировали и собирали кровь из шеи. Пробы депротеинировали равным объёмом 10% раствора трихлоруксусной кислоты, центрифугировали при 6000 g течение 15 мин; в супернатанте определяли аммиак с реактивом Несслера и глутамин (по аммиаку после 10 мин гидролиза при 100оС в присутствии 0,3 М H2SO4).
В 3-й серии, после Ц (1000 мг/кг), вводили МС и через 0,5; 1,0; 2,0 или 3,0 ч (т. е., 3,5; 4,0; 5,0 или 6,0 ч после введения Л) отбирали кровь из v. portae. Пробы депротеинировали и центрифугировали; спектрофотометрически определяли содержание в них МС (при 670 нм) и эндогенных ВСММ (при 238, 254, 260, 280 и 310 нм, [1, 3]).
В 4-й серии опытов оценивали влияние Л на тяжесть интоксикации Ц. Ежечасно в течение 6 ч измеряли продолжительность удерживания крыс на сфере диаметром 9 см (показатель равновесия и координации движений) и виса на решётке спиной книзу (показатель мышечной силы и выносливости); регистрировали сроки гибели.
Значимость влияния Л и (или) Ц на метаболические и неврологические показатели оценивали с помощью одно - и двухфакторного дисперсионного анализа; апостериорный анализ проводили методом наименьших значимых различий Фишера. Межгрупповые различия средней продолжительности жизни (СПЖ) оценивали с помощью критерия Манна-Уитни.
Результаты исследования
Введение животным лактулозы, существенно не изменяя содержание химуса в слепой кишке, снижало его рН на 1,0, зависимую от уреазы аммиакпродуцирующую активность — на 35% и повышало содержание аммиака в химусе на 26—28% (таблица1).
К 3 ч после введения Ц уровень аммиака был повышен в портальной крови и в крови, полученной при декапитации, на 228 и 199 мкМ (в 3,6 и 9,0 раз, в сравнении с контролем), соответственно. Снижалось отношение глутамина крови к аммиаку (в 2,5 и 1,5 раза, соответственно). Профилактическое введение Л не оказывало значимого влияния на эти изменения (рисунок 1).
Через 1—3 ч после введения МС у животных, получивших Ц, содержание МС в портальной крови было в 2,2—2,3 раза выше, чем у интактных крыс. Применение Л существенно не влияло на эти изменения. Содержание в портальной крови эндогенных ВСММ после введения Ц повышалось на 20—30%. Наблюдалась тенденция к повышению концентрации ВСММ в портальной крови на фоне профилактического введения Л, однако во все сроки наблюдения, кроме одного, она не была статистически значима (рисунок 2).
Продолжительность удерживания крыс на сфере и виса на перевёрнутой решётке, у интактных крыс превышавшая 30 с, после введения Ц дозозависимо снижалась. На фоне введения Л наблюдалась незначительная тенденция к усугублению этих расстройств. Л существенно не влияла на сроки гибели животных и на летальность (таблица 2).
Таким образом, острая интоксикация Ц сопровождалась увеличением потоков аммиака и ВСММ из желудочно-кишечного тракта в портальную кровь. Интенсификация поступления аммиака в портальную систему вследствие нарушения его вовлечения в состав глутамина в существенной мере определяла формирование системной гипераммониемии. Введение Л подавляло образование аммиака в кишечном химусе, но, при этом, существенно не влияло на поступление в кровь аммиака и ВСММ, а также на летальность, сроки гибели животных или на вызывавшиеся Ц острые неврологические расстройства — гипокинезию, атаксию и мышечную слабость. Полученные данные не поддерживают допущение о возможности благоприятного влияния Л на выраженность токсемии, летальность и неврологический статус организма при миелоабляционных режимах применения Ц.
Таблица 1
Влияние внутрижелудочного введения лактулозы крысам на рН и показатели обмена аммиака в химусе слепой кишки (M ± m, n = 4)
Экспери-менталь-ная группа крыс | Срок, ч | Индекс массы химуса, г на 1 кг массы тела | Показатели состава химуса | |||
рН | Содержание аммиака, ммоль/кг | Аммиакпродуцирующая активность, ммоль/(кг•час) | ||||
В отсутствие мочевины | В присутствии мочевины | |||||
Контроль | — | 9,7 ± 0,7 | 7,0 ± 0,1 | 39 ± 2 | 10 ± 2 | 151 ± 5 |
Опыт | 3 | 9,9 ± 1,1 | 6,5 ± 0,3 | 49 ± 2* | 9 ± 1 | 98 ± 6** |
6 | 11,6 ± 1,2 | 6,0±0,2* | 54 ± 4* | 12 ± 1 | 96 ± 7** |
Значимое различие с контрольной группой: * р ≤ 0,05; ** р ≤ 0,001
Таблица 2
Влияние лактулозы на тяжесть интоксикации циклофосфаном у крыс
Вещество, введённое в/ж за 3 ч до ЦФ | Доза цикло-фосфана, мг/кг | Средние величины показателей (M ± m) | Пало/всего | ||
Продолжительность удерживания | Продолжительность виса | Продолжительность жизни, ч | |||
Вода | 200 | 10,8 ± 1,1 | >30 | 420 ± 40 | 8/12 |
Лактулоза | 10,6 ± 1,6 | >30 | 519 ± 65 | 10/12 | |
Вода | 600 | 9,3 ± 1,2 | 18,0 ± 1,8 | 19,3 ± 1,1 | 6/6 |
Лактулоза | 6,3 ± 1,9 | 16,2 ± 1,1 | 23,4 ± 0,7 | 6/6 | |
Вода | 1000 | 1,3 ± 0,2 | 4,8 ± 0,5 | 8,0 ± 0,8 | 6/6 |
Лактулоза | 0,7 ± 0,2 | 4,0 ± 0,5 | 6,1 ± 0,6 | 6/6 |
Литература
1. и соавт. Лабораторная диагностика синдрома эндогенной интоксикации. Методические рекомендации. — Пермь, 2005. - 35 с.
2. Лечение болезней внутренних органов / . — М.: Медицинская литература, 2001 Т. 1: Лечение болезней органов дыхания. Лечение болезней органов пищеварения - 560 с.
3. Малахова регистрации эндогенной интоксикации. Пособие для
врачей. Санкт-Петербург: СПбМАПО, 1995. — 33 с.
4. , , Ивницкий острой токсичности циклофосфана при увеличении пула аммиака в пищеварительном тракте крыс // Бюл. эксперим. биол. мед., 2010. — Т. 149, № 6. — С. 657-660.
5. , , Ивницкий аммиака из желудочно-кишечного тракта в общий кровоток при внутрибрюшинном введении циклофосфана крысам // Бюл. эксп. биол. мед., 2010. — Т. 150, № 8. — С. 170-176.
6. Lorch, A. Single versus sequential high-dose chemotherapy in patients with relapsed or refractory germ cell tumors: a prospective randomized multicenter trial of the German Testicular Cancer Study Group / A. Lorch, C. Kollmannsberger, J. T. Hartmann [et al.] // J. Clin. Oncol. — 2007. — Vol. 25. — P. 2778—2784.
7. McDonald G. B., Slattery J. T., Bouvier M. E., et al. Cyclophosphamide metabolism, liver toxicity, and mortality following hematopoietic stem cell transplantation // Blood, 2003. —Vol. 101. — P. 2043–2048.
8. Reeds P. J., Burrin D. G. Glutamine and the bowel // J. Nutr., 2001. — Vol. 131. — P.2505S—2508S.
Подписи к рисункам
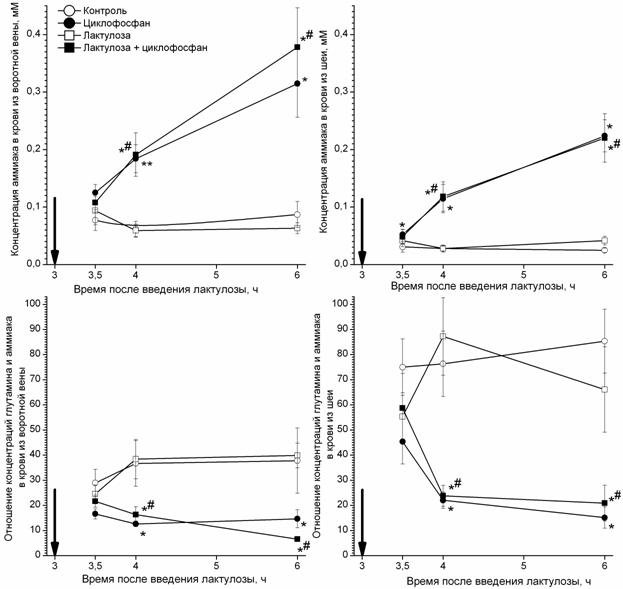
Рисунок 1. Влияние лактулозы на содержание аммиака и отношение
в крови крыс при острой интоксикации циклофосфаном (M ± m, n = 6)
Время введения циклофосфана показано стрелкой.
Значимые различия, p ≤ 0,05: * — с контрольной группой;
# — с животными, получавшими только лактулозу.
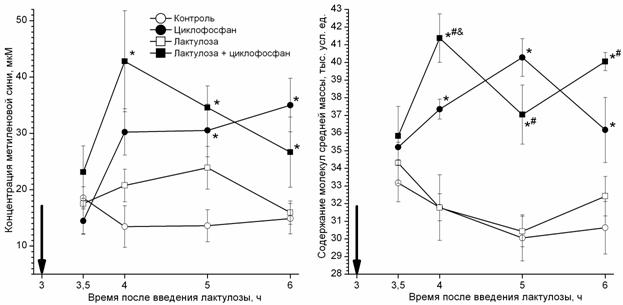
Рисунок 2. Влияние лактулозы на содержание веществ средней молярной массы в портальной крови крыс при острой интоксикации циклофосфаном (M±m, n=6).
Время введения циклофосфана (в/б) и метиленового синего (в/ж) показано стрелкой.
Значимые различия, p ≤ 0,05: * — с контрольной группой;
# — с животными, получавшими только лактулозу;
& — с животными, получавшими только циклофосфан.
Данные для построения рисунков
Рисунок 1. Влияние лактулозы на содержание аммиака и отношение глутамин/аммиак в крови крыс при острой интоксикации циклофосфаном (M±m, n=6).
* — Значимое различие с контрольной группой, р < 0,05
† — Значимое различие с животными, не получавшими лактулозу, р < 0,05
Верхний левый квадрант (по оси абсцисс — время после введения лактулозы, ч; по оси ординат — аммиак крови из v. portae, мМ):
Группа крыс | Срок после введения лактулозы, ч | ||
3,5 | 4,0 | 6,0 | |
Контроль | 0,077±0,018 | 0,062±0,013 | 0,087±0,022 |
Лактулоза | 0,094±0,025 | 0,059±0,011 | 0,063±0,010 |
Циклофосфан | 0,125±0,014 | 0,184±0,024* | 0,315±0,059* |
Лактулоза+циклофосфан | 0,108±0,017 | 0,191±0,039*# | 0,378±0,068*# |
Верхний правый квадрант (по оси абсцисс — время после введения лактулозы, ч; по оси ординат — аммиак крови из шеи, мМ):
Группа крыс | Срок после введения лактулозы, ч | ||
3,5 | 4,0 | 6,0 | |
Контроль | 0,031±0,009 | 0,028±0,006 | 0,025±0,004 |
Лактулоза | 0,042±0,011 | 0,028±0,004 | 0,042±0,008 |
Циклофосфан | 0,052±0,009 | 0,115±0,025* | 0,224±0,028* |
Лактулоза+циклофосфан | 0,049±0,013 | 0,118±0,026*# | 0,220±0,042*# |
Нижний левый квадрант (по оси абсцисс — время после введения лактулозы, ч; по оси ординат — отношение концентраций глутамина и аммиака в крови из v. portae):
Группа крыс | Срок после введения лактулозы, ч | ||
3,5 | 4,0 | 6,0 | |
Контроль | 29±5 | 37±9 | 38±13 |
Лактулоза | 25±4 | 38±8 | 40±5 |
Циклофосфан | 17±2* | 13±1* | 15±3* |
Лактулоза+циклофосфан | 22±2 | 16±3*# | 7±1*# |
Нижний правый квадрант (по оси абсцисс — время после введения лактулозы, ч; по оси ординат — отношение концентраций глутамина и аммиака в крови из шеи):
Группа крыс | Срок после введения лактулозы, ч | ||
3,5 | 4,0 | 6,0 | |
Контроль | 75±11 | 76±13 | 85±1 |
Лактулоза | 55±10 | 87±15 | 66±1 |
Циклофосфан | 45±9 | 22±3* | 15±4* |
Лактулоза+циклофосфан | 59±14 | 24±4*# | 21±7*# |
Значимые различия, p ≤ 0,05: * — с контрольной группой;
# — с животными, получавшими только лактулозу.
Рисунок 2. Влияние лактулозы на содержание веществ средней молярной массы в портальной крови крыс при острой интоксикации циклофосфаном (M±m, n=6).
* — Значимое различие с контрольной группой, р < 0,05
† — Значимое различие с животными, не получавшими лактулозу, р < 0,05
Левое поле (по оси абсцисс — время после введения лактулозы, ч; по оси ординат —содержание метиленового синего, мкМ):
Группа крыс | Срок после введения лактулозы, ч | |||
3,5 | 4,0 | 5,0 | 6,0 | |
Контроль | 18,5±2,0 | 13,5±3,7 | 13,6±2,8 | 14,9±2,7 |
Лактулоза | 17,5±5,4 | 20,8±2,9 | 23,9±3,8 | 15,9±2,1 |
Циклофосфан | 14,5±2,4 | 30,2±4,1 | 30,5±4,7* | 35,0±4,7* |
Лактулоза+циклофосфан | 23,1±4,6* | 42,8±8,9* | 34,6±3,8* | 26,7±6,2* |
Правое поле (по оси абсцисс — время после введения лактулозы, ч; по оси ординат —содержание эндогенных веществ средней молярной массы, условные единицы):
Группа крыс | Срок после введения лактулозы, ч | |||
3,5 | 4,0 | 5,0 | 6,0 | |
Контроль | 33171±1060 | 31789±758 | 30058±1311 | 30632±1487 |
Лактулоза | 34299±1175 | 31767±1858 | 30426±863 | 32417±1126 |
Циклофосфан | 35200±710 | 37353±569* | 40275±1075* | 36172±1843* |
Лактулоза+циклофосфан | 35836±1664 | 41372±1372*& | 37039±1675*# | 40045±515*# |
Значимые различия, p ≤ 0,05: * — с контрольной группой;
# — с животными, получавшими только лактулозу;
& — с животными, получавшими только циклофосфан.
Собственноручные подписи авторов:
Доктор медицинских наук | Владимир Леонидович Рейнюк |
Кандидат медицинских наук | Тимур Васильевич Шефер |
Кандидат химических наук | Константин Андреевич Краснов |
Доктор медицинских наук профессор | Юрий Юрьевич Ивницкий |
Реквизиты автора, осуществляющего связь с редакцией:
Рейнюк Владимир Леонидович, 198215 Санкт-Петербург, бульвар Новаторов, кВ 2,
Электронная почта: *****@***ru
Реферат
The influence of cyclophosphamide and lactulose on the flux
of gut ammonia and medium sized molecules into blood in rats
Vladimir L. Rejniuk, Timur V. Schäfer, Konstantin A. Krasnov, Jury Ju. Ivnitsky
Institute of Toxicology, Federal Medical Biological Agency, 1, ul. Bekhtereva, St. Petersburg, 192019 Russia
To estimate the influence of lactulose on neurological manifestations of the severe acute cyclophosphamide (C) intoxication, rats have been gavaged with 1.5 M solution of lactulose (30 mmol/kg) 3 h before C dosing (200, 600 or 1000 mg/kg). Within 3.0—6.0 h after the administration of lactulose, the pH of chymus in the caecum has been reduced by 1.0, the urease-dependent ammonia production in the chymus has been suppressed by 35%, the ammonia content increased by 38%. Within 3 h after C administration, the ammonia content in portal blood and in general circulation increased 3.6 and 9.0-fold, respectively; the glutamine/ammonia ratios decreased. The translocation of methylene blue, administered by the gavages, from chymus to portal blood has been intensified, as well as that of endogenous medium sized molecules. C-induced alterations of metabolism of ammonia and medium sized molecules have not been influenced by the administration of lactulose, as well as manifestations of C acute neurotoxicity and the lethal action of C. Therefore, the acidification of chymus by means of lactulose suppressed the chymus ammonia production while having no significant effect on C-induced translocation of gastrointestinal ammonia and medium sized molecules into blood, neurological manifestations of C intoxication and lethal action of C.
Keywords: Lactulose; Cyclophosphamide; Ammonia; Methylene blue; Medium sized molecules



