При анализе объектов с низким содержанием кислот объем пробы на одно титрование согласно стандартизированным методам равен 100 см3, что для двух параллельных определений требует достаточно большого объёма объекта. Чтобы показать возможность титрования растворов с небольшим содержанием кислот (опыты на примере с уксусной и муравьиной кислотами, рисунок 4), поступали следующим образом. Одновременно в три ячейки для титрования помещали 50 см3 пробы. Добавляли навеску сухой соли хлорида щелочного металла (2,9 – 3 г для хлорида натрия) до её концентрации в ячейке 1 моль/дм3 (этот приём позволил исключить разбавление анализируемого раствора), перемешивали магнитной мешалкой или воздухом, свободным от двуокиси углерода, до полного растворения соли. Продолжая перемешивание, включали регистрацию pH и источник тока. Так как при использовании трёх каналов регистрации наблюдалась задержка сигнала от каждого последующего сигнала, то запись текущих значений pH проводили с интервалом в три секунды. Отсюда следует неопределенность в точности измерения количества электричества, равная Dt∙100/tк, %, где Dt - время задержки сигнала, tк – время, затраченное на титрование до точки эквивалентности. При Dt = 3 с и tк = 1000 с относительная погрешность равна 0,3%.
Концентрацию уксусной и муравьиной кислот определяли по формуле
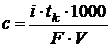 , (3)
, (3)
где c – концентрация кислоты, моль/дм3;
i – сила тока, А; tk – время, затраченное на титрование, с;
F – число Фарадея, 96500 Кл/моль;
V – объём анализируемой пробы, 50 см3.
При расчете концентраций учитывали разбавление пробы.
На рисунке 6 приведены кривые титрования образцов яблочного сока (а) и безалкогольных напитков: пепси-колы (б), фанты (в) и спрайта (г), взятых в торговой сети. Титрование проводили током 0,020 А в трёхзвенной ячейке. Результаты титрования (расчет кислотности) приведены в таблице 1. Так как по требованиям национального стандарта [72] кислотность (x) в безалкогольных напитках определяют объёмом гидроокиси натрия с(NaOH) = 1 моль/дм3, израсходованным на титрование 100 см3 проанализированного продукта, в см3, то данные столбца 2 из таблице 1 пересчитывали в соответствии с требованиями стандартного метода [72] по формуле: x = c∙100 (столбец 3). Для соков в соответствии с требованиями стандартизированной методики титруемая кислотность рассчитывается на содержание превалирующей кислоты (для яблочного сока – яблочная кислота) [73], однако для удобства сравнения результатов анализа, полученных разными методами, показатели кислотности приведены в единых единицах измерений согласно требованиям методики [71] для всех образцов, включая яблочный сок, и представлены как объем раствора гидроокиси натрия с(NaOH) = 0,1 моль/дм3, использованный на титрование 100 см3 пробы (таблица 1, столбцы 3 и 4). Как видно из таблицы 1, результаты, полученные по новой методике, совпадают с результатами стандартных методов. Следует отметить, что стандартный метод требует удаления углекислого газа кипячением раствора и постоянного внесения поправки на отклонение концентрации гидроокиси натрия от номинала. В нашем методе двуокись углерода удаляется продувкой, а концентрация основания определяется током генерации. Методика позволяет точно определять кислотность в темноокрашенных напитках без ошибки оператора на визуальную фиксацию перехода окраски индикатора.
Таким образом, нами впервые предложена трехзвенная электролитическая ячейка для одновременного исследования трех проб методом непрерывного потенциометрического титрования кулонометрически генерированным основанием, что повысило в три раза экспрессность анализа и позволило усовершенствовать метод с использованием обычной кулонометрической ячейкой. Разработана методология эксперимента. Показана возможность применения данной установки для определения кислотности вин, соков и безалкогольных напитков одновременно в трёх пробах. В результате анализа кривых титрования индивидуальных кислот, так и проб виноградных вин, предложены специфические критерии, которые могут быть использованы для оценки подлинности и качества готовой продукции.
Растворы кислот готовили из реактивов не ниже квалификации ч. д.а. на бидистиллированной воде, хранящейся под слоем азота для исключения попадания углекислого газа. Величину рН раствора в процессе титрования кулонометрически генерированным основанием измеряли с помощью анализатора жидкости стандартной точности (модели "Эксперт-001-3(0.1)", "Эксперт-001-3(0.4)") в электрохимической ячейке, состоящей из термостатированного стакана, лабораторного комбинированного pH-электрода общего назначения марки ЭСК-10307. В ячейку помещались генерирующие электроды (графитовый катод и серебряный анод) и с помощью источника постоянного тока Б5 – 49 задавался необходимый ток генерации.
Массовые концентрации катионов щелочных и щёлочноземельных металлов и аминокислот определяли методом электрофоретического разделения на приборе для капиллярного электрофореза «Капель-105» по разработанным в ГНУ СКЗНИИСиВ методикам. Титруемую кислотность в виноматериалах находили по ГОСТ Р 51621-2000 [79].
Математическую обработку экспериментальных данных проводили с помощью персонального компьютера в математическом пакете Mathcad. Одномолярный фоновый раствор хлористого калия готовили следующим образом: необходимую навеску ![]() квалификации х. ч. увлажняли небольшим количеством соляной кислоты для разрушения карбонатов, затем высушивали и прокаливали в муфельной печи до постоянного веса при температуре 200 °С для удаления избытка
квалификации х. ч. увлажняли небольшим количеством соляной кислоты для разрушения карбонатов, затем высушивали и прокаливали в муфельной печи до постоянного веса при температуре 200 °С для удаления избытка ![]() . Рабочий раствор готовили непосредственно перед работой на дистиллированной воде, свободной от углекислого газа. Раствор перемешивали воздухом, свободным от углекислого газа. То, что в процессе титрования не происходило разбавления титранта, упрощало расчёты и уменьшало вероятность влияния угольной кислоты. При титровании в среде постороннего электролита с постоянной ионной силой раствора коэффициенты активности находили по калибровке соляной кислотой. В некоторых случаях вначале определяли смешанные константы, то есть принимали в первом приближении, что
. Рабочий раствор готовили непосредственно перед работой на дистиллированной воде, свободной от углекислого газа. Раствор перемешивали воздухом, свободным от углекислого газа. То, что в процессе титрования не происходило разбавления титранта, упрощало расчёты и уменьшало вероятность влияния угольной кислоты. При титровании в среде постороннего электролита с постоянной ионной силой раствора коэффициенты активности находили по калибровке соляной кислотой. В некоторых случаях вначале определяли смешанные константы, то есть принимали в первом приближении, что 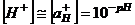 . Применяли химически чистые кислоты.
. Применяли химически чистые кислоты.
Для подтверждения правильности сделанных выводов, в обсуждении результатов диссертации, использованы справочные данные и работы других авторов. Кроме того, при анализе ряда выдвинутых положений использованы литературные данные по строению кристаллической решетки рассматриваемых кислот.
Для автоматизации опытов была использована экспериментальная установка как для разового потенциометрического титрования одной пробы, так и для одновременного титрования нескольких проб с кулонометрической генерацией основания.
Комплекс кулонометрического титрования кислот с автоматической записью кривых титрования создан на базе анализатора жидкости «ЭКСПЕРТ-001», персонального компьютера, источника стабилизированного тока и специальной ячейки.
Ячейка состоит из серебряного анода и графитового катода, в ней нет диафрагмы, разделяющей катодное и анодное пространство. На аноде выделяется осадок хлорида серебра, который выполняет роль диафрагмы, а на катоде - газообразный водород, препятствующий поглощению углекислого газа из воздуха раствором. Именно такая конструкция значительно увеличивает точность титрования. Мы добились относительной погрешности 0,2%, что ниже капельной ошибки. Электролиз ведётся до появления четкого скачка рН на кривой титрования, записываемой прибором. Для регенерации анода необходимо погрузить его на ночь в разделённый диафрагмой стакан, заполненный раствором хлоридом натрия, подкисленным 1 моль/дм3 ![]() . В одну из камер помещали пластинку цинка, в другую серебряный анод и замыкали электроды. Чтобы показать возможность титрования растворов с небольшим содержанием кислот (опыты с уксусной и муравьиной кислотой) поступали следующим образом. В ячейки для титрования помещали 50 см3 пробы и добавляли навеску сухой соли хлорида щелочного металла до его концентрации в ячейке 1 моль/дм3 (этот приём позволил исключить разбавление анализируемого раствора) и перемешивали магнитной мешалкой или воздухом, свободным от двуокиси углерода, до полного растворения соли. Включали перемешивание, регистрацию рН и источник тока. Так как при использовании трёх каналов регистрации наблюдается задержка сигнала от каждого последующего сигнала, то запись текущих значений рН проводили с интервалом в три секунды. Отсюда следует неопределенность в точности измерения количества электричества примерно равная
. В одну из камер помещали пластинку цинка, в другую серебряный анод и замыкали электроды. Чтобы показать возможность титрования растворов с небольшим содержанием кислот (опыты с уксусной и муравьиной кислотой) поступали следующим образом. В ячейки для титрования помещали 50 см3 пробы и добавляли навеску сухой соли хлорида щелочного металла до его концентрации в ячейке 1 моль/дм3 (этот приём позволил исключить разбавление анализируемого раствора) и перемешивали магнитной мешалкой или воздухом, свободным от двуокиси углерода, до полного растворения соли. Включали перемешивание, регистрацию рН и источник тока. Так как при использовании трёх каналов регистрации наблюдается задержка сигнала от каждого последующего сигнала, то запись текущих значений рН проводили с интервалом в три секунды. Отсюда следует неопределенность в точности измерения количества электричества примерно равная ![]() t×100/tk, %. Здесь
t×100/tk, %. Здесь ![]() t - время задержки сигнала, tk - время, затраченное на титрование до точки эквивалентности. При
t - время задержки сигнала, tk - время, затраченное на титрование до точки эквивалентности. При ![]() t =3 с и tk = 1000 с ошибка равна 0,3%.
t =3 с и tk = 1000 с ошибка равна 0,3%.
Проведено титрование ряда неорганических и органических кислот в модельных смесях и реальных объектах.
Установка работает стабильно при значениях тока от 0,1 до 50 мА. Методика позволяет практически исключить влияние диоксида углерода, в то время как при обычном титровании кислот, точность определения осложняется трудностью получения раствора основания, не содержащего карбонатов, образующихся при поглощении углекислого газа из воздуха. Ниже будет показано, что ввиду высокой информативности кривой титрования можно отделить область влияния углекислого газа. Существенным преимуществом предлагаемого способа является исключение разбавления раствора титрантом.
Кроме того, результат дает детальную информацию об экстремальных участках кривой титрования, что позволяет интерпретировать механизм изучаемого процесса.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 |



