Для оценки эмоционального состояния крыс используют следующие показатели:
Длительность реакции груминга (с). Груминг у грызунов представляет собой чрезвычайно распространенную форму поведения, выполняющую в организме ряд важных функций – уход за кожей и шерстью, терморегуляцию, распределение химических веществ и др.
Короткий груминг характеризуется 1 – 2 быстрыми круговыми движениями лап вокруг носа и небольшой области около него, а длительный груминг характеризуется умыванием области глаз, заведением лап за уши и переходом на умывание всей головы, лап, боков, туловища, ано-генитальной области, хвоста. Реакция груминга в эмоциогенных ситуациях является смешанной реакцией, отражающей наличие эмоциогенного напряжения. У грызунов груминг специфически активируется при действии стресса, и поэтому считается одним из его поведенческих маркеров.
Продолжительность реакции замирания (с). Фризинг рассматривается как показатель сильного стресса, вызванного помещением животного в незнакомую обстановку.
Длительность реакции принюхивания (с).
Кроме того после окончания теста и помещения животного в домашнюю клетку следует подсчитать количество болюсов (уровень дефекации), являющееся индексом "эмоциональности" животного.
Полученные результаты занести в таблицу (М ± SEM, n=5):
Сроки исследования | Интактные | Ложно оперированные животные | Ишемия (0,9% раствор NaCl) |
Горизонтальная активность (пройденное расстояние за 5 мин) | |||
Фон | |||
10 дней | |||
Вертикальная активность (количество вертикальных стоек за 5 мин) | |||
Фон | |||
10 дней | |||
Длительность груминга, с | |||
Фон | |||
10 дней | |||
Длительность реакции замирания, с | |||
Фон | |||
10 дней | |||
Длительность реакции принюхивания, с | |||
Фон | |||
10 дней |
Вопросы:
1. Какие нарушения можно выявить по результатам теста «открытое поле»?
2. О чем могут свидетельствовать частые и длительные эпизоды замирания, низкая подвижность и редкие вертикальные стойки в тесте «открытое поле»?
Лабораторная работа №5.
Тест «Водный лабиринт Морриса»
Для исследования пространственного обучения и памяти у крыс в тесте Морриса используют цилиндрический бассейн, который показан на рисунке 4, диаметром 120 см (Morris Water Maze LE820120, PanLab/Harvard Apparatus, Испания) заполненный непрозрачной водой, в которую погружена небольшая (10 см) невидимая платформа. Схема зон бассейна представлена на рисунке 5.

Рисунок 4. Тестирование пространственной памяти в «водном лабиринте Морриса»
Протокол теста состоит из пяти сеансов обучения, по пять проб в каждом для крысы. Сеансы проводят в одно и тоже время суток с интервалом 48 ч в течение 10 дней до проведения операции по моделированию ишемии. Помещение животных в бассейн в течение всего эксперимента производят напротив платформы у противоположной стенки. Максимальная длительность пробы составляет 60 – 120 с. В процессе обучения после обнаружения платформы животному позволяется находиться на ней 30 с, затем проба повторяется 5 раз.
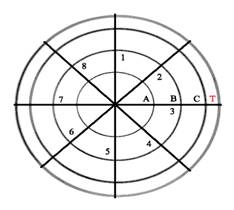
Рисунок 5. Схема зон бассейна водного лабиринта Морриса: зона Т – зона тигмотаксиса, зоны А, В и С – дополнительные внутренние зоны бассейна, 1-8 – номера секторов бассейна
Треки животного фиксируются с помощью установки для видеорегистрации данных. Анализ данных выполняется с помощью программы FreeTrack. Так как программа видеорегистрации работает по принципу контрастности, эксперимент для белых животных проводится в темной комнате.
Отбираются животные, способные к обучению и формированию пространственной памяти. Для оценки научения поиску в качестве стандартного критерия используют латентность решения задачи. Количественную оценку этого критерия проводят с помощью индивидуального коэффициента сохранения (Кс), значение которого равняется отношению суммы латентных периодов нахождения платформы в первом сеансе к сумме латентных периодов в каком-либо из последующих сеансов (Кс1 – отражает выполнение задачи во втором сеансе научения по сравнению с первым; Кс2 – в третьем сеансе по сравнению с первым и т. д.). Соответственно, чем выше Кс, тем быстрее происходит научение.
Через 10 суток постишемического периода проводят тестирование на сохранение долговременной памяти: тест состоит из одной пробы длительностью 100 с. При этом платформа в лабиринте отсутствует.
Определяют отсроченный коэффициент сохранения (оКс). оКс – доля времени пребывания крысы в квадранте, где находилась платформа, по отношению в общему времени пребывания крысы в водном лабиринте Морриса.
При этом считается нормой, если животное провело в квадранте, где находилась платформа, около 25 % общего времени пребывания в лабиринте.
Полученные данные занести в таблицу:
Сроки исследования | Интактные | Ложно оперированные животные | Ишемия (0,9% раствор NaCl) |
Вопрос:
1. Какие виды памяти исследуют в тесте «Водный лабиринт Морриса»?
ТЕМА №3
«Биохимические маркеры ишемического повреждения»
Снижение перфузии ткани мозга сопровождается уменьшенной доставкой кислорода из кровеносного русла к клеткам, где он участвует в реакциях аэробного образования энергии, так как является субстратом терминального фермента митохондриальной дыхательной цепи – цитохромоксидазы. Развивающееся гипоксическое состояние представляет собой сложный фазный процесс, приводящий к переключению на анаэробный энергетический путь и накоплению молочной кислоты (лактата).
В адаптивных реакциях мозга принимают участие различные нейрохимические системы. Среди них особую роль отводят нейротрофическим факторам (NGF, BDNF, NT3, NT4) и внутриклеточным ферментам, такими как нейронспецифическая енолаза (НСЕ), лактатдегидрогеназа (ЛДГ), креатинкиназа (КК). Главной особенностью нейротрофических факторов является не только способность контролировать развитие нервной системы, миграцию и дифференциацию нервных клеток, но и участвовать в модификации метаболизма.
Лабораторная работа №6
«Оценка тканевой гипоксии по соотношению лактат/пируват в ткани головного мозга»
С целью максимально быстрой фиксации ткани для прекращения метаболических реакций и сохранения уровня субстратов применялся метод замораживания мозга.
Замороженные, с помощью жидкого азота, полушария головного мозга гомогенизиуют в фарфоровой ступке, охлажденной жидким азотом. Далее гомогенат депротеинизируют 5% раствором хлорной кислоты (НСlО4).
Тканевой экстракт для определения глюкозы, пирувата и лактата готовят из расчета: 2 г ткани на 6,5 мл НСlО4. Выдерживают на холоде в течение 15 минут и производят центрифугирование при 3000 g 15 мин.
Получившийся супернатант переносят во взвешенную заранее охлажденную центрифужную пробирку (m1). Определяют массу пробирки с супернатантом (m2). Производят нейтрализацию хлорной кислоты 69% раствором углекислого калия (К2СО3), доводя рН до 7,0 (рН определяют при помощи индикаторной бумаги). Определяют массу пробирок с измененной рН (m3).
Для осаждения перхлоратов калия пробирку оставляют на холоде на 10 мин, затем центрифугируют при 3000 g 5 мин. Надосадочную жидкость сливают в чистую пробирку. Количественное содержание субстратов в ткани мозга выражают в микроМолях исследуемого вещества на 1 г влажной ткани (мкмоль/г).
Определение концентрации пировиноградной кислоты (пируват)
Принцип метода:
Пируват в присутствии НАДН и ЛДГ восстанавливается до лактата по реакции:
Пируват + НАДН + Н+ → лактат + НАД+
Количество использованного в реакции пирувата эквивалентно количеству НАДН, убыль которого регистрируется при длине волны 340 нм.
Ход определения:
Для определения концентрации пирувата в пробирки наливают 2 мл 0,5 М трис-буфера (рН = 6,9), 0,6 мл тканевого экстракта и аккуратно перемешивают. Затем добавляют 0,05 мл 6 мМ НАДН2 и снова перемешивают. На спектрофотометре определяют оптическую плотность E1 (λ = 340 нм). После спектрофотометрирования добавляют в растворы 1,0 мл ЛДГ (5Е белка/мл) и через 20 мин повторно определяют оптическую плотность (Е2.).
Расчет концентрации:
Концентрацию пирувата рассчитывали по формулам:
Mпир = ∆E* V * K/6,22; K = (mo + 3,3)*(m3-m1)/mo-(m2-m1); где
М – концентрация субстрата в мкмоль/г влажной ткани;
∆E – разница экстинкции от начала и до полного окончания реакции
Е1 – Е2;
V – объём пробы, мл;
6,22 – коэффициент микромолярной экстинкции восстановленной формы пиридиннуклеотидов;
К – коэффициент разведения по отношению к 1 г ткани;
mo – объём ткани для анализа,
m1 – масса стеклянной пробирки,
m2 – масса пробирки с фильтратом,
m3 – масса пробирки после нейтрализации.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



