Таблица 4. Спектр тромбофилии у пациенток с аномальным расположением плаценты и синдромом потери плода
Спектр тромбофилии абс. (%) | Предлежание плаценты при данной беременности n=15 | Предлежание плаценты в анамнезе n=30 | Предлежание плаценты и СПП в анамнезе n=21 | Все обследованные n=66 |
Генетическая тромбофилия | 13 (86,7%) | 20 (66,7%) | 15 (71,4%) | 48 (72,7%) |
Мультигенная тромбофилия | 13 (86,7%) | 6 (20%) | 4 (19%) | 23 (34,8%) |
Сочетанная тромбофилия | 10 (66,7%) | 8 (26,7%) | 3 (14,2%) | 21 (31,8%) |
АФС | 2 (13,3%) | 10 (33,3%) | 4 (19%) | 16 (24,2%) |
FV Leiden | 2 (13,3%) +/+ +/- | 1 (3%) +/+ +/- | 2 (9,5%) | 5 (7,5%) |
MTHFR C 677T | +/+2 (13,3%) +/-3 (20%) | +/+3 (10%) +/-5 (16,7%) | +/+ 1 (4,7%) +/-4 (19%) | 6 (9%) 12 (18,1%) |
MTHFD 1958 G/A | +/+ (-) +/- (-)1 (6,6%) | +/+ (-) +/- (-) | +/+ (-) +/- (-) | 1 (1,5%) |
MTHFR 1298 A/C | +/+ (-) 1 (6,6%) +/- (-) | +/+2 (6,7%) +/-1 (3%) | +/+ 1 (4,7%) +/-1 (4,7%) | 4 (6%) 2 (3%) |
2756 метионин синтазы (МТS) | +/+(-) +/-(-) | +/+(-) +/-4 (13,3%) | +/+1 (4,7%) +/-1 (4,7%) | 1 (1,5%) 5 (7,6%) |
46 A/G редуктазы метионинсинтетазы (MTRR) | +/+ (-) +/- (-) | +/+ (-) 1(3%) +/- (-) | +/+ (-) +/- (-)1 (4,7%) | 1 (1,5%) 1 (1,5%) |
675 4 G/5G РА1-1 | +/+ (-) 2 (13,3%) +/- (-) | +/+ 3 (10%) +/- 2 (6,7%) | +/+ (-) +/- (-) 2 (9,5%) | 5 (7,6%) 4 (6%) |
L/D тканевого активатора плазминогена ТРА | +/+ (-) +/- 1 (6,6%) | +/+ 2 (6,7%) +/- 1 (3%) | +/+ 1 (4,7%) +/- (-) | 3 (4,5%) 2 (3%) |
Фибриноген | +/+ (-) +/- (-) | +/+ 1 (3%) +/- (-) | +/+ (-) +/- 1 (4,7%) | 1 (1,5%) 1 (1,5%) |
F Hag 46 C/T | +/+ 1 (6,6%) +/+ (-) | +/+ (-) +/- 2 (6,7%) | +/+ (-) +/- 1 (4,7%) | 1 (1,5%) 3 (4,5%) |
Примечание: Нет мутации -/-; гетерозиготная форма мутации +/-; гомозиготная форма +/+.
Учитывая высокую частоту тромбофилии у пациенток с аномальным расположение плаценты по клиническим группам (рисунок 1), предлежание плаценты при данной беременности n=15 выявлен высокий процент генетической тромбофилии - 86,7%; предлежание плаценты в анамнезе n=30 генетическая тромбофилия составила - 66,7%; предлежание плаценты и СПП в анамнезе n=21 генетическая тромбофилия составила - 71,4%.Это позволило нам выдвенуть суждение о ранней профилактике осложнений во время беременности, коррекции дозы НМГ в зависимости от срока беременности, и данных системы гемостаза, а также в послеродовом периоде.
Рисунок 1. Частота и спектр генетической и приобретенной тромбофилии

Данные, указанные в таблице 5, позволили нам предположить наличие причинно-следственных связей между тромбофилией и аномалиями прикрепления плаценты, прогнозировать отягощенное течение беременности, СПП, предлежание плаценты, возникновение тромбогеморрагических осложнений у таких пациенток и дали возможность предупредить и минимизировать в дальнейшем эти осложнения.
Таблица 5. Спектр тромбофилии у пациенток с СПП в анамнезе
Мутации (полиморфизмы) абс. (%) | Предлежание плаценты при данной беременности n=15 | Предлежа ние плаценты в анамнезе n=30 | Предлежание плаценты и СПП в анамнезе n=21 | Все обследованные n=66 |
MTHERC 677T | +/+ 1(6,7%) +/-2(13,3%) | +/+2(6,7%) +/-4(13,3%) | +/+1 (4,8%) +/-3(14,2%) | 13(14,6%) |
FV Leiden | +/+2(13,3%) +/-(-) | +/+(-) +/-1(3,3%) | +/+(-) +/-2(9,5%) | 5(7,6%) |
PtG20210A | +/+(-);+/-1(6,7%) | +/+(-);+/-(-) | +/+(-);+/-(-) | 1(1,5%) |
Полиморфизмы 6754 G/5 G в гене ингибитора активатора плазминогена 1 типа РА1-1 | +/+1(6,7%) +/-(-) | +/+2(6,7%) +/-1(3,3%) | +/+(-) +/-1(4,8%) | 5(7,6%) |
Примечание: Нет мутации -/-; гетерозиготная форма мутации +/-; гомозиготная форма +/+.
Из рисунка 2, мы считаем целесообразным пациенток с предлежанием плаценты в анамнезе, равно как при данной беременности, обследовать с целью выявления генетического гипофибринолиза и циркуляции АФА. Это позволит предотвратить как дефекты имплантации и плацентации, так и частоту акушерских кровотечений, а соответственно – снизить материнскую смертность и улучшить перинатальные исходы.
Рисунок 2. Структура тромбофилии у пациенток с аномальным расположением плаценты
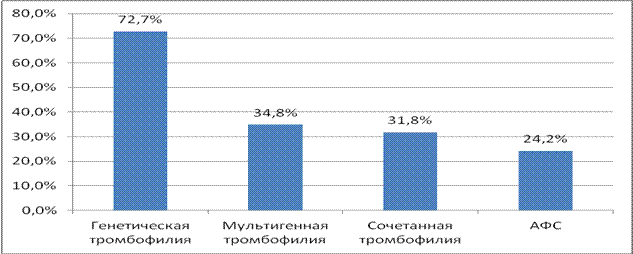
У всех обследованных пациенток с предлежанием плаценты выявляются генетические и приобретенные тромбофилии, оказывающие влияние на течение и исход беременности. В связи с этим мы предлагаем проводить скрининг на наличие генетической тромбофилии у пациенток с аномальным расположением плаценты.
Выводы
1. Пациенткам как с синдромом потери плода и предлежанием плаценты в анамнезе, так и с предлежанием плаценты при данной беременности необходимо обследование на приобретенную и генетическую тромбофилию.
2. Пациентки с предлежанием плаценты, ранними преэмбрионическими потерями, СПКЯ являются группой риска по невынашиванию беременности и формированию предлежания плаценты, а также по формированию тромбогеморрагических осложнений в родах.
3. У пациенток с предлежанием плаценты и синдромом потери плода в 72,7% случаев выявлена генетическая тромбофилия. При этом мутации FV Leiden - 7,5%.
Полиморфизмы 675 4G/5G в гене ингибитора активатора плазминогена 1 типа РА1-1 выявлены у 5 пациенток – гомозиготная форма, что составляет 7,6%; гетерозиготная форма составляет 4 пациентки – 6%.
Полиморфизм «1/D» в гене активатора плазминогена выявлен у 3 пациенток – гомозиготная форма, что составляет 4,5%; гетерозиготная форма составляет 2 пациентки – 3%.
Полиморфизмы F Hag «46 С/Т» выявлены у 1 пациентки, – гомозиготная форма, что составляет 1,5%; гетерозиготная форма составляет 3 пациентки – 4,5%.
У 24,2% пациенток определяется АФС-синдром.
4. Применение низкомолекулярного гепарина, антиоксидантов, витаминов группы В, натурального прогестерона начинается с фертильного цикла и в течение всей беременности, что позволяет предотвратить повторные потери плода у женщин с сочетанными формами тромбофилии, предлежанием плаценты и СПП в анамнезе.
5. Индивидуализация ведения пациенток с предлежанием плаценты и тромбофилией, с динамическим контролем маркерами тромбофилии, циркуляции АФС-антител позволила снизить риск отягощенного течения беременности.
6. У пациенток с предлежанием плаценты в анамнезе и тромбофилией последующая беременность должна планироваться с учетом патогенетических механизмов скрытых генетических дефектов гемостаза.
Практические рекомендации
1. Всем пациенткам с предлежанием плаценты в анамнезе и при данной беременности необходимо исследование на наличие исходных дефектов системы гемостаза, в первую очередь выявление циркуляции АФС, антигенов и антител к кофакторам фосфолипидов, полиморфизма 6754 G/5G, РАI -1, 1/D, тканевого активатора плазминогена 1, F Hag 46 C/T.
2. Генетически обусловленный гипофибринолиз, а также его сочетание с АФС-синдромом и другими формами тромбофилии у пациенток с ранними преэмбрионическими потерями, СПКЯ является показанием для назначения НМГ (низкомолекулярных гепаринов: фраксипарин, клексан), антиоксидантной и витаминотерапии в предгравидарном периоде.
3. У пациенток с тромбофилией и placenta pravia в анамнезе необходимо проводить профилактическую терапию в фертильном цикле и во время беременности, обязательно при динамическом контроле за уровнем маркеров ДВС-синдрома, общеоценочных гемостазиологических тестов. К ним относятся:
1) АЧТВ, ПИ, тромбоэластограмма, функциональная активность тромбоцитов, факторов свертывания крови;
2) время акклюзии сосуда;
3) маркеры ДВС-синдрома (РКМФ, Д-димер).
4. При обнаружении резко повышенных маркеров ДВС-синдрома у пациенток с предлежанием плаценты показано обследование на генетическую тромбофилию.
5. При выявлении невыраженных признаков активации внутрисосудистого свертывания крови (Д-димера, гипер - или гипоагрегации тромбоцитов) показано исследование на циркуляцию АФ-антител, кофакторов к фосфолипидам, уровень гомоцистеинемии.
6. Ведение пациенток с предлежанием плаценты и тромбофилией должно быть индивидуально с учетом выявленных дефектов гемостаза: при динамическом контроле за реальными маркерами тромбофилии (Д-димер, кофактор к фосфолипидам) патогенетическая терапия включает в себя низкомолекулярный гепарин, лечебную дозу фолиевой кислоты, антиагрегантную, антиоксидантную и иммуноглобулинотерапию.
Список работ, опубликованных по теме диссертации
1) , Бадалова и приобретенная формы тромбофилии в генезе предлежания плаценты. // Материалы IX Всероссийского научного форума «Мать и дитя». - Москва, 2007. – с.18-19.
2) Бадалова значение определения молекулярных маркеров тромбофилии и эндотелиопатии у пациенток с метаболическим синдромом и отягощенным акушерским анамнезом. // Материалы IX Всероссийского научного форума «Мать и дитя». – Москва, 2007. – с.329-330.
3) Бадалова ведения беременности у пациенток с предлежанием плаценты и тромбофилией. // «Врач» 2011-№8-с.78-80.
4) Бадалова синдром и аномалии прикрепления плаценты. // «Врач» 2011-№11-с.65-67.
5) Бадалова -диагностическая значимость полиморфизма генов, предрасполагающих к развитию воспаления и тромбофилии. // «Врач» 2012- №1-с.83-84.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



