1) нафтеновые кислоты
2) смоляные кислоты – канифоли.
По виду метало - сиккативы могут быть:
- свинцовые
- кальциевые
- кобальтовые
- цинковые
- марганцевые
- ванадиевые
- железные
Сиккатив получают нагреванием льняного масла с оксидами указанных металлов (нафтенаты) или реакцией нейтрализации соответствующих гидроксидов канифолью.
Каталитическая активность сиккативов определяется способность металла, переходить от устойчивой наименьшей степени окисления в менее устойчивое состояние с высшей степенью окисления.
(RCOO)2Fe + ~ CH-CH=CH~ → (RCOO)2OHFe3+ + ~ CH-CH=CH~ →
׀ ׀
OOH •O
→ ~ CH-CH=CH~
׀
O
׀
O
׀
~ CH-CH=CH~
Me2+ + OH - → Me3+ + •OH
На практике чаще используют набор сиккативов, так как каждый из них обладает и ценными, и негативными свойствами.
Кобальтовые сиккативы.
- способствуют эффективному высыханию наружной ленки, а подпленочная масса остается жидкой, что ведет к образованию “морщин”, наплывов.
Свинцовые сиккативы.
- наиболее часто используемые сиккативы объемного действия. Недостаток – токсичность, а также вследствие возможности высаждения PbS, происходит помутнение покрытия. Поэтому свинцовые сиккативы в отдельности не используют.
Марганцевые сиккативы.
- ускоряют испарение с поверхности и с объема, но, исходя из того, что светлый Mn2+ переходит в темный Mn3+, его нельзя использовать в светлых красках. Кроме того, все остальные сиккативы, взятые в избытке, ускоряют процесс высыхания, вплоть до деструкции, а избыток Mn уменьшает скорость высыхания.
Железные сиккативы.
- придают некрасивый цвет, его используют в дешевых желтых красках.
Кальциевые сиккативы.
- используют в добавлении к Pb-Mn, они препятствуют высаждению PbS и помутнению покрытия, ускоряют сушку при низких температурах.
Алюминиевые сиккативы.
- объемного действия. Нетоксичны, хорошо сохраняют цвет, но для их приготовления необходимо специальное дорогостоящее связующее, что затрудняет и удорожает производство.
Сиккативы продолжают действовать, находясь в твердой пленке, что может привести к деструкции пленкообразователя, растрескиванию покрытия. Поэтому их нужно вводить по рецептуре не более 2% от массы пленкообразователя.
Природные смолы.
Канифоль.
Канифоль - это смола хвойных деревьев. В сосновой смоле 30 % канифоли, основное - скипидар.
Первый способ получения канифоли состоит в том, что из живицы отгоняют скипидар, а остающееся вещество- канифоль.
Второй способ получения канифоли: старые пни сосновых деревьев измельчают и заливают органическими растворителями, фильтруют и отгоняют легкокипящие растворители. В остатке- канифоль.
С19Н29СООН
![]()
![]() СН3 СООН
СН3 СООН



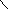 СН3
СН3
![]()
![]() СН СН3
СН СН3
СН3
![]()
![]() СН3 СООН
СН3 СООН


 левокимаровая
левокимаровая
кислота
![]()
![]()
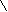
![]() СН3
СН3
![]()
![]() СН СН3
СН СН3
СН3
![]()
![]()


 СН3 СООН декстрокимаровая
СН3 СООН декстрокимаровая
кислота
![]() СН3
СН3
![]()
![]()
![]() СН СН2
СН СН2
СН3
Канифоль - хрупкая стеклообразная масса от светло - желтого до темно - коричневого цвета с температурой размягчения 50- 70 0С. Хорошо растворима во всех органических растворителях и в маслах.
Как самостоятельный пленкообразователь она не испаряется, так как очень хрупкая и имеет высокое КЧ (150- 170). Чаще всего ее используют как модификатор фенолоформальдегидных и алкидных смол для придания блеска.
Часто используют канифольные эфиры и малеиновый аддукт.
Эфиры канифоли получают из глицерина.

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() СН2 СН СН2 + 3 С19Н29СООН СН2 СН СН2 + 3Н2О
СН2 СН СН2 + 3 С19Н29СООН СН2 СН СН2 + 3Н2О

![]()
![]() ОН ОН ОН О О О
ОН ОН ОН О О О

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() С О С О С О
С О С О С О
С19Н29 С19Н29 С19Н29
Глицериновый эфир канифоли имеет температуру размягчения 75- 77 0С.
А пентанитритовый эфир канифоли 100- 105 0С.
КЧ этих эфиров 15- 20 мг КОН/1г эфира.
Эфиры канифолей используют как добавки к маслам, лакам для придания твердости и глянца, а к нитроцеллюлозным краскам для улучшения адгезии.
Соли канифольных кислот называют резинаты и используют в качнстве секкативов.
![]()
![]()
![]()
![]() СН3 СООН О
СН3 СООН О


![]()
![]()

 СН С
СН С

![]() + О
+ О
![]()
![]()
![]()
![]()

![]() СН С
СН С
![]()
![]() СН3 О
СН3 О

![]() СН СН3
СН СН3
СН3
![]()
![]() СН3 СООН
СН3 СООН
![]()
![]()

 О
О

![]()
![]()

![]()
![]() СН С
СН С

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



