Достоинством установки является комплексное решение вопросов санитарной очистки больших объёмов вентвыбросов с глубокой утилизацией тепла.
Технологический процесс сжигания газовых выбросов и утилизации тепла состоит из следующих стадий:
1. Сжигание газовых выбросов в реакторах с использованием в качестве топлива природного газа или мазута;
2. Утилизация тепла дымовых газов после реактора для получения пара в котлах;
3. Утилизация тепла дымовых газов после котла-утилизатора в экономайзере для подогрева теплофикационной воды от 70°С до 100°С.
При сгорании органические вещества выделяют определенное количество энергии что позволяет рассматривать их не только как обезвреживаемый компонент, но и как вторичный энергоресурс.
Общим для всех методов является окисление примеси в ГВВ с помощью кислорода воздуха до СО2, Н2О, N2 и других соединений, причем, важнейшими характеристиками процесса, независимо от технического метода окисления являются тепловой эффект и константа равновесия. Последнюю обычно вычисляют через теплоту и энтропию реакции.
Целью рассмотренного ниже расчета является снижение концентрации примеси ГВВ от исходной концентрации С0 до значения ПДК в воздухе путем окисления ацетона до безвредных веществ.
Теплота сгорания паров ацетона
Первый закон термодинамики позволяет рассчитать теплоту химического процесса:
Qр = ∆Н = ∆U + ∆νRT.
Из уравнения видно, что тепловые эффекты ∆Н и ∆U = Qν различаются на величину ∆νRT, где ∆ν – разница стехиометрических коэффициентов продуктов реакции и исходных веществ.
В газофазном процессе ∆νRT может быть достаточно большой величиной. При составлении уравнения реакции сгорания (окисления) необходимо, чтобы стехиометрический коэффициент был равен единице. Тогда дальнейшие расчеты будут отнесены к 1 молю целевого компонента. Это упростит материальные балансы процесса. Так, при сгорании паров ацетона:
С3Н6О (г) + 4О2 → 3СО2(г) + 3Н2О(г)
Вступает в реакцию (4 +1) моль газов, а получается (3 +3) моль, т. е. ∆ν =3 + 3 – (4 + 1) = 1.
Тепловой эффект реакции ∆Н или ∆U может быть рассчитан по закону Гесса или через его следствия. Для расчета используем следствие из закона Гесса:
![]()
Где νi и ∆Н˚f – стехиометрические коэффициенты и теплоты образования исходных веществ и продуктов реакции. Находим термодинамические характеристики участников реакции при температуре Т = 298 К и сводим их в таблицу.
Эти данные позволяют рассчитать энтальпию реакции при температуре 298 К по уравнению
∆Н˚298 = 3·(-394) + 3·(-242) – (-216) = -1450 кДж/моль
Если бы данную реакцию проводили в реакторе постоянного объема, то тепловой эффект составил
∆U˚298 = ∆H˚298 - ∆ν·R·T = -1450 -1·8,314·10-3·298 = -1452,5 кДж/моль
В данном случае реакция проводится при нормальном давлении (Р =101 кПа) и при заданной температуре t =350˚C или Т =623 К. Чтобы пересчитать тепловой эффект ∆H˚298 к реальным условиям, воспользуемся уравнением Кирхгофа:
∆Н˚Т = ∆Н˚298 + ∆Ср (Т - 298),
Где ∆Ср –изменение теплоемкости в ходе реакции
![]()
Средние теплоемкости веществ для Т = 623 К находим методом линейной интерполяции из справочных данных и заносим в таблицу. Например, для ацетона:
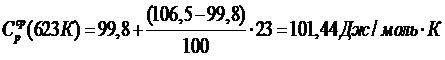
Таблица: Термодинамические характеристики изучаемой реакции
Вещество | ν1 | ∆Н˚f298 кДж/моль | ∆S˚298Дж/моль· К | Срср Дж/моль· К |
С3Н6О О2 СО2 Н2О | 1 4 3 3 | -216 0 -394 -242 | 295 205 214 189 | 101,44 31 43,46 35,23 |
∆Н˚298 кДж/моль -1450 | 94 | 10,64 | ||
∆Н˚Т кДж/моль -1446,5 | ||||
∆S˚298Дж/моль· К | ||||
∆S˚ТДж/моль· К 101,85 | ||||
Срср Дж/моль· К | ||||
∆G˚298 кДж/моль -1478 | ||||
∆G˚T кДж/моль -1510 | ||||
Kр (Т) 10126 |
Так же вычисляем Срср (623 К) для остальных участников реакции.
∆Срср = 3·43,46 +3· 35,23 –(101,43 + 4·31) = 10,64 Дж/моль· К
∆Н˚623 = -1450 +10,64 ·10-3· (623-298) = -1446,5 кДж/моль.
Как видно, температурная поправка в данном случае невелика, и сделанное допущение ∆Ср = const правомочно. Полученные данные заносим в таблицу.
Энтропия реакции сгорания ацетона
Чтобы проектируемый процесс протекал в заданном направлении при обоснованно выбранных условиях (P, V, T), он должен быть самопроизвольным.
Критерием оценки работоспособности процесса при постоянных Т и Р является (∆G)Р, Т< 0. Для его вычисления, необходимо рассчитать изменение энтропии системы.
Для участников реакции переносим справочные данные по абсолютной энтропии. Энтропия является функцией состояния, следовательно, ее изменение в ходе химического процесса подчиняется закону Гесса
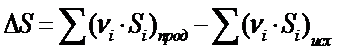
∆S˚298 = 3·214 + 3·189 – (295 + 4·205) = 642 + 567 – 1115= 94 кДж/моль · К
Для перехода к технологической температуре Т =623 К воспользуемся уравнением типа Кирхгофа (в приближении ∆Ср = const):
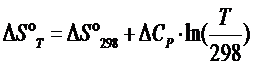
Подставляем в последнее уравнение данные из таблицы
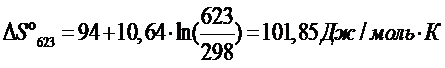
Химическое сродство
При постоянных Т и Р химическое сродство выражается отрицательным значением энергии Гиббса в химическом процессе
(∆G)Р, Т< 0.
Справочные данные (Т =298 К, Р =101кПа) позволяют оценить стандартное химическое сродство по уравнению Гиббса-Гельмгольца:
∆G˚298 =∆H˚298 - 298·∆S˚298
Для изучаемой реакции эти данные приведены в таблице
∆G˚298 = -1450·103 - 298·94 = -1478кДж
Энергия Гиббса зависит от температуры и давления
dG = - SdT + VdP
∆G˚623 = -1446,5 - 623·101,85·10-3 = -1510 кДж
Таким образом, ∆G˚623<< 0, т. е. химическое сродство велико, и проектируемый процесс протекает в необходимом направлении.
Состав паровоздушной смеси в зоне реакции
Окисление вредной примеси происходит в воздухе. При этом в воздухе содержатся компоненты этой реакции в следующих примерных объемных или мольных (yi) долях:
Кислород – 20,8%;
Углекислый газ – 0,03%;
Водяной пар – 2%;
Перейдем к мольно-объемной концентрации, используя закон Дальтона и уравнение Менделеева-Клапейрона:
Pi = П · yi;
Pi = сiRT
ci = (П/RT)·yi
Тогда при атмосферном давлении П = 101,3 кПа и Т = 623 К
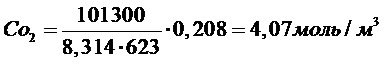
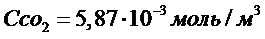

В ходе реакции окисления состав воздуха будет изменяться, так как кислород расходуется на окисление, а количество углекислого газа и воды возрастает за счет продуктов реакции. Рассчитаем состав реальной газовой фазы при протекании реакции окисления ацетона:
1моль
4моль
3моль
3моль
 С3Н6О 4О2 3СО2 3Н2О
С3Н6О 4О2 3СО2 3Н2О
0,019моль 0,076моль 0,057моль 0,057моль
Стехиометрические количества компонентов в 1м3 газа приведены под соответствующими компонентами, исходя из концентрации паров ацетона при температуре окисления:
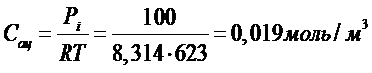
Тогда расход кислорода на окисление составит 0,019·4 =0,076 моль/м3; в результате окисления ацетона выделится:
СО2 0,019·3 = 0,057 моль
Н2О 0,057 моль
В результате концентрации в зоне реакции составят:
Компонент | О2 | СО2 | Н2О |
Концентрация в воздухе, моль/м3 | 4,07 | 0,00587 | 0,39 |
Изменение концентрации в воздухе, моль/м3 | -0,076 | +0,057 | +0,057 |
Концентрация в зоне реакции: моль/м3 | 3,99 | 0,0629 | 0,447 |
Pi =CiRT, Па | 20667 | 325,8 | 2315,3 |
2) Константа равновесия реакции окисления ацетона
Условием равновесного химического процесса является
(∆G)Р, Т = 0.
Из этого уравнения, используя понятие химического потенциала компонентов газовой фазы
μi = μi˚ + RT · ln Pi
для химической реакции следует выражение для константы равновесия
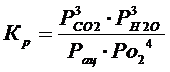
Константа равновесия является важнейшей технологической величиной, так как позволяет определить равновесную концентрацию ацетона в реальных условиях (Т и концентрации компонентов в воздухе) процесса.
Рассчитать константу равновесия позволяет следствие из уравнения изотермы химической реакции
∆G˚T = - RT · lnKP
Величина ∆G˚T была рассчитана выше и приведена в таблице, тогда
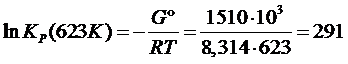
lnKP(623K) = 2,303 lgKP = 291
lnKP =126
KP =10126
Такая большая величина KP говорит о том, что равновесие в реакции окисления ацетона полностью сдвинуто в сторону продуктов реакции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



