Метод хемосорбции основан на поглощении газов и паров твёрдыми или жидкими поглотителями с образованием мало летучих или малорастворимых химических соединений. Обычно это экзотермические процессы и обратимые, поэтому при > t° раствора образующееся химические соединения разлагается с выделением исходных элементов. Примером служит очистка газов от H2S с применением мышьяковощелочного, этаноламинового и др. растворов, очистка газов от оксидов азота с помощью известкового раствора. Эти методы называются мокрыми.
Абсорбционные методы очистки отходящих газов подразделяют по следующим признакам:
- по абсорбируемому компоненту по типу применяемого абсорбента по характеру процесса – с циркуляцией и без циркуляции газа по использованию абсорбента - регенерацией и возвращением его в цикл( циклические) и без регенерации( не циклические ) по использованию улавливаемых компонентов с рекуперацией и без рекуперации по типу рекуперируемого продукта по организации процесса – периодические и непрерывные по конструктивным типам абсорбционной аппаратуры
Выбор метода очистки зависит от многих факторов: концентрации, объёма и t° газа, примесей и т. д.
Адсорбционные методы очистки газов используют для удаления из них газообразных и парообразных примесей в адсорберах.
Достоинство метода – это высокая степень очистки, а недостаток – невозможность очистки запылённых газов.
В качестве адсорбентов или поглотителей применяют вещества, имеющие большую площадь поверхности на единицу массы. Например, поверхность активированных углей 105 -106 м2/кг. Их применяют для очистки газов от органических паров, удаления неприятных запахов и газообразных примесей, содержащихся в промышленных выбросах. В качестве адсорбентов используются глинозём, силикагель, Al2O3, синтетические цеолиты или молекулярные сита.
Адсорбцию широко используют при удалении паров растворителя из отработанного воздуха при окраске автомобилей органических смол и паров растворителей, при производстве стеклотканей, а также паров эфира, ацетона и др. растворителей, в производстве нитроцеллюлозы и бездымного пороха, для очистки выхлопных газов автомобилей; для удаления ядовитых компонентов (H2S); для удаления радиоактивных газов и т. д.
2.2. Характеристика системы и её параметры:

 Газовоздушный Рац = Рраб = 1240 Па T= 298 К раствор ацетона V0 = 73 см3/моль
Газовоздушный Рац = Рраб = 1240 Па T= 298 К раствор ацетона V0 = 73 см3/моль
Ацетон (ж) в W0 = 0,44 см3/г
адсорбенте E0 = 21,5 кДж/моль
P0298 = 259 Торр = 34530 Па
Реальные не идеальные системы удовлетворительно описываются термическим уравнением теории объемного заполнения микропор (ТОЗМ)
![]()
Где а – величина адсорбции, моль/г; W0 – параметр адсорбента – объем микропор, см3/г; V0 – мольный объем адсорбата, см3/моль; Е0 – параметр адсорбента – характеристическая энергия адсорбции бензола; β – коэффициент подобия; α – термический коэффициент адсорбции, К-1 ; Т – температура адсорбции; Т0 = 298 К и
![]()
-изменение химического потенциала сорбтива при адсорбции.
Пусть очистку ГВВ от паров ацетона производят в адсорбере, заполненном микропористым (радиус пор равен 13/Е0 = 13/21,5 = 0,6 нм) активным углем СКТ. Рабочее давление ацетона Рраб = 1240 Па, давление насыщенного пара Р0 = Р0298 = 259 Торр = 34530 Па. Тогда изменение химического потенциала при адсорбции будет равно:
![]()
Коэффициент подобия равен отношению парахоров ацетона и бензола:
![]()
Парахор бензола равен П0 = 205,4. Для ацетона парахор рассчитываем как сумму парахоров атомов С3Н6О:
![]()
Тогда β =140/205,4 = 0,68.
Термический коэффициент сорбции вычисляем по уравнениям:
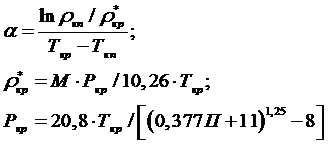
Где ρкп, ρкр* - плотность ацетона при температурах кипения (Ткп) и критической (Ткр).
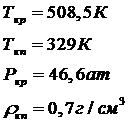
![]()
![]()
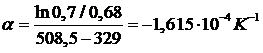
Рассчитываем величину адсорбции (согласно термическому уравнению ТОМЗ) при рабочем давлении и Т = 298 К.
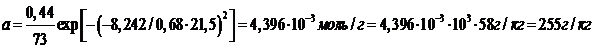
Адсорберы обычно располагают на открытом воздухе или в неотапливаемых помещениях, а величина адсорбции существенно зависит от температуры, что учитывает термическое уравнение ТОМЗ через термический коэффициент адсорбции α. Вычислим величину адсорбции для максимальной (t˚= 35˚C) и минимальной (t˚= -15˚C) температур. Однако давление насыщенного пара Р0 также зависит от температуры. Для его расчета воспользуемся следствием из уравнения Клаузиса-Клапейрона:
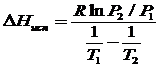
Рассчитав ∆Нисп можно вычислить давление насыщенного пара при любой температуре (при допущении, что ∆Нисп не зависит от температуры):
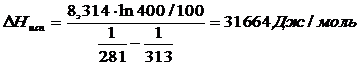
Вычисляем Р0Т через Р0298 = 34530 Па, и изменение химического потенциала:
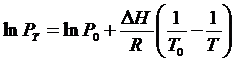
При минимальной температуре: Т = -15 +273 = 258 К
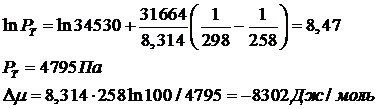
При максимальной температуре: Т = 35 +273 = 308 К
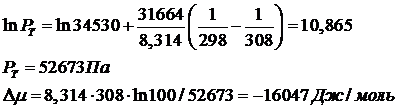
Теперь можно рассчитать величину адсорбции
-при минимальной температуре:
![]()
-при максимальной температуре:
![]()
После улавливания паров ацетона активным углем адсорбат удаляют из угля нагреванием с помощью водяного пара, последний выходит из адсорбера в смеси с парами ацетона и конденсируется. Обычно расход водяного пара составляет 2-5 кг на кг адсорбата. Концентрацию полученного раствора ацетона в воде можно увеличить методом ректификации.
3.1. Метод ректификации
По табличным данным построим зависимость температуры кипения раствора С2Н4О2 в воде от состава раствора (нижняя кривая) и пара (верхняя кривая). Состав выражен в мольных долях С2Н4О2. Концентрация раствора, который поступает на ректификацию, равна хн = 0,10 = 10% мольн. По первому закону Коновалова, на монотонных участках равновесной кривой концентрации жидкой и паровой фаз различаются. Начальный раствор закипает при температуре (точка D ), при этом образуется пар (точка Е) с концентрацией. Это является теоретической основой разделения раствора, так как если сконденсировать полученный пар, то образуется раствор с концентрацией много большей, чем концентрация исходного раствора.
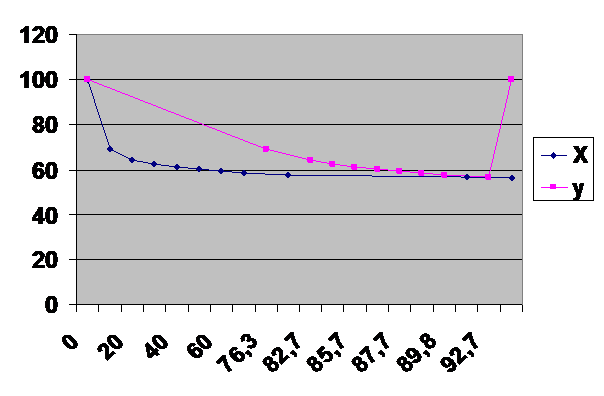 По второму закону Коновалова, в экстремальных условиях равновесной кривой концентрации паровой и жидкой фаз совпадают. Это азеотропная точка А, координаты которой. В этой точке процесс разделения должен прекратиться, так как образуется «однокомпонентный» нераздельно кипящий раствор (число независимых компонентов равно числу индивидуальных химических веществ) за вычетом уравнений связи концентраций). Следовательно, теоретически данный раствор может быть разделен только на чистую воду и азеотропный раствор.
По второму закону Коновалова, в экстремальных условиях равновесной кривой концентрации паровой и жидкой фаз совпадают. Это азеотропная точка А, координаты которой. В этой точке процесс разделения должен прекратиться, так как образуется «однокомпонентный» нераздельно кипящий раствор (число независимых компонентов равно числу индивидуальных химических веществ) за вычетом уравнений связи концентраций). Следовательно, теоретически данный раствор может быть разделен только на чистую воду и азеотропный раствор.
Исходный раствор при кипении дает пар состава (точка Е), обогащенный С2Н4О2 . При этом раствор обедняется С2Н4О2 и температура его кипения повышается по кривой DlC и последняя его порция будет иметь концентрацию в точке С – хс. Пар состава может быть сконденсирован и повторно испарен, на диаграмме это точка в, концентрация в которой после кондкенсации паров составит. Повторное же испарение раствора с концентрацией хс (точки d и e) даст практически чистую воду с содержанием С2Н4О2.
Таким образом, равновесный процесс разделения раствора с хн = 0,10 содержит четыре теоретических ступени разделения (теоретические тарелки; ЧТТ = 4) при получении дистиллята с заданной концентрацией и кубового остатка.
Например, на разделение поступает раствора. Так как все концентрации выражены в мольных долях, целесообразно массу раствора выразить в молях, для этого рассчитываем среднюю молекулярную массу исходного раствора
Схема материальных потоков:
Тогда, общий баланс:
Баланс по С2Н4О2:
Решая систему уравнений, получаем:
Если на первую тарелку поступает начальный раствор в количестве при температуре (точка М), то он будет выкипать до концентрации и образуется пар с концентрацией (точки l и m).
Схема материального баланса:
Из этого следует:
Решая систему уравнений, получаем:
4.1. БИОХИМИЧЕСКАЯ ОЧИСТКА СТОЧНЫХ ВОД — (биологическая очистка) — основной способ очистки сточных вод, содержащих загрязнения органического происхождения, заключающийся в минерализации этих загрязнений вследствие жизнедеятельности микроорганизмов. В процессе дыхания микробов органические вещества окисляются и освобождается энергии, необходимая для жизненных функций.
Часть энергии идет на процесс синтеза клеточного вещества, т. е. на увеличение массы бактерий, количества активного ила и биологической пленки в очистных сооружениях.
В минерализации органических соединений сточных вод участвуют бактерии, которые по своему отношению к кислороду разбиваются на 2 группы: аэробные (использующие при дыхании растворенный в воде кислород) в анаэробные (развивающиеся в отсутствии свободного кислорода).
Необходимыми условиями для жизнедеятельности организмов, способствующих очистке, и эффективного использования аэробных очистных сооружений являются:
наличие в сточных водах органических веществ, способных окисляться биохимически; непрерывное снабжение сооружений кислородом в достаточном количестве; активная реакция очищаемой воды (в пределах 7—8,5 рН); температура воды не ниже 10° и не выше 30°; наличие биогенных элементов — азота, фосфора, калия в необходимых количествах; содержание минеральных солей и воде не выше 10 г/л; отсутствие токсических веществ в концентрациях, ядовито действующих на микроорганизмы.
Биохимическая очистка сточных вод протекает в две одновременно начинающиеся фазы: сорбция поверхностью тел бактерий растворенных органических веществ и коллоидов; окисление и минерализация растворенных и адсорбированных органических веществ микробами.
Для биохимической очистки бытовых в промышленных сточных вод применяются следующие очистные сооружения: аэробные — биологические пруды, поля орошения, поля фильтрации (см. Поля орошения и фильтрации), биофильтры, аэрофильтры и аэротенки; анаэробные — септики, двухъярусные отстойники, метантенки. Выбор типа сооружений определяется характером и количеством сточных вод, местными условиями, требованиями к качеству очищенной воды, наличием свободных земельных площадей и т. д.
Перед биохимической очисткой из сточных вод необходимо удалить взвешенные вещества, смолы и масла. В результате очистки содержание органических веществ в сточных водах снижается на 90—95%; они теряют способность к загниванию, становятся прозрачными, количество бактерий в них сильно снижается.
Биохимическая очистка фекально-хозяйственных сточных вод достаточно хорошо изучена, разработаны методы расчета очистных сооружений. При очистке производственных сточных вод, ввиду их большого разнообразия, расчетные параметры очистных сооружений устанавливаются на основании результатов лабораторных опытов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



