3) Определим равновесное давление ацетона при реальных парциальных давлениях компонентов реакции. Для этого необходимо перейти от Па к атм (1атм = 101300 Па), так как величина энергии Гиббса измерена при стандартном давлении 1 атм. Тогда:
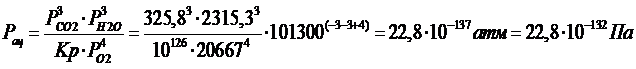
Сац = Рац · RT = 22,8 · 10-132 · 8,314 · 623 = 1,2 · 10-127 моль/м3
Эта концентрация значительно ниже ПДК и, таким образом, метод каталитического дожигания в равновесных условиях позволяет практически полностью очистить воздух от паров ацетона.
4) Кинетика каталитической реакции окисления паров ацетона
Реальные процессы протекают в условиях, далеких от равновесия с определенной конечной скоростью и при повышенных температурах.
Скорость протекания реакции можно выразить с помощью кинетического уравнения:
ω = k1 · Cn1ац Сn2О2
где k1 –константа скорости, которая не зависит от концентрации реагентов и растет с увеличением температуры; n1 и n2 –частные порядки реакции по ацетону и кислороду.
В данном случае реакция протекает при большом избытке кислорода, поэтому можно принять СО2 = const, тогда
ω = k1 · Cn1ац = k1 · Сn2О2
где k = k1 · Сn2О2 ; С – концентрация ацетона; n –порядок реакции.
Окисление ацетона ведем на твердом катализаторе. Процесс- гетерогенный и может проходить в кинетической и диффузионной области. Для определения порядка реакции и константы скорости такого сложного процесса необходимы экспериментальные данные, например, изменение концентрации ацетона во времени и константы скорости при двух температурах.
Кинетика каталитического окисления ацетона при температуре 490˚С
K(530˚С)/k(490˚С) = 2,1
τ, с | 0 | 1 | 5 | 10 | 15 | 20 | 40 | 60 |
С, моль/м3 | 10 | 1,94 | 0,738 | 0,481 | 0,374 | 0,313 | 0,203 | 0,158 |
lnC | 2,3 | 0,66 | -0,3 | -0,73 | -0,98 | -1,16 | -1,59 | -1,85 |
1/C | 0,1 | 0,52 | 1,36 | 2,08 | 2,67 | 3,19 | 4,93 | 6,33 |
Изменение константы скорости реакции при увеличении температуры
t1, ˚С | t2, ˚С | К2/К1 |
490 | 530 | 2,1 |
Целочисленный порядок реакции удобно определить графическим методом. Для этого интегрируем кинетическое уравнение при n = 0; 1 и 2 (пределы интегрирования 0- τ и С0 -С)
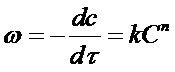
n = 0; - dc/dτ; С = С0 – kτ;
n = 1; - dc/dτ = kC; lnС = lnС0 – kτ;
n = 2; - dc/dτ = kC2; 1/С = 1/С0 – kτ;
Таким образом, имеем линейные уравнения при y =С; lnC или 1/С; х = τ. Если реакция протекает, например, по первому порядку, то экспериментальные данные должны дать линейный график в координатах lnC = f(τ), в других координатах получится криволинейная зависимость. Для этого дополняем таблицу строками lnC и 1/С и строим кинетические кривые в функциональных координатах уравнений.
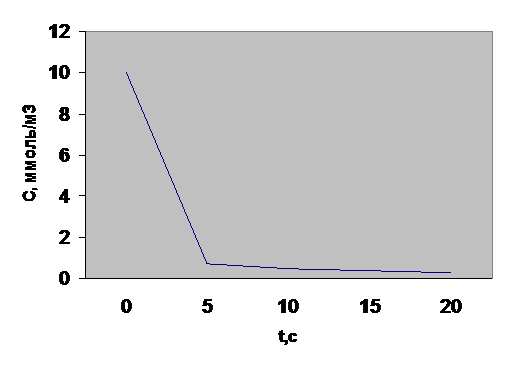
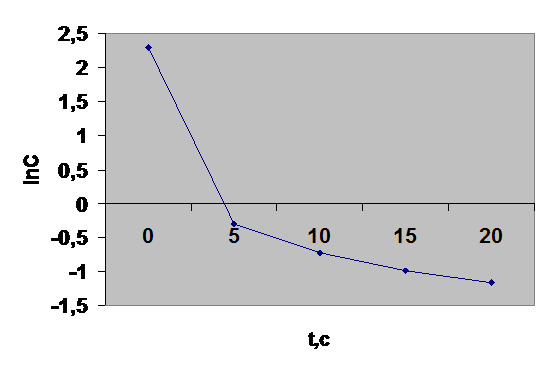
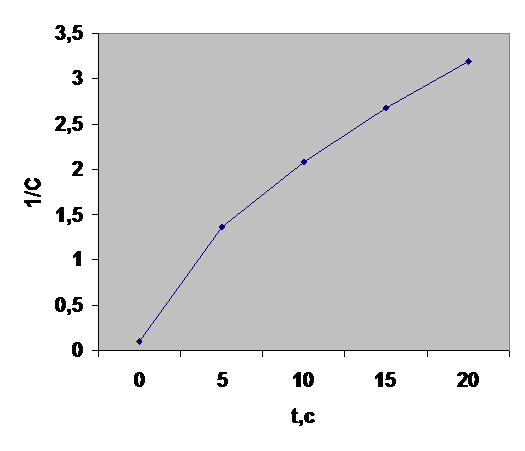
Как видно, экспериментальные данные не подчиняются кинетическим уравнениям 0-, 1- и 2-го порядков. Вероятно, в данном случае порядок имеет дробную величину. В связи с этим применим дифференциальный метод анализа, который заключается в том, что при логарифмировании уравнения ω = k1 · Cn1ац = k1 · Сn2О2
lnw = lnk + nlnC
получается линейная зависимость lnw от lnC, а угловой коэффициент при этом равен n и отрезок отсекаемый на оси lnw равен lnk.
Скорость реакции вычисляем графическим дифференцированием кинетической кривой. Для этого разбиваем ось времени на одинаковые участки по ∆τ = 5 с и измеряем ∆С на каждом участке. Тогда заменяя криволинейную зависимость на каждом участке на линейную, получаем значения средней скорости реакции в пределах выбранных концентраций
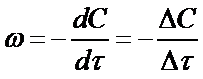
Данные сводим в таблицу.
Определение порядка и константы скорости реакции окисления ацетона
τ, с | 0 | 5 | 10 | 15 | 20 |
С, моль/м3 | 10 | 0,738 | 0,481 | 0,374 | 0,313 |
∆С, моль/м3 | - | 9,262 | 0,257 | 0,107 | 0,061 |
W=(∆С/ ∆τ)·102 | 185,24 | 5,04 | 2,14 | 1,22 | |
СCp, моль/м3 | 5,369 | 0,6095 | 0,4275 | 0,3435 | |
lnw | 5,22 | 1,62 | 0,76 | 0,199 | |
ln СCp | 1,68 | -0,495 | -0,85 | -1,614 | |
k·103 | |||||
Затем рассчитываем на каждом участке ССр = (Ci+1 - Ci)/2 и строим зависимость lnw = f (lnCСр). Наилучшим способом проводим прямую линию, отвечающую уравнению lnw = lnk + nlnC. Кинетический порядок реакции равен тангенсу угла наклона прямой.
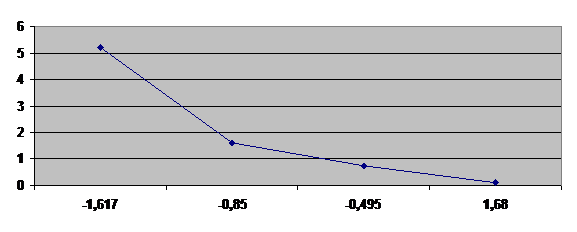
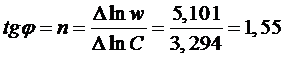
Среднюю константу скорости реакции определяем, экстраполируя кривую к lnC = 0
lnk = 0,6
k = 1,81
Таким образом, кинетическое уравнение в данном случае можно записать:
![]()
Или после интегрирования этого уравнения получаем:
Из последнего уравнения рассчитываем константу скорости для заданных концентраций и времен k = и результаты вносим в таблицу. Средняя константа скорости равна
Что практически совпадает с измеренной графическим методом. Температурную зависимость скорости реакции передает уравнение Аррениуса:
![]()
Где k0 – предэкспоненциальный множитель; Е – энергия активации.
Экспериментальные данные позволяют рассчитать эти константы. Для этого логарифмируем и записываем уравнение Аррениуса для двух заданных температур:
![]()
Вычитаем первое уравнение из второго и вычисляем энергию активации
Рассчитываем предэкспоненциальный множитель
Большая величина Е показывает, что реакция протекает в кинетической области, т. к. для диффузионной области энергия активации не превышает 20 кДж/моль.
Энергия активации и предэкспонента в теории абсолютных скоростей реакции связаны с энтропией и энтальпией переходного состояния
Тогда энергия Гиббса образования переходного состояния равна
Таким образом, выполненные действия позволяют проводить расчет скорости процесса на выбранном катализаторе при заданных исходных концентрациях компонента и температурах, так как порядок реакции, энтропия переходного состояния и энергия активации не зависят от концентрации и температуры:
Задание 3.3 Адсорбционная очистка вентиляционных газов от вещества А (ацетона) и выделение его в чистом виде методом ректификации
1. См. разд. 3.1.
2. Вентиляционные газы очищаются от вещества А методом адсорбции при температуре 25˚ с использованием активного угля СКТ. Максимальная температура адсорбера t2 =35˚C, минимальная t1 =-15˚C. Адсорбция- экзотермический процесс, поэтому, чтобы снизить температуру в адсорбере вентиляционные газы разбавляют воздухом в 2 раза.
2.1. Дать характеристику адсорбционного метода очистки газов
2.2. Рассчитать процесс адсорбции.
3. Десорбция вещества А (С2Н4О2) водяным паром позволила получить раствор с концентрацией хн = 0,10 в количестве Gн= 1000 кг. Методом ректификации при давлении Р получены дистиллят и кубовый остаток с концентрациями хД =0,005 и хК = 0,95 соответственно.
3.1. Дать характеристику метода ректификации.
3.2. Рассчитать процесс ректификации.
4. Низкоконцентрированный раствор разбавляется другими сточными водами в 10 раз и направляется на биологическую очистку.
4.1. Дать характеристику биохимической очистке сточных вод.
4.2. Рассчитать кинетику процесса (принять порядок реакции n=1)
4.3. Дать прогноз изменения времени процесса при колебаниях температуры ±5˚ С и увеличении концентрации сточных вод в 10 раз.
К1, ч-1 | 0,13 |
K2/K1 | 3,0 |
t1,˚C | 20 |
t2,˚C | 30 |
2.1. Адсорбционный метод очистки газов
Абсорбционный метод – скрубберный метод, заключается в разделении газовоздушной смеси на составные части путём поглощения одного или нескольких газовых компонентов (абсорбатов) этой смеси жидким поглотителем ( абсорбентом ) с образованием раствора. Решающим условием при выборе абсорбента является растворимость в нём извлекаемого компонента и её зависимость от t° и p. Хорошо растворимыми называются газы, которые при 0 °С, 101,3 кПа растворяются в количество сотни граммов на 1кг растворителя. Таким образом, удаляют NH3, HF, HCl используя в качестве поглотителя просто воду.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



