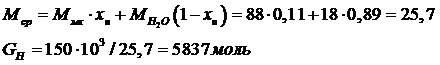
Общий материальный баланс:
![]()
Баланс по МК:
![]()
Тогда:
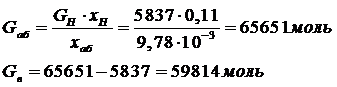
Задание 3.6. Разделение растворов электролитов
1. Выделить из разбавленного раствора кристаллы вещества А (AgNO3), если количество раствора Ga = 400 кг, начальная концентрация равна ma = 5 (г/1000г Н2О), температура вымораживания растворителя ta = -3˚C, концентрация раствора, подаваемого на кристаллизацию при температуре tкр = 10˚C, равна mв = 7000 .
1.1. Дать характеристики процессов вымораживания, выпаривания растворителей и кристаллизации растворенного вещества, рассчитать материальные потоки.
Изобразить на диаграмме состояния процессы, перечисленные в п. 1.1.
2. Как изменится процесс разделения, если произвести начальное концентрирование раствора методом обратного осмоса при давлении π =100 атм.
2.1. Дать характеристику мембранных процессов.
2.2. Рассчитать процесс обратноосмотического концентрирования раствора.
Решение:
Рассмотрим, как можно выделить нитрат серебра из разбавленного раствора с концентрацией ma = 5 (г/1000г Н2О), находящегося при начальной температуре tкр = 10˚C. Строим фазовую диаграмму состояния системы AgNO3 – H2O.
m | 132 | 500 | 897 | 1220 | 2000 | 4000 | 6000 | 8000 | 9500 |
tкрист | -2 | -3,5 | -7,19 | 0 | 15 | 53 | 80 | 103 | 115 |
tкип | 101 | 102 | 103 | 103,5 | (105) | (108) | (111) | (114) | (115) |
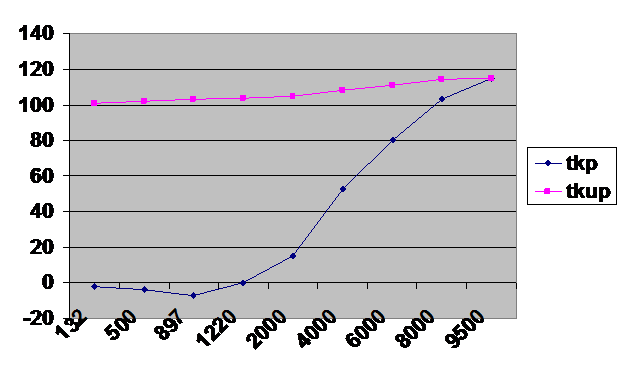 Концентрирование исходного раствора методом вымораживания растворителя.
Концентрирование исходного раствора методом вымораживания растворителя.
Сточные воды в большинстве своем имеют очень низкую концентрацию. Поэтому, если ставить цель выделить из них ценный или вредный компонент, то первой операцией должно быть концентрирование раствора. Это может быть достигнуто тремя путями: обратным осмосом, выпаркой и вымораживанием растворителя. Последний упомянутый метод связан с тем, что при концентрациях ниже эвтектической при охлаждении раствора из него кристаллизуется только растворитель, а концентрация раствора повышается вдоль линии ликвидуса. Метод вымораживания растворителя в отечественной технологии кристаллизации применяется редко, вероятно из-за низкого уровня развития холодильной техники.
Если в отстойнике сточные воды имеют ПДК или близкую к ним концентрацию, то замерзание отстойника в зимнее время ведет к вымораживанию растворителя и возможному повышению ПДК в десятки раз.
Охладим исходный разбавленный раствор (точка а), тогда в точке в начнут выделяться кристаллы воды. Температуру начала кристаллизации воды определяем по криоскопической формуле:
![]()
Для этого вычисляем входящие в неё величины. Нитрат серебра – сильный электролит:
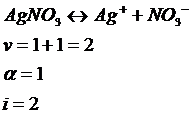
Молярность раствора:
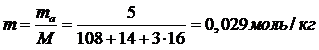
Криоскопическая константа для воды
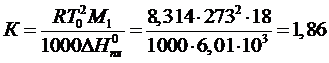
Где Т0 = 273 К – температура кристаллизации воды; М1 – молекулярная масса воды; ∆Н0пл – энтальпия плавления льда, Дж/моль.
Таким образом,
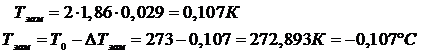
При дальнейшем охлаждении раствора до заданной температуры ta = -3˚С из него будут выделятся кристаллы воды (лед), а концентрация раствора будет увеличиваться по линии ликвидуса bdE и в точке d достигнет md = 377 г/кг = 377/170 = 2,2 моль/кг.
Пусть на концентрирование поступает Ga= 400 кг раствора AgNO3, переводим рабочие концентрации в массовые доли г/кг раствора:
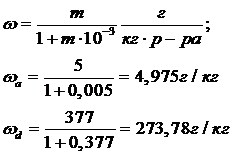
Тогда схема материальных потоков будет:

Исходный
раствор
Ga=400 кг
ωа = 4,975 г/кг
 |  |


Лед Конц. раствор
Gл, ωл = 0. Gd, ωd = 273,78 г/кг
Общий материальный баланс:
![]()
Материальный баланс по AgNO3
![]()
Тогда
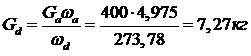
![]()
Таким образом, методом вымораживания растворителя масса сточных вод снизилась с 400 кг до 7 кг, а концентрация их повысилась в 298,78/4,975= 60 раз.
Концентрирование исходного раствора методом обратного осмоса
Рассмотренный тепло-массообменный процесс концентрирования разбавленного раствора требует затраты большого количества энергии, более экономичными являются мембранные процессы. Осмотическое давление разбавленного раствора AgNO3 можно вычислить по формуле:
![]()
При этом концентрация (С) должна быть отнесена к 1 м3 раствора. Принимая плотность раствора равной плотности воды, получаем:
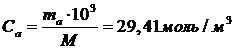
Тогда при температуре Т = 283К
![]()
Осмотическое давление концентрированного раствора (md=377г/кг) нельзя рассчитать по такому уравнению, так как введенные упрощения при его выводе корректны только для бесконечно разбавленного раствора. Для раствора любой концентрации в приближении идеального раствора:
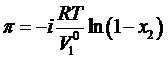
Где V01 = 18·10-6 м3/моль – мольный объем воды; x2 – мольная доля AgNO3 в растворе
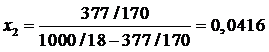
Тогда:
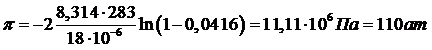
Схему материальных потоков при обратноосмотическом разделении раствора можно представить в следующем виде:

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()


 Ga, ωa Gd, ωd Концентрат
Ga, ωa Gd, ωd Концентрат
 Мембрана
Мембрана
Исходный
раствор
Вода Gл, ωл
Концентрирование раствора AgNO3 методом испарения растворителя (выпаривание)
Полученный после вымораживания или мембранного разделения раствор в количестве Gd = 7,27 кг с концентрацией md =377 г/кг направим на выпаривание. Для этого по линии нагреваем раствор до температуры кипения te. Приближенно эту температуру можно вычислить по эбулоскопической формуле.
Эбулоскопическая константа равна:
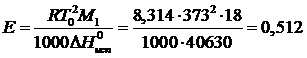
Где ∆Н0исп = 40630 Дж/моль – энтальпия испарения воды при температуре кипения Т0 = 373 К
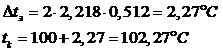
Эта температура несколько ниже экспериментальной величины tв = 101,33˚С, приведенной на графике.
При выпаривании концентрация раствора и температура кипения возрастают по линии еf. В точке f температура кипения составляет 12,5˚ и концентрация раствора достигает заданной величины mf = 7000 г/кг растворителя.
Составляем схему материальных потоков и рассчитываем количества концентрированного раствора Gf и пара:

Исходный раствор
Gd = 7,27 кг
ωd = 273 г/кг
 |  |


Пар Концентрат
W, ωn = 0 Gf; ωf = 0,875
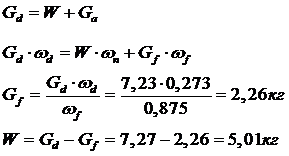
Кристаллизация AgNO3 из концентрированного раствор
Полученный после выпаривания концентрированный раствор AgNO3 в количестве Gf=2,26 кг с концентрацией ωf = 0,875 (mf = 7000 г/кг Н2О) при охлаждении становится насыщенным. Дальнейшее его охлаждение по линии hg сопровождается кристаллизацией AgNO3, а концентрация раствора соответственно понижается по линии ликвидуса hlE. Если кристаллизацию проводить при температуре tg = 10˚C то конечную концентрацию маточного насыщенного раствора найдем на пересечении изотермы (10˚C) и линии ликвидуса: ml = 1740 г/кг
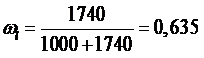
Составим схему материальных потоков и вычислим количества выделенных кристаллов AgNO3 и маточного раствора

Концентрат
Gf=2,26 кг
ωf = 0,875


Кристаллы Маточный раствор
Gкр, ωкр = 1 Gl, ωl = 0,635
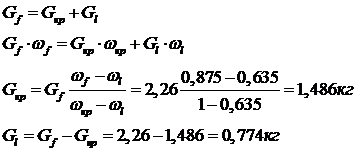
Маточный раствор можно добавить к раствору, полученному после вымораживания и направить на выпаривание. Тогда на выпаривание будет направлено G кг раствора с концентрацией ω.


Gd = 7,27 кг Gl= 0,774 кг
![]()
 ωd = 0,273 ωl = 0,635
ωd = 0,273 ωl = 0,635

G = 7,81кг
ω = 0,287
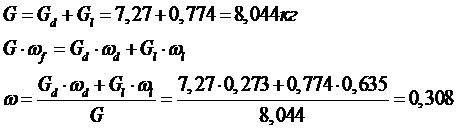
Таким образом, в результате проведенных операций из исходного раствора Ga = 400кг (ωа = 4,975) получен чистый растворитель в виде льда Gл =392,73 кг и пара W = 5,01 кг и кристаллы AgNO3 Gкр =7,27 кг.
В последнем процессе при кристаллизации AgNO3 необходимо отводить теплоту кристаллизации. Мольную теплоту кристаллизации можно определить по приближенному уравнению
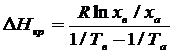
Где ха, хв - концентрации (мольные доли) насыщенного раствора при температурах Та и Тв. Для AgNO3 находим параметры насыщенных растворов при температурах, близких к выбранной температуре кристаллизации: ma = 2000 г/кг, ta =15˚С; mв = 1220 г/кг, tв =0˚С.
Переводим концентрации mi раствора в мольные доли:
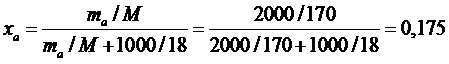
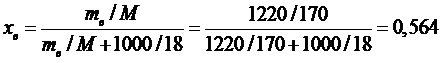
И подставляем их в уравнение:
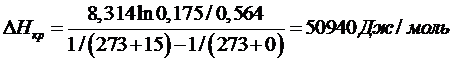

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



