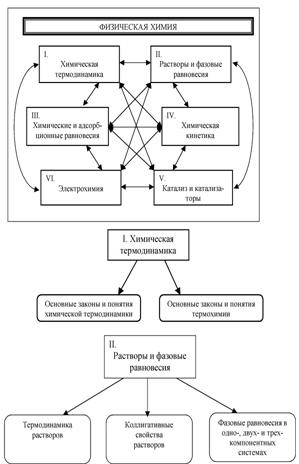
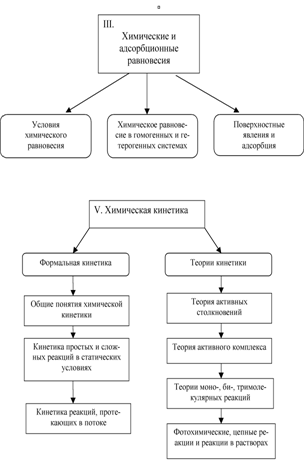
Программа курса построена по блочно-модульному принципу, в ней выделены несколько разделов/тем:
|
|
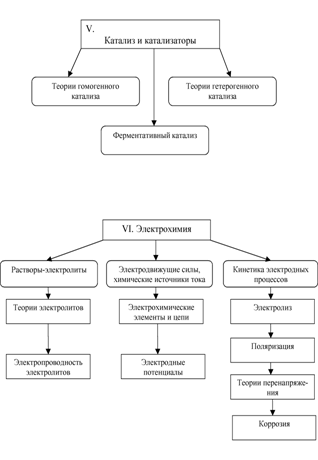
2. КОМПЕТЕНЦИИ ОБУЧАЮЩЕГОСЯ, ФОРМИРУЕМЫЕ
В РЕЗУЛЬТАТЕ ОСВОЕНИЯ ДИСЦИПЛИНЫ
· быть способным и готовым использовать основные законы естественнонаучных дисциплин в профессиональной деятельности, применять методы математического анализа и моделирования, теоретического и экспериментального исследования (ПК-1);
· использовать знания о современной физической картине мира, пространственно-временных закономерностях, строении вещества для понимания окружающего мира и явлений природы (ПК-2);
В результате освоения дисциплины обучающийся должен:
знать:
· об основных проблемах и вопросах, решаемых в данном курсе и применительно к биотехнологии;
· о существующих подходах к рассмотрению вопросов основных разделов физической химии;
· о связи физической химии с другими дисциплинами – биохимией, физиологией, биофизикой.
уметь:
· применять теоретические положения физической химии при рассмотрении различных физико-химических свойств и явлений, для анализа конкретных процессов;
· использовать теоретические знания по физической химии в своей практике;
· раскрывать взаимосвязь между основными разделами физической химии и другими науками;
· анализировать, сопоставлять, систематизировать полученные на лекционных, практических и лабораторных занятиях научные факты;
· выдвигать и обосновывать гипотезы о причинах возникновения того или иного состояния, события, описываемых в физической химии, о возможных путях их развития и последствиях;
владеть:
· умением выбирать методы физической химии при изучении того или иного явления, учитывая все их преимущества и недостатки;
· навыками определения параметров, характеристик физико-химических процессов и систем, используя известные методы, средства, закономерности физической химии;
3. ЦЕЛЬ И ЗАДАЧИ ОСВОЕНИЯ ДИСЦИПЛИНЫ
Целью освоения дисциплины ФИЗИЧЕСКАЯ ХИМИЯ
является:
формирование у студентов фундаментальных теоретических представлений о сущности основных физико-химических процессов. Курс физической химии в подготовке специалистов данного направления служит базой для изучения многих специальных дисциплин: биохимии, биофизики, физиологии и других. В ходе изучения происходит формирование необходимого кругозора по теоретическим и практическим вопросам химии, о ее тесной взаимосвязи с другими областями знаний. Курс не только помогает студенту усвоить предмет физической химии, но и способствует развитию самостоятельных навыков в применении ее законов, то есть формированию физико-химического мышления. Ядро курса составляют основные разделы физической химии – химическая термодинамика и термохимия, термодинамика растворов, химическое и фазовое равновесия, адсорбция, химическая кинетика, катализ, электрохимия. Лабораторные работы, охватывающие основные разделы физической химии, способствуют более глубокому пониманию физико-химических явлений, развивают умение формулировать и анализировать конкретную проблему, принимать самостоятельное решение
Задачи освоения дисциплины:
· сформировать понимание, что физическая химия является одной из фундаментальных дисциплин, лежащих в основе естествознания;
· владеть навыками теоретических методов расчета различных физико-химических процессов;
· овладеть навыками практического использования физико-химических методов исследования в своей деятельности.
4. СТРУКТУРА ДИСЦИПЛИНЫ ПО ВИДАМ УЧЕБНОЙ РАБОТЫ,
СООТНОШЕНИЕ ТЕМ И ФОРМИРУЕМЫХ КОМПЕТЕНЦИЙ
Общая трудоемкость дисциплины составляет 10 зачетных единиц, 180 часов.
№ | Разделы, темы дисциплины | Неделя семестра | Виды учебной работы (в часах) | Формы текущего контроля успеваемости | Формируемые компетенции (код) | Всего компе-тенций | ||
Л. | Лабраб. | Сам. раб. | ||||||
Семестр 2 | ||||||||
1 | Тема 1. Предмет физической химии, основные разделы и методы исследования. Химическая термодинамика, основные определения и понятия - термодинамические системы, термодинамические состояния, параметры, процессы, функции состояния. Термодинамические равновесные системы и процессы. Внутренняя энергия, закон сохранения энергии. Теплота и работы различного рода. Первый закон термодинамики. Энтальпия | 1 | 2 | 6 | 6 | Домашнее задание | ПК-1, ПК-2 | 3 |
2 | Тема 2. Термохимия. Теплоемкости. Тепловой эффект химической реакции. Закон Гесса и его следствия. Зависимость теплового эффекта реакции от температуры, уравнение Кирхгоффа. | 2 | 2 | 6 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
3 | Тема 3. Теоремы и лемма Карно. Различные формулировки второго начала термодинамики. Направление естественных процессов. Энтропия. Изменение энтропии в необратимых процессах, неравенство Клаузиуса. Энтропия и вероятность. | 3 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
4 | Тема 4. Определение абсолютной энтропии. Вычисление изменения энтропии в необратимых процессах, объединенный закон термодинамики. Определение абсолютной энтропии. Вычисление изменения энтропии в необратимых процессах, объединенный закон термодинамики. | 4 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
5 | Тема 5. Характеристические функции. Термодинамические потенциалы – энергия Гиббса, энергия Гельмгольца и их свойства. Уравнения Максвелла. Уравнение Гиббса-Гельмгольца и его роль в химии. | 5 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
6 | Тема 6. Критерии возможности протекания самопроизвольных химических реакций для открытых систем. Химический потенциал. Характеристические функции идеальных и реальных газов. Химический потенциал для идеальных и реальных систем, активность, фугитивность. | 6 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
7 | Тема 7. Растворы различных классов. Различные способы выражения состава растворов, смеси идеальных газов. Термодинамика растворов. Гомогенные системы, идеальные и реальные растворы. | 7 | 2 | 6 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
8 | Тема 8. Общие свойства растворов. Уравнение Гиббса-Дюгема. Давление насыщенного пара жидких растворов. Законы идеальных жидких растворов – закон Генри, закон Рауля. | 8 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
9 | Тема 9. Коллигативные свойства растворов – эбуллиоскопия, криоскопия, осмотические явления. | 9 | 2 | 6 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
10 | Тема 10. Растворимость газообразных и твердых веществ в жидкости. Равновесие жидкость-пар в бинарных системах. Первый закон Коновалова, правило рычага. | 10 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
11 | Тема 11. Растворы с положительными и отрицательными оклонениями от закона Рауля. Второй закон Коновалова, азеотропные смеси и их свойства. Простая, фракционная перегонка. Ректификация. Перегонка азеотропов. | 11 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
12 | Тема 12. Химическое равновесие, условия химического равновесия. Закон действия масс, его кинетический вывод. Закон действия масс для гетерогенных реакций. Принцип Ле-Шателье. Зависимость констант равновесия от температуры, уравнения изотермы, изохоры, изобары химической реакции. | 12 | 2 | 6 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
13 | Тема 13. Фазовые переходы первого рода, уравнение Клайперона-Клаузиуса и его применение к различным фазовым переходам первого рода. Условия самопроизвольного перехода вещества из одной фазы в другую | 13 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
14 | Тема 14. Гетерогенные системы. Гетерогенное фазовое равновесие. Правило фаз Гиббса. | 14 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
15 | Тема 15. Однокомпонентные системы. Диаграмма состояния воды. Диаграмма состояния серы. Двухкомпонентные системы. | 15 | 2 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
16 | Тема 16. Различные диаграммы состояния и их анализ на основе правила фаз Гиббса. | 16 | 2 | 6 | 6 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
17 | Тема 17. Поверхностные явления. Внутреннее давление жидкости. Поверхностное натяжение. Влияние природы вещества, температуры, концентрации на поверхностное натяжение. Понятие о ПАВ и ПИВ. Поверхностная активность. Понятие адсорбции, адсорбента, адсорбата. Силы адсорбционного взаимодействия. Виды адсорбции. | 17 | 2 | 6 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
18 | Тема 18. Изотермы адсорбции – изотермы Генри, Ленгмюра, Фрейндлиха, БЭТ, Гиббса. Адсорбция на границе раздела фаз: твердое тело-газ (Адсорбционная теория Лэнгмюра), жидкость-газ, адсорбция из растворов. | 18 | 2 | 6 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
Семестр 3 | ||||||||
1 | Тема 1. Химическая кинетика, ее основные понятия. Скорость химической реакции. Основной постулат химической кинетики. Понятие порядка, молекулярности. Кинетика необратимых гомогенных реакций 1-го, 2-го,3-го порядков. | 1 | 2 | 6 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
2 | Тема 2. Методы определения порядка. Кинетика сложных реакций. | 2 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
3 | Тема 3. Влияние температуры на скорость химических реакций – правило Вант-Гоффа, уравнение Аррениуса. Основные теории химической кинетики – теория активных столкновений. | 3 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
4 | Тема 4. Теория переходного состояния. Цепные реакции, свободные радикалы. Фотохимические реакции. | 4 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
5 | Тема 5. Катализ. Виды катализа – гомогенный, гетерогенный, ферментативный. Основные свойства катализаторов. Факторы, влияющие на катализ. Теория механизма гомогенного катализа. | 5 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
6 | Тема 6. Общие сведения о кинетике и механизмах ферментативных реакций. | 6 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
7 | Тема 7. Кислотно-основной катализ. | 7 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
8 | Тема 8. Гетерогенный катализ – теория мультиплетов Баландина. | 8 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
9 | Тема 9. Электрохимия, основные понятия. Теория слабых электролитов Аррениуса, ее недостатки. | 9 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
10 | Тема 10. Теории сильных электролитов. Понятие средней активности и среднего коэффициента активности. Ионная сила, закон Дебая-Гюккеля. | 10 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2, ПК-7 | 3 | |
11 | Тема 11. Электропроводность – удельная и эквивалентная. Подвижность ионов. Измерение электропроводности, ее практическое применение. Числа переноса ионов. | 11 | 2 | 4 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
12 | Тема 12. Электрохимические элементы. ЭДС гальванического элемента. Правило знака ЭДС. Уравнение Гиббса - Гельмгольца. Уравнение Нернста для ЭДС. Определение ЭДС. | 12 | 2 | 6 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
13 | Тема 13. Возникновение межфазных скачков на границах раздела фаз. Двойной электрический слой. Электродный потенциал. | 13 | 2 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
14 | Тема 14. Классификация электродов, электроды I, II, рода. Газовые электроды. | 14 | 2 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
15 | Тема 15. Неравновесные электродные процессы. Электролиз. Перенапряжение водорода. | 15 | 2 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
16 | Тема 16. Элементы неравновесной термодинамики. Понятие о стационарном состоянии и методах его анализа и определения. | 16 | 2 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 | |
17 | Тема 17. Элементы кинетики биологических процессов. | 17 | 3 | 6 | 5 | Домашнее задание. Письменный опрос (10 мин.). Решение задач. | ПК-1, ПК-2 | 3 |
18 | Тема 18. Обобщение: место физической химии в окружающем мире и ее роль в биохимических исследованиях. | 18 | 1 | 6 | 5 | ПК-1, ПК-2 | 3 |
5. Содержание дисциплины

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |