Карбоновую кислоту называют так, как назвали бы соответствующий углеводород, добавить суффикс - ов, окончание - ая и слово кислота.
Гомологический ряд начинает кислота, в которой (подобно альдегидам), функциональная группа связана не с углеводородным радикалом, а с атомом водорода. Это метановая кислота НСООН.
Часто используют тривиальные названия, которые связаны главным образом с источником их получения.
Гомологический ряд предельных одноосновных карбоновых кислот.
Формула кислот | Название по систематической номенклатуре | Название тривиальное |
НСООН | метановая кислота | муравьиная |
СН3 - СООН | этановая кислота | уксусная |
СН3 - СН2 - СООН | пропановая кислота | пропионовая |
СН3 - СН2 - СН2 - СООН | бутановая кислота | масляная |
СН3 - СН2 - СН2 - СН2 - СООН | пентановая кислота | валериановая |
С15Н31 - СООН | гексадекановая | пальмитиновая |
С17Н35 - СООН | октадекановая | стеариновая |
R - СООН
Общие формулы карбоновых кислот
СnH2n+1COOH
Приложение 5
Простейшую из кислот - муравьиную - НСООН, впервые получил в 1670 г английский естествоиспытатель Джон Рей, нагревая муравьев в перегонной колбе. В природе широко распространены и более сложные по составу кислоты. Такова, например, масляная кислота СН3-(СН2)2-СООН, которая образуется при прогоркании сливочного масла - это из-за нее испорченное масло так неприятно пахнет и горчит. Она обусловливает и запах пота. Родственная ей капроновая кислота СН3 - (СН2)4 - СООН входит в состав козьего молока. В корнях растения валерианы содержится некоторое количество изовалериановой кислоты (СН3)2 - СН2 - СН2 - СООН - ее можно выделить, обработав высушенные корни растения перегретым водяным паром.
Высшие кислоты - стеариновая С15Н31- СОООН и пальмитиновая С17Н35- СООН, впервые выделенная из пальмового масла. Долгое время основным их источником были природные жиры, например свиное сало или говяжий жир. Сейчас эти кислоты получают и синтетически - каталитическим окислением углеводородов нефти. Практическое значение имеют главным образом натриевые соли этих кислот - стеарат натиря С17Н35СООNa и пальмитат натрия С15Н31СООNа: они являются основными компонентами мыла.
Приложение 6
Интерактивный модуль
http://fcior. edu. ru/card/8349/stroenie-i-svoystva-odnoosnovnyh-karbonovyh-kislot-ih-poluchenie-i-primenenie. html (3стр)
Изомерия карбоновых кислот.

Приложение 7
С4Н9СООН
Изомерия углеродного скелета.
СН3 - СН2 - СН2 - СООН бутановая кислота
СН3- СН - СООН 2 - метилпропановая кислота
СН3
Приложение 8
В результате сильного влияния карбонильной группы 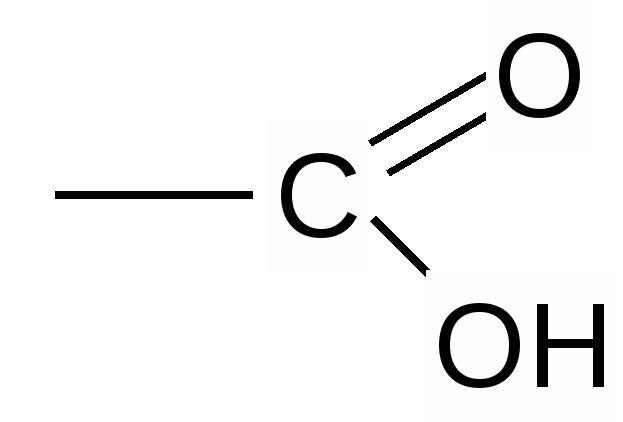 на гидроксил - ОН связь атома водорода в гидроксиле сильно ослабевает и он может отщепляться в виде иона. Это влияние можно представить так. В карбонильной группе электроны смещаются от атома углерода к кислороду как более электроотрицательному элементу. Углерод приобретает некоторый положительный заряд и притягивает к себе электроны от второго атома кислорода из гидроксильной группы. Это, в свою очередь, вызывает сдвиг электронного облака связи О - Н в направлении атома кислорода:
на гидроксил - ОН связь атома водорода в гидроксиле сильно ослабевает и он может отщепляться в виде иона. Это влияние можно представить так. В карбонильной группе электроны смещаются от атома углерода к кислороду как более электроотрицательному элементу. Углерод приобретает некоторый положительный заряд и притягивает к себе электроны от второго атома кислорода из гидроксильной группы. Это, в свою очередь, вызывает сдвиг электронного облака связи О - Н в направлении атома кислорода:
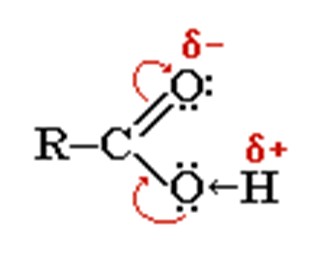
В результате связь между кислородом и водородом гидроксильной группы сильно ослабляется и становится возможным отщепление водорода.
Все карбоновые кислоты подобно неорганическим кислотам обладают кислотными свойствами и при диссоциации образуют ионы водорода:
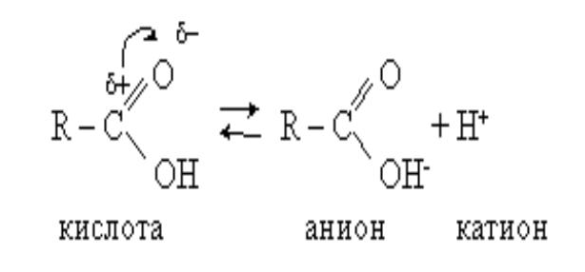
Приложение 9
Карта - инструкция
Лабораторный опыт: "Исследование физических свойств предельных одноосновных кислот"
Вспомните технику безопасности при работе с кислотами - аккуратное обращение (вызывает ожоги).
1. Рассмотреть карбоновые кислоты: муравьиную, уксусную, пальмитиновую. Определить их агрегатное состояние.
2. Определить, имеют ли они запах.
3. Проверить их отношение к воде. Для этого взять три пробирки, налить в каждую по 2 мл воды.
В пробирку № 1 - добавить 2 - 3 капли муравьиной кислоты
№ 2 - добавить 0,5 мл уксусной кислоты
№ 3 - добавить немного пальмитиновой кислоты
Встряхните пробирки. Данные опыта занесите в таблицу.
Карбоновые кислоты | Агрегатное состояние | Запах | Растворимость в воде |
Муравьиная кислота | |||
Уксусная кислота | |||
Пальмитиновая кислота |
Вывод: С1 - С8(низшие) - жидкости, запах, хорошая растворимость
с С9 (высшие) - твердые, без запаха, не растворимые в воде.
Растворимость уменьшается с увеличением относительной молекулярной массы.
Приложение 10
Карта - инструкция
Лабораторный опыт: "Действие растворимых карбоновых кислот на индикаторы"
1. В три пробирки налейте по 2 мл уксусной кислоты.
2. В каждую пробирку капните индикатор:
В пробирку №1 - лакмус
В пробирку №2 - метилоранж
В пробирку №1 - фенолфталеин
Свои наблюдения занесите в таблицу.
Лакмус | Метилоранж | Фенолфталеин |
3. Определить среду раствора уксусной кислоты. Какие свойства уксусной кислоты сходны со свойствами неорганических кислот?
Вывод: карбоновые кислоты, также, как и неорганические кислоты, имеют кислую среду, которую обуславливают ионы Н+.
Приложение 11
Общие свойства с неорганическими кислотами.
1. Взаимодействие с активными металлами.
2СН3СООН + Mg = Mg(CH3COO)2 +H2↑
уксусная ацетат магния
кислота
2СН3СООН + Zn = Zn(CH3COO)2 +H2↑
уксусная ацетат цинка
кислота
2. Взаимодействие с основными оксидами.
2НСООН + СаO = Са(HCOO)2 + H2O
муравьиная формиат кальция
кислота
3. Взаимодействие со щелочами:
СН3СН2СООН + NaОН = СН3СН2СООNa + Н2О
пропионовая пропионат натрия
кислота
4. Взаимодействие с солями более слабых и летучих кислот.
2 СН3СООН + Na2CO3 = 2CH3COONa + CO2 ↑ + H2O
уксусная ацетат натрия
кислота
Приложение 12
Особые свойства карбоновых кислот.
1. Реакция этерификации - взаимодействие карбоновых кислот со спиртами с образованием сложных эфиров.
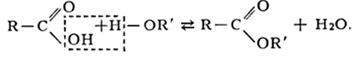
Катализаторами являются минеральные кислоты (Н2SO4).
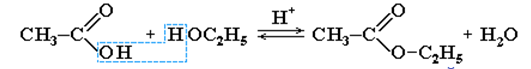
уксусная кислота этанол этиловый эфир
уксусной кислоты
(этилацетат)
2. Взаимодействие с галогенами.
У карбоновых кислот под влиянием карбоксильной группы увеличивается подвижность атомов водорода, стоящих при атоме углерода, соседнем с карбоксильной группой. Поэтому они замещаются на атомы хлора или брома:
H O H O
Сl - Cl + H - C - C Cl - C - C + HCl
H O - H H O - H
хлоруксусная кислота
б
СН3СН2СООН + Br2 СН3СНВrСООН + НBr
- бромпропионовая
кислота
Радикалы, содержащие хлор или бром, влияют на кислотность карбоксильной группы. Хлоруксусная кислота диссоциирует примерно в 10 раз больше, чем уксусная, а трихлоруксусная кислота по силе близка к соляной или серной.
Приложение 13
Задание. Рукой передвиньте на доске кислоты и составьте правильную последовательность.
СН2Сl - COOH, СН3 - СООН, CCl3 - COOH, CHCl2 - COOH
Правильная последовательность:
СН3 - СООН, СН2Сl - COOH, CHCl2 - COOH, CCl3 - COOH.
Приложение 14
Задание. (Интерактив) Используя функцию интерактивной доски "Перо", впишите на доске в уравнениях недостающее вещество:
1) СН3СООН + ... → СН3СООNa + H2O
2) ... + HO - C2H5 ↔ CH3 - CH2 - COOC2H5 + H2O
3) СН3СООН + Na2O → ... + H2O
Правильные ответы:
1) СН3СООН + NaOH → СН3СООNa + H2O
2) CH3 - CH2 - COOH + HO - C2H5 ↔ CH3 - CH2 - COOC2H5 + H2O
3) СН3СООН + Na2O → СН3СООNa + H2O
Приложение 15
Получение.
1. Действуя на соль органической кислоты более сильной неорганической кислотой.
2 СН3 - СООNa + H2SO4 → 2CH3 - COOH + Na2SO4

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



