подчеркивал, что живое вещество – самая активная форма материи во Вселенной. Оно производит гигантскую геохимическую работу в биосфере, полностью преобразовав верхние оболочки Земли за время своего существования.
10.2. Геохимическая работа живого вещества
Более 99 % энергии, поступающей на поверхность Земли, составляет излучение Солнца. Эта энергия растрачивается в громадном большинстве физических и химических процессов в гидросфере, атмосфере и литосфере: перемешивании воздушных и водных масс, выветривании, испарении, перераспределении веществ, растворении минералов, поглощении и выделении газов и т. п.
На Земле существует один-единственный процесс, при котором энергия солнечного излучения не только тратится и перераспределяется, но и связывается, запасается на очень длительное время. Этот процесс – создание органического вещества в ходе фотосинтеза. Сжигая в топках каменный уголь, мы освобождаем и используем солнечную энергию, запасенную растительностью сотни миллионов лет назад.
Основная планетарная функция живого вещества на Земле заключается, таким образом, в связывании и запасании солнечной энергии, которая затем идет на поддержание множества других геохимических процессов в биосфере.
За время существования жизни на Земле живое вещество превратило в химическую работу огромное количество солнечной энергии. Значительная часть ее в ходе геологической истории накопилась в связанном виде. Для современной биосферы характерны залежи угля и других органических веществ, образовавшихся в палеозое, мезозое и кайнозое.
В биосфере в результате жизнедеятельности микроорганизмов в больших масштабах осуществляются такие химические процессы, как окисление и восстановление элементов с переменной валентностью (азот, сера, железо, марганец и др.). Геологические результаты деятельности этих организмов проявляются в образовании осадочных месторождений серы, образовании в анаэробных условиях залежей сульфидов металлов, а в аэробных – окисление их и перевод в растворимое состояние, возникновение железных и железомарганцевых руд.
За счет жизнедеятельности огромного числа гетеротрофов, в основном грибов, животных и микроорганизмов, происходит гигантская, в масштабах всей Земли, работа по разложению органических остатков. При деструкции органической массы протекают два параллельных процесса: минерализации и образования почвенного гумуса со значительным запасом энергии. Гумус – это основа почвенного плодородия. Его разложение протекает в дальнейшем очень медленно, под влиянием определенной, автохтонной микрофлоры почв, чем достигается постоянство в обеспечении растений элементами минерального питания.
Природные воды, обогащенные продуктами минерализации, становятся химически высокоактивными и разрушают горные породы.
Живые организмы создали и поддерживают газовый состав современной атмосферы. Некоторая несбалансированность процессов синтеза и разложения органических веществ в биосфере определила кислородный режим современной воздушной оболочки Земли.
Кислород атмосферы накоплен за счет фотосинтеза. Единственный источник абиогенного поступления свободного кислорода – фотодиссоциация молекул воды в верхних слоях атмосферы – очень незначителен.
Выделенный растениями кислород вновь используется на окисление углерода при минерализации органического вещества и дыхании организмов, но так как часть органических веществ захоранивается в осадочных породах, то эквивалентное количество О2 остается в атмосфере. Значительная часть его идет на окисление минеральных веществ. Весь наличный запас свободного кислорода в атмосфере оценивается в 1,6 · 1015 г, зеленые растения могут воссоздать его за 10 тыс. лет.
В верхних слоях тропосферы под влиянием ультрафиолетового излучения из кислорода образуется озон. Существование озонового экрана также результат деятельности живого вещества, которое, по выражению , «как бы само создает себе область жизни».
Углекислый газ поступает в атмосферу за счет дыхания всех организмов. Второй, менее мощный его источник – выделение по трещинам земной коры из осадочных пород за счет химических процессов, совершающихся под действием высоких температур. Он также имеет биогенное происхождение. Часть углекислого газа поступает в атмосферу из абиогенного источника – непосредственно из мантии Земли при вулканических извержениях. Эта часть лишь 0,01 % от СО2, выделенного живыми организмами. Расходуется углекислый газ в процессах органического синтеза, а также на выветривание горных пород и образование карбонатов.
Азот атмосферы химически инертен, но и он участвует в процессах синтеза и распада органического вещества. Азот усваивают из атмосферы многие прокариотические организмы – азотфиксаторы. После гибели бактерий азот переходит в доступные растениям соединения и включается в цепи питания и разложения.
К газам органического происхождения относятся также сероводород, метан и множество других летучих соединений, создаваемых живым веществом. За один день, например, 1 га можжевелового леса может выделить в атмосферу до 30 кг летучих веществ – фитонцидов.
Продуцируя и потребляя газообразные вещества, организмы биосферы поддерживают постоянство состава воздушной оболочки Земли.
Живое вещество перераспределяет атомы в биосфере. Многие организмы обладают способностью накапливать, концентрировать в себе определенные элементы, несмотря на часто ничтожное содержание их в окружающей среде. Например, литотамниевые водоросли накапливают в своих телах до 10 % магния, в раковинах брахиопод содержится около 20 % фосфора, в серных бактериях – до 10 % серы. Многие организмы концентрируют кальций, кремний, натрий, алюминий, иод и т. д. Отмирая и захораниваясь в массе, они образуют скопления этих веществ. Возникают залежи таких соединений, как известняки, бокситы, фосфориты, осадочная железная руда и др. Многие из них человек использует как полезные ископаемые.
Живое вещество активно участвует также в грандиозных процессах перемещения, миграции атомов в биосфере через систему больших и малых круговоротов.
10.3. Стабильность биосферы
Основой самоподдержания жизни на Земле являются биогеохимические круговороты. Процессы созидания органического вещества, аккумулирующего энергию, и противоположные процессы его разложения с высвобождением этой энергии одинаково необходимы для существования жизни. Все доступные для живых организмов химические соединения в биосфере имеют предел. Исчерпаемость пригодных для усвоения химических веществ часто тормозит развитие тех или иных групп организмов в локальных участках суши или океана. По выражению академика , единственный способ придать конечному свойства бесконечного – это заставить его вращаться по замкнутой кривой. Все химические элементы, используемые в процессах жизнедеятельности организмов, совершают постоянные перемещения, переходя из живых тел в соединения неживой природы и обратно. Возможность многократного использования одних и тех же атомов делает жизнь на Земле практически вечной при условии постоянного притока нужного количества энергии.
Глобальный биогеохимический круговорот вещества на планете представляет собой систему сложно переплетенных циклов отдельных элементов, связанных друг с другом по аналогии с деталями часового механизма (рис. 163). Объединяясь в разных пропорциях в составе сложных органических молекул, синтезируемых в живых телах, атомы различных элементов вне живого вещества имеют свою «судьбу» в атмосфере, гидросфере и литосфере. Круговороты планетарного масштаба создаются из бесчисленных локальных циклических перемещений атомов, движимых жизнедеятельностью организмов в отдельных экосистемах, и тех перемещений, которые вызываются действием ландшафтных и геологических причин (поверхностный и подземный сток, ветровая эрозия, движение морского дна, вулканизм, горообразование и т. п.). Различают поэтому малые и большие круговороты в соответствии с объемом рассматриваемых экосистем: локальные биологические круговороты, биогеохимические циклы материков и океанов и, наконец, общепланетарный биогеохимический круговорот.
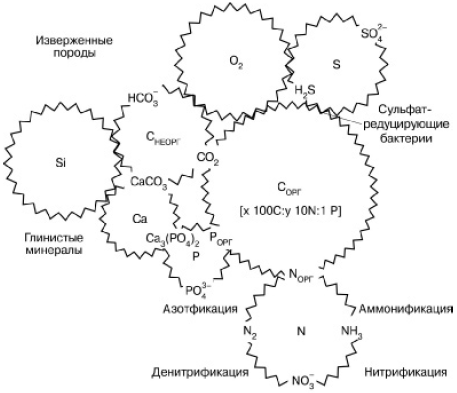
Рис. 163. Сопряжения циклов элементов в биосфере (по , 1998)
Вместе с тем отличительная черта биологических круговоротов – их неполная замкнутость. Часть химических элементов и их соединений постоянно выпадает из общей циркуляции и скапливается вне организмов, создавая своего рода запасы биогенных веществ. Так были накоплены кислород и азот в атмосфере, горючие ископаемые и другие породы земной коры. В масштабах геологического времени даже небольшое неравновесие в создании и разрушении органических веществ приводит к направленному преобразованию поверхностных слоев Земли.
Запасы биогенных веществ, мало доступные для живых организмов и медленно вовлекающиеся поэтому в биологический круговорот, составляют так называемый резервный фонд того или иного химического элемента в биосфере (например, кальция в карбонатных породах). Другая часть, интенсивно циркулирующая между телами организмов и окружающей средой, называется подвижным, или обменным, фондом. Соотношения между резервным и обменным фондами в биосфере у всех биогенных элементов различны.
Углерод. Углерод как химический элемент является основой жизни. Он может соединяться разными способами со многими другими элементами, образуя простые и сложные органические молекулы, входящие в состав живых клеток. По распространению на планете углерод занимает одиннадцатое место (0,35 % от веса земной коры), но в живом веществе в среднем составляет около 18 или 45 % от сухой биомассы.
В атмосфере углерод входит в состав углекислого газа СО2, в меньшей мере – в состав метана СН4 или следового количества других газообразных соединений. В гидросфере СО2 растворен в воде, и общее его содержание намного превышает атмосферное. Океан служит мощным буфером регуляции СО2 в атмосфере: при повышении в воздухе его концентрации увеличивается поглощение углекислого газа водой. Некоторая часть молекул СО2 реагирует с водой, образуя угольную кислоту, которая затем диссоциирует на ионы НСО3– и СО2-3. Эти ионы реагируют с катионами кальция или магния с выпадением карбонатов в осадок. Подобные реакции лежат в основе буферной системы океана, поддерживающей постоянство рН воды. При подкислении (увеличении концентрации ионов Н+) происходит сдвиг влево в цепи: СО2 воздуха → СО2 воды → Н2СО3 → Са(НСО3)2 → СаСО3. При подщелачивании усиливается выпадение в осадок карбонатов кальция.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 |



