протекает до конца, т. к. ц0Li+/Li = −3,05 В, а в результате протекания процесса образуется хорошо растворимое основание;
- Процесс:
Zn + 2Н2О = Zn(OH)2 + Н2↑
практически не идет т. к. ц0Zn+2/Zn= −0,76 В, однако в результате протекания процесса образуется трудно растворимое основание.
2. Взаимодействует с некоторыми неметаллами:
Br2 + H2O D HBrO + HBr
Окислитель- продукт продукт
восстановитель окислен. восстановл.
C + H2O t→ CO + H2↑.
восстановитель окислитель продукт продукт
окислен. восстановл.
3. Со многими основными и кислотными оксидами вода образует гидроксиды или кислоты:
ВаО + Н2О = Ва(ОН)2; N2О5 + Н2О = 2НNО3,
основный кислотный
4. Участвует в реакциях гидролитического разложения соединений (гидролиз солей), например:
КNО2 + Н2О D КОН + НNО2 или SO2Cl2+ 2Н2О = Н2SО4 +2HCl.
5. Взаимодействует со многими безводными солями, образуя аквакомплексы и кристаллогидраты: NiSO4*7H2O = [Ni(H2O)6]SO4*H2O.
6. Способствует протеканию большого числа окислительно-восстановительных и обменных процессов между другими веществами.
7. Вода – практически универсальный растворитель. В живых организмах вода образует среду для переноса питательных веществ к клеткам и для удаления вредных веществ.
Соединения пероксидного типа (соединения со с. о. кислорода (-1/2, -1))
Энергия сродства к электрону молек эВ, а ее энергия ионизации – 12,08 эВ. При химических превращениях молекула кислорода может присоединять или терять электроны с образованием молекулярных ионов типа: О2−2, О2−, О2+.
В ряду: О2+→ О2 → О2− → О2−2 расстояние между атомами кислорода увеличивается, а средняя энергия связи уменьшается.
1) При присоединении одного электрона к молекуле кислорода образуется надпероксид-ион О2−:
О2 + 1з = О2−, ΔН0298 = −84 кДж/моль.
Производные радикала О2− - надпероксиды. Они образуются при взаимодействии наиболее активных щелочных металлов (К, Rb, Cs) с кислородом, например: К + О2 = КО2 (с. о. атома О = −1/2).
Свойства надпероксидов
Обладают парамагнитными свойствами, окрашены, что обусловлено неспаренным электроном у надпероксид-иона О2−.
Сильные окислители, бурно реагируют с водой: 4КО2 + 2H2O = 4КОН + 3О2.
2) При присоединении двух электронов к молекуле кислорода образуется пероксид-ион О2−2 :
О2 + 2з = О2−2, ΔН0298 = 159 кДж/моль.
Атомы кислорода в пероксид-ионе связаны 2-х электронной связью, поэтому он диамагнитен. Производные радикала О2-2 - пероксиды. Все пероксиды – неокрашены. Они образуются при окислении ряда активных металлов, например:
Ва + О2 = ВаО2 (пероксид бария).
Наибольшее практическое значение имеет пероксид (перекись) водорода H2O2. Ее молекула имеет следующее геометрическое строение:
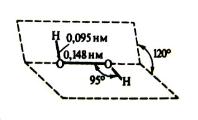
Молекула пероксида водорода сильно полярная (μ = 0,7 D), поэтому между молекулами возникает водородная связь, приводящая к их ассоциации. При обычных условиях пероксид водорода – сиропообразная жидкость. С водой смешивается в любых соотношениях, в воде проявляет слабые кислотные свойства:
H2O … H2O2 ⇔ H3O+ + HO2-, Кд = 2,24⋅10-12.
Химические свойства пероксида водорода
1) Пероксид-радикалы участвуют в реакциях обмена:
H2O2 + 2КОН = К2O2 + 2H2O,
ВаО2 + H2SO4 = ВаSO4↓ + H2O2.
Последняя реакция используется для получения пероксида водорода.
2) Более характерны реакции, приводящие к разрушению связи О-О, т. е. H2O2 проявляет окислительные и восстановительные свойства (окислительно-восстановительную двойственность):
а) окислитель: H2O2 + 2Н+ + 2з = 2H2O, φ0 = 1,78 В;
H2O2 + 2з = 2ОН-, φ0 = 0,87 В;
б) восстановитель: O2-2 - 2з = O20,
H2O2 - 2з = O2 + 2H+, φ0 = −0,68 В;
H2O2 + 2ОН - - 2з = O2 + 2 H2O, φ0 = +0,076 В.
Например:
а) 2NaI + Na2O2 + 2H2SO4 = I2 + 2Na2SO4 + 2H2O.
восст. окисл. среда пр. окисл. пр. восст.
б) 2KMnO4 + 5H2O2 + 2H2SO4 = 2MnSO4 + 5O2 + K2SO4 + 8H2O.
окисл. восст. среда пр. восст. пр. окисл.
Окислительные свойства пероксида водорода выражены сильнее, чем восстановительные, поскольку в ней всегда присутствуют следы атомарного кислорода [O]. Восстановительные свойства H2O2 проявляет только по отношению к очень сильным окислителям, таким, как пермаганат калия.
3) Для пероксида водорода характерной является реакция диспропорционирования:
H2O2(-1) + H2O2(-1) = 2H2O(-2) + О2(0).
4) Молекула H2O2 в качестве нейтрального лиганда может входить во внутреннюю сферу комплексных соединений: [Fe(H2O)5(H2O2)]-3, а также образовывать аналогичные кристаллогидратам пероксогидраты: K2CO3⋅2H2O2; CaO2⋅2H2O2; BaO2⋅2H2O2 ⋅2H2O и др.
5) Роль лиганда в комплексном соединении может играть пероксид-ион (O22-). Кислоты, в составе которых имеется пероксид-ион, называются пероксокислотами. Например:
Название кислоты | Химическая формула | Графическая формула |
Пероксоазотная | HNO4 | O H-O-O-N≪ O |
Пероксомоносерная | H2SO5 | H-O-O O >S≪ H-O O |
Все пероксокислоты являются сильными окислителями и в растворах, и в расплавах. Это объясняется следующим: при гидролизе пероксокислот образуется пероксид водорода, что используется для его получения в промышленности: H2SO5 + H2O = H2SO4 + H2O2.
Применение пероксида водорода. Его водные растворы используются для отбеливания различных материалов, для обеззараживания сточных вод. Пероксид водорода используется в качестве окислителя ракетного топлива.
Соединения со степенью окисления кислорода (+1, +2).
Эти с. о. кислорода проявляются в его соединениях с фтором, например: О(+2)F2 (дифторид кислорода) и О2(+1)F2 (диоксидифторид кислорода).
Дифторид кислорода непосредственно получить невозможно, его получают косвенным путем – при быстром пропускании газообразного фтора через 2%-ный раствор щелочи:
2F2 + 2NaOH = OF2 + 2NaF + H2O.
Это – ядовитый газ бледно-желтого цвета, термически устойчивый, сильный окислитель, эффективный фторирующий агент.
Диоксидифторид кислорода образуется при взаимодействии простых веществ под действием электрического разряда:
/F
О−О + F2 = O=O
F/
Соединение крайне неустойчиво, является сильным окислителем.
Соединения со степенью окисления кислорода (+4)
В качестве производного, в котором кислород проявляет с. о., равную +4, можно рассматривать озон: О3 = О(+4)О2(-2).
Молекула озона диамагнитна, имеет угловую форму, порядок связи О-О в молекуле озона – 1,5, молекула слабополярна (μ = 0,17 D). Ее строение с точки зрения метода валентных связей (МВС) можно представить следующим образом. Центральный атом кислорода находится в состоянии sp2-гибридизации и имеет уголковое строение:
О4+ | |
О2- | О2- |
В химическом отношении более активен, чем кислород. Озон – очень сильный окислитель. Так, О2 не окисляет иодид-ион, а О3 окисляет:
2KI + О3 + Н2О = I2 +2КОН + О2.
Эта реакция используется для открытия озона: в воздух, содержащий озон, помещают бумажку, смоченную растворами КI и крахмала; по мере протекания процесса бумажка синеет.
Озон обладает высоким сродством к электрону, поэтому при присоединении одного электрона образуется озонид-ион: О3 + 1з = О3−. При действии озона на щелочные металлы образуются озониды, состоящие из катиона металла и озонид-ионов (О3-).
Например: К + О3 = КО3(-1/3).
Озониды – парамагнитны, окрашены в красный цвет, что объясняется наличием у озонид-иона одного неспаренного электрона. Озониды являются сильными окислителями.
Применение озона. Используется для очистки питьевой воды, для дезинфекции воздуха в помещениях, в различных химических синтезах.
СераСера известна человеку с давних времен. Она является типичным неметаллом. Известны соединения серы почти со всеми элементами. Элемент третьего периода, электронный аналог кислорода. Электронное строение атома элемента выражается электронной формулой – 3216S 1s22s22p63s23p4. Электронное строение валентного слоя – 3s23p4 или в виде электронографической формулы:
n=3 | ↓↑ | ↓ | ↑ |
↓↑ |
s p d
Валентные возможности серы расширены за счет свободных 3d-орбиталей. Для серы, в соответствии с правилом четности, наиболее устойчивыми являются четные степени окисления (с. о.): -2, 0, +2, +4, +6, наиболее характерными – высшая с. о. (+6) и низшая с. о. (-2).
Природные соединения. Достаточно широко распространенный элемент: в земной коре содержится ~5⋅10-2 масс. долей %, в мировом океане - 9⋅10-2 масс. долей процента. Формы нахождения в земной коре – многообразны:
- Самородная сера; Сульфиды и полисульфиды: FeS2 – пирит, PbS – галенит, ZnS – сфалерит, As2S3 – аурипигмент, Bi2S3 – висмутовый блеск (висмутин), FeAsS - мышьяковый колчедан (арсенопирит) и др.; Сульфаты: гипс – CaSO4⋅2H2O, глауберова соль – Na2SO4⋅10H2O, барит – ВaSO4 и др.; Содержится в водах морей, некоторых минеральных источников (в виде H2S), выделяется при вулканической деятельности; Входит в состав каменных углей, нефти, природных газов.
Получение. Способы получения свободной серы также различны:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



