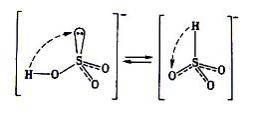
Несвязывающая электронная пара пространственно направлена, поэтому сульфит-анион – активный донор электронной пары и легко переходит в тетраэдрические ионы: гидросульфит-анионы НSO3- и сульфат-анионы SO4-2, что обуславливает его достаточно сильные восстановительные свойства:
SO3-2 + 2ОН - - 2з = SO4-2 + Н2О, φ0 = -0,90 В.
Например: 2KmnO4 + 3Na2SO3 + Н2О = 3Na2SO4 + 2mnO2↓ + 2КОН.
окисл. восст. среда прод. ок. прод. восст.
Свойства SO2 и сульфитов
- Сульфиты в растворах постепенно окисляются даже кислородом воздуха: 2SO3-2 + О2 = 2SO4-2. Восстановительные свойства проявляет и диоксид серы, который на солнечном свету окисляется хлором: SО2 + Сl2 = SO2Сl2. При взаимодействии с более сильными восстановителями производные S(IV) проявляют окислительные свойства:
S(+4)О2 + 2Н2S(-2) = 3S0↓ + 2Н2О.
Окислитель восстановитель
- При нагревании сульфиты диспропорционируют:
4Na2S(+4)O3=3Na2S(+6)O4+Na2S(-2).
- В водных растворах соли сернистой кислоты подвергаются гидролизу.
Применение диоксиды серы:
- при производстве серной кислоты; в бумажном и текстильном производствах; в качестве отбеливающего средства; для консервации плодов.
Соединения со степенью окисления серы (+6)
Эта с. о. проявляется в следующих соединениях и отвечающих им анионных комплексах:
SF6 | SO2Hal2 | SO3 |
- | [SO3Hal]- | [SO4]-2 |
В обычных условиях фторид серы (VI) – газ, а оксогалогениды серы (VI) – жидкости или газы. Молекулы SF6, SO2Наl2, SO3 имеют, соответственно, форму правильного октаэдра, искаженного тетраэдра и плоского треугольника:
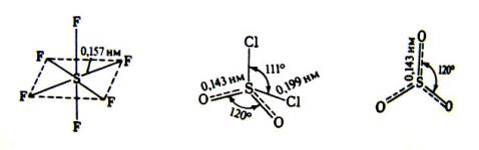
Cоединения S (VI) – типичные кислотные соединения. Большинство из них легко гидролизуется, образуя соответствующие кислоты:
SО3+ Н2О = 2Н+ + SO4-2;
SО2Сl2 + 2Н2О = 4Н+ + SO4-2+ 2Сl-.
Гексафторид серы SF6 отличается высокой химической стойкостью, не взаимодействует ни с водой, ни со щелочами, ни с кислотами. Атом серы находится в этом соединении в состоянии sp3d2-гибридизации. Геометрическое строение молекулы SF6 – правильный октаэдр.
Используется в качестве газообразного изолятора в генераторах высокого напряжения.
Оксид серы (VI) (триоксид серы, серный ангидрид).
Для S (VI) характерным является к. ч. = 4, поэтому молекула SO3 полимеризуется в кольцеобразные или открытые полимерные цепи.
Известно несколько модификаций SO3:
1) при конденсации паров SO3 образуется летучая жидкость, состоящая из циклических полимерных молекул (SO3)3;
2) льдообразная модификация γ- SO3 образуется при ее охлаждении;
3) асбестовидная модификация α- SO3 состоит из зигзагообразных цепей различной длины.
SO3 хорошо растворяется в воде, в результате чего образуется серная кислота. Процесс растворения сопровождается выделением теплоты:
SO3 +Н2О = Н2SO4, ΔН0298 = −62,7 кДж/моль.
Химические свойства серной кислоты.
Безводная серная кислота – вязкая маслянистая жидкость без запаха и цвета, практически не проводящая электрический ток. Является ионизирующим растворителем, однако ее собственная ионизация незначительна:
Н2SO4 … Н2SO4 ⇔ Н3SO4+ + НSO4-, К = 2,7⋅10−4.
В водных растворах серная кислота – сильная двухосновная кислота: К1 = 1⋅103, К2 = 1,2⋅10-2.
В соответствии с представлениями ВМС, химическое строение сульфат-ионов представляется следующим образом: атом серы в сульфат-ионе находится в состоянии sp3-гибридизации, поэтому он имеет форму правильного тетраэдра; все расстояния и углы в нем равноценны. А химическое строение молекулы серной кислоты отвечает искаженному тетраэдру, еще большее искажение характерно для гидросульфат-аниона. Сульфат-анион – SO42- – имеет форму правильного тетраэдра, поскольку все расстояния и углы в нем равноценны:
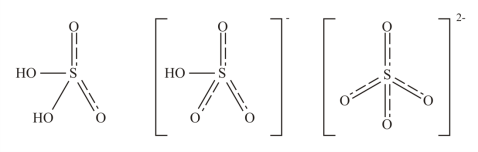
Молекула серной кислоты | Гидросульфат-анион | Сульфат-анион |
Свойства концентрированной серной кислоты.
1) Обладает сильным водоотнимающим действием, поэтому ее используют в качестве эффективного осушителя.
2) Обладает сильными окислительными свойствами, она окисляет:
- Br и HI – до свободных галогенов:
2КBr + 2H2SO4(конц.) = К2SO4 + Br2 + SO2↑ + H2O;
8КI + 5H2SO4(конц.) = 4К2SO4 + 4I2 + H2S↑ + 4H2O;
- уголь – до СО2: 6С + 4H2SO4(конц.) = 6СO2 + 4S↓ + 4H2O; серу – до SO2: 3S + 2H2SO4(конц.) = 3SO2 + 2S↓ + 2H2O; обугливает органические материалы (бумага, шерсть, кожа); взаимодействует со всеми металлами, за исключением Ag, Au, Pt. Концентрированная серная кислота пассивирует некоторые металлы: алюминий, хром, железо.
Окислителем в концентрированной серной кислоте является сера (VI), которая в зависимости от силы восстановителя может быть восстановлена до сероводорода, свободной серы или сернистого ангидрида. В частности, в зависимости от активности металла образуются разные продукты восстановления; металл окисляется при этом до высших с. о.. Это можно представить в виде следующей схемы:
Активный (1) → | H2S↑ | ||
H2SO4(конц.) + Ме | Ср. активности (2) → | S↓ | + Ме2(SO4)n + Н2О |
Малоактивный (3) → | SO2↑ |
Примеры:
1) 4Mg + 5H2SO4(конц.) = 4MgSO4 + H2S↑ + 4H2O;
2) 3Zn + 4H2SO4(конц.) = 3ZnSO4 + S↓ + 4H2O;
3) Cu + 2H2SO4(конц.) = CuSO4 + SO2↑ + 2H2O.
Свойства разбавленной серной кислоты.
Разбавленная серная кислота также взаимодействует с металлами. Однако окислителем в этих процессах является катион водорода, восстановители – атомы металла. Все металлы, имеющие стандартный электродный потенциал ниже нуля, φ0 0 (т. е., стоящие в ряду активности металлов до водорода), взаимодействуют с разбавленной серной кислотой. При этом образуется соль металла в его низшей с. о. и идет восстановление водорода. Эта реакция идет до конца, если в результате процесса образуется растворимая в воде соль. Например:
Fe + H2SO4(разб.) = FeSO4 + H2↑;
Pb + 4H2SO4(разб.) ≠ PbSO4↓ + H2↑.
Последний процесс термодинамически возможен, т. к. Pb находится в ряду напряжений до водорода (φ0 = −0,127 В), однако на поверхности металла образуется пленка из малорастворимого вещества PbSO4, которая изолирует поверхность металла от дальнейшего взаимодействия, процесс практически прекращается.
Соли серной кислоты – сульфаты и гидросульфаты – в основном хорошо растворимы в воде. Из водных растворов они выделяются в виде кристаллогидратов.
Применение серной кислоты:
- при производстве кислот, щелочей, солей, хлора, минеральных удобрений, взрывчатых веществ; в органическом синтезе; для очистки керосина, нефтяных масел и продуктов коксохимической промышленности (бензол, толуол); в производстве лакокрасочных материалов; для травления поверхности черных металлов (снятие окалины).
Тиосульфаты. Получение, свойства, применение.
При кипячении раствора сульфита натрия с порошком серы образуется тиосульфат натрия, натриевая соль тиосерной кислоты (Н2S2O3 или Н2SO3S):
Na2SO3(р-р) + S(кр.) t= Na2S2O3(р-р) (или Na2SO3S),
Или в ионно-молекулярной форме:
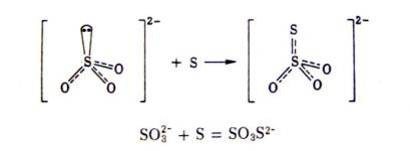
Свойства тиосульфатов обусловливаются присутствием атомов серы в двух разных с. о.: +6 и –2:
Na | O | S(2-) | |
Na | O | S(6+) | O |
Наиболее характерными свойствами тиосульфатов являются:
1) Восстановительные свойства:
Na2SO3S + Cl2 + H2O = Na2SO4 + S + 2HCl.
При действии на тиосульфат натрия слабых окислителей, например, йода, получим:
Na2SO3S + I2 = Na2S4O6 + 2NaI, или
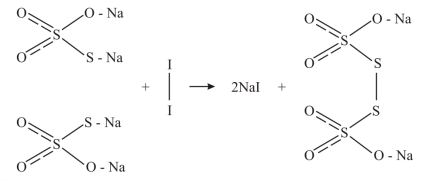
Тетратионат натрия, Na2S4O6 – соль тетратионовой кислоты, Н2S4O6, которая относится к политионовым кислотам, имеющим состав Н2SnO6 (n=3ч6).
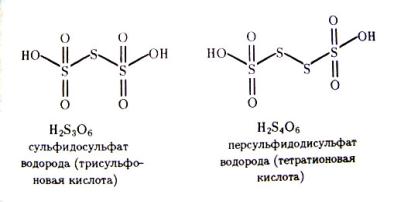
Это двухосновные кислоты, характеризующиеся как неустойчивые, существующие только в водных растворах. Тетратионовая кислота также является неустойчивой, ее соли более устойчивы, они могут быть получены в кристаллическом состоянии.
2) Склонность к диспропорционированию. Тиосульфат водорода (тиосерная кислота) Н2SO3S неустойчив и при получении распадается (диспропорционирует):
Na2SO3S + Н2SO4 = Na2SO4 + Н2SO3S.
↓ ↓
Н2SO3 S
Из тиосульфатов наибольшее практическое значение имеет тиосульфат натрия (гипосульфит) Н2S2O3·3Н2O. Он используется в фотографии и медицине.
Производные серной кислоты
1) Подобно оксиду серы (VI) полимерными могут быть и сульфат-анионы. Так, при растворении серного ангидрида (SO3) в концентрированной серной кислоте образуется серия полисерных кислот:
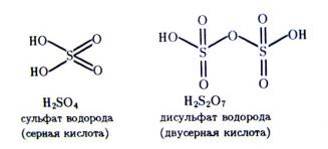
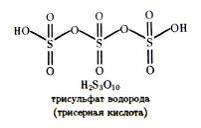
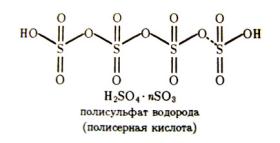

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



