Смесь кислот: H2SO4, H2S2O7, H2S3O10, H2S4O13 – представляет собой густую маслянистую, дымящую на воздухе жидкость, которую называют олеум.
2) Одним из лигандов в сульфат-анионе может быть пероксорадикакал, О2−2:
−2
О | O | О |
S | ||
O | О |
Производные [SO3(O2)]−2 – аниона (SO5−2) называются пероксосульфатами (VI), а водный раствор H2SO5 – пероксомоносерной кислотой.
3) роль мостика, объединяющего тетраэдрические структурные единицы (SO4−2), может также играть пероксидная группировка атомов:
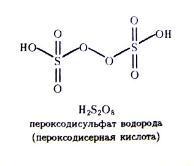
Пероксодисерную кислоту можно получить при электролизе водного раствора серной кислоты или водного раствора гидросульфатов:
А (+): 2НSO4− − 2м = H2S2O8.
Обе кислоты – и пероксомоносерная, и пероксодисерная – гидролизуются с образованием пероксида водорода:
H2S2O8 + 2H2O = 2H2SO4 + H2O2,
H2SO5 + H2O = H2SO4 + H2O2.
Все пероксосульфаты (VI) являются сильными окислителями.
ОБОРУДОВАНИЕ Активные клавиши

Рис. 3.1. Функции манипулятора
Левая клавиша мыши (ЛКМ) - при нажатии берется объект (пробирка,
палочка для перемешивания, капельница)
Средняя клавиша мыши (СКМ) - при прокрутке назад (на себя) сцена отдаляется, при прокрутке вперед (от себя) сцена приближается.
Правая клавиша мыши (ПКМ) - при нажатии на объект происходит действие (из капельницы капает вещество, палочка перемешивает вещество)
Движение мыши:
движение вправо - сцена движется вправо,
движение влево - сцена движется влево,
движение вверх - сцена движется вверх,
движение вниз - сцена движется вниз.
Лабораторное оборудование
Для проведения лабораторной работы необходимо следующее оборудование:
На лабораторном столе стоят:
Опыт №1:
- 4 капельницы с надписями: H2SO4 Ba(NO3)2 Sr(NO3)2 Pb(NO3)2
Опыт №2:
- 2 капельницы с надписью: Иодная вода; Na2S2O3
Опыт №3:
- 2 склянки с надписью: Al (алюминий) Сu (медь) 1 капельница с надписью: H2SO4 (р)
Опыт №4:
- 1 капельница с надписью: 3% H2O2
- 1 склянка с надписью: МnO Тонкая деревянная палочка Зажигалка
Для каждого опыта:
- Штатив с пробирками Стаканчик с водой Стеклянная палочка для перемешивания реактивов Микрошпатель
Справа находится кнопка вызова меню (рис. 3.2). В нем можно увидеть выпадающее меню для переключения между опытами (кнопки «Опыт 1», «Опыт 2» и т. д.), кнопку «Начать заново», кнопку выхода из лабораторной работы, окна с подсказками к текущему опыту в лабораторной работе (какие вещества нужно добавить в пробирку), кнопку для вызова окна настроек (рис. 3.4), в котором можно включить полноэкранный режим, настроить качество графики. Для выхода из полноэкранного режима нажать клавишу ESC.

Рис. 3.2. Кнопка вызова бокового меню

Рис. 3.3. Боковое меню.
Рис. 3.4. Окно настроек
При наведении курсора мышки на капельницу с веществом в верхней части экрана появляется надпись с названием вещества. На рис. 3.5. показан пример отображения надписи при наведении курсора на капельницу с надписью H2SO4.

Рис. 3.5. Отображение названия капельницы в верхней части экрана
4. ПОРЯДОК ПРОВЕДЕНИЯ РАБОТЫ
Цель работы: Изучение свойств р - элементов: 1. Свойств серной кислоты и ее солей; 2. Восстановительные и окислительные свойства сульфитов – солей сернистой кислоты; 3. Окислительные свойства кислорода.
Опыт № 1. Получение малорастворимых солей серной кислоты.
Налить в три пробирки по 2 - 3 капли разбавленной серной кислоты. Добавить в каждую из пробирок по 1- 2 капли раствора: в первую – нитрата бария, во вторую – нитрата стронция, в третью – нитрата свинца.
Отметить цвет образовавшихся осадков. Написать уравнения реакций. Сравнить величины ПР образовавшихся малорастворимых сульфатов и решить в каком случае происходит наиболее полное осаждение сульфат – ионов.
Последовательность действий:
- Берем первую пробирку (нажать на пробирку ЛКМ); Берем капельницу с надписью H2SO4 (нажатие ЛКМ); Капаем 3 капли H2SO4 в пробирку (3 нажатия ПКМ); Отставляем капельницу с H2SO4 в сторону (нажатие ЛКМ); Берем капельницу с надписью Ba(NO3)2 (нажатие ЛКМ); Капаем 3 капли Ba(NO3)2 в пробирку с H2SO4 (3 нажатия ПКМ); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Наблюдаем выпадение осадка белого цвета; Убираем пробирку с содержимым в штатив (нажатие ЛКМ); Берем вторую пробирку (нажатие ЛКМ); Берем капельницу с надписью H2SO4 (нажатие ЛКМ); Капаем 3 капли H2SO4 во вторую пробирку (3 нажатия ПКМ); Отставляем капельницу с H2SO4 в сторону (нажатие ЛКМ); Берем капельницу с надписью Sr(NO3)2 (нажатие ЛКМ); Капаем 3 капли Sr(NO3)2 в пробирку с H2SO4 (3 нажатия ПКМ); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Наблюдаем выпадение осадка белого цвета; Убираем пробирку с содержимым в штатив (нажатие ЛКМ); Берем третью пробирку (нажатие ЛКМ); Берем капельницу с надписью H2SO4 (нажатие ЛКМ); Капаем 3 капли H2SO4 в третью пробирку (3 нажатия ПКМ); Отставляем капельницу с H2SO4 в сторону (нажатие ЛКМ); Берем капельницу с надписью Pb(NO3)2 (нажатие ЛКМ); Капаем 3 капли Pb(NO3)2 в пробирку с H2SO4 (3 нажатия ПКМ); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Наблюдаем выпадение осадка белого цвета; Убираем пробирку с содержимым в штатив (нажатие ЛКМ); Записываем уравнения данных реакций в молекулярном и кратком ионно-молекулярном виде. Сравнить величины произведения растворимости образовавшихся сульфатов и сделать вывод, в каком случае происходит наиболее полное осаждение сульфат-ионов.
Опыт № 2 Взаимодействие тиосульфата натрия с галогенами.
Окисление тиосульфата натрия йодной водой.
В пробирку с йодной водой (5 – 6 капель) прибавлять по каплям раствор тиосульфата натрия до обесцвечивания йодной.
Наблюдается ли в этом случае появление свободной серы?
Написать уравнения реакции, если тиосульфат – ион окисляется до тетратионат иона (S2O32- → S4O62- ) и реакция идет по схеме:
Na2S2O3 + I2 → Na2S4O6 + NaI
Последовательность действий:
Берем пробирку (нажать ЛКМ на пробирку); Берем капельницу с надписью Йодная вода (нажатие ЛКМ); Капаем 5 капель иодной воды в пробирку (5 нажатий ПКМ); Отставляем капельницу с надписью иодная вода в сторону (нажатие ЛКМ); Берем капельницу с надписью Na2S2O3 (нажатие ЛКМ); Добавляем по каплям Na2S2O3 в пробирку с иодной водой до полного обесцвечивания (5 нажатий ПКМ); Отставляем капельницу с надписью Na2S2O3 в сторону (нажатие ЛКМ); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Наблюдаем, что выпадение свободной серы не происходит; Записываем уравнение соответствующей реакции в молекулярном виде, если тиосульфат-ион окисляется до тетратионат иона (S2O32- → S4O62-).Опыт № 3 Взаимодействие серной кислоты с металлами.
Взаимодействие разбавленной серной кислоты с металлами
Взять 2 пробирки и поместить в одну из них несколько кусочков алюминия, во вторую – несколько кусочков меди. Прилить в каждую из пробирок по 5 – 6 капель раствора серной кислоты.
В каком случае реакция не будет протекать? Написать уравнение протекающей реакции. Какой элемент является окислителем?
Последовательность действий:
Берем пробирку (нажать ЛКМ на пробирку); Берем капельницу с надписью H2SO4 (р) (нажатие ЛКМ); Капаем 4 капли H2SO4 (р) в пробирку (4 нажатия ПКМ); Отставляем капельницу с надписью H2SO4 (р) в сторону (нажатие ЛКМ); Помещаем с помощью микрошпателя 1 кусочек алюминия из склянки с надписью Al (алюминий) в пробирку с H2SO4 (р) (нажатие ЛКМ на микрошпатель); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Наблюдаем, что происходит интенсивное выделение пузырьков газа. Записать уравнение соответствующей реакции. Какой газ выделяется в процессе окисления металла? Какой элемент является окислителем? Убираем пробирку с содержимым в штатив (нажатие ЛКМ);; Берем вторую пробирку (нажатие ЛКМ); Берем капельницу с надписью H2SO4 (р) (нажатие ЛКМ); Капаем 4 капли H2SO4 (р) в пробирку (4 нажатия ПКМ); Отставляем капельницу с надписью H2SO4 (р) в сторону (нажатие ЛКМ); Помещаем с помощью микрошпателя 1 кусочек меди из склянки с надписью Сu (медь) в пробирку с H2SO4 (р) (нажатие ЛКМ на микрошпатель); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Наблюдаем, что выделение пузырьков газа не происходит Делаем вывод о возможности взаимодействия разбавленной серной кислоты с медью. Почему разбавленная серная кислота не может окислить медь?Опыт № 4 Получение кислорода при каталитическом разложении пероксида водорода.
Последовательность действий:
Берем пробирку (нажать ЛКМ на пробирку); Берем капельницу с надписью 3% H2O2 (нажатие ЛКМ); Капаем 5 капель 3% H2O2 в пробирку (5 нажатий ПКМ); Отставляем капельницу с надписью 3% H2O2 в сторону (нажатие ЛКМ); Помещаем 1 микрошпатель из склянки с надписью МnO в пробирку с 3% H2O2 (нажатие ЛКМ на микрошпатель); Отставляем склянку с надписью МnO в сторону (нажатие ЛКМ); Берем стеклянную палочку и перемешиваем содержимое в пробирке (нажатие ЛКМ); Поджигаем палочку при помощи зажигалки (нажатие ЛКМ на зажигалку); тлеющая палочка вносится в пробирку для убеждения в выделении кислорода. Написать уравнения реакции разложения пероксида водорода Составить электронно-ионные уравнения полуреакций.5. КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
Исходя из строения атома кислорода, указать его валентность. Какие степени окисления проявляет кислород в соединениях? Привести примеры. Дать характеристику молекулярного кислорода указав химические свойства, строение молекулы, магнитные свойства молекулы. Сколько кислорода в а) литрах (н. у.); б) в граммах; в) в молях необходимо для получения 160 г оксида магния? Исходя из электронного строения атома серы указать, какие валентные состояния и степени окисления характерны для этого элемента. Написать формулы соединений серы, в которых она является: а) только окислителем; б) только восстановителем; в)восстановителем и окислителем. Указать какие свойства проявляет сероводород при взаимодействии с водными растворами KMnO4, H2O2, NaOH. Составить уравнения реакций. Привести пример реакции в которой сера может быть и окислителем и восстановителем. Тип реакции? Написать уравнение реакции сероводорода с сернистым газом и определить, какие объемы их вступили в реакцию (н. у.), если масса образовавшейся серы 0,2 кг? Чем отличается действие концентрированной серной кислоты на металлы от действия разбавленной кислоты? Подтвердить ответ, составив уравнения реакций. Сколько граммов серной кислоты необходимо для растворения 50 г ртути? Сколько из них пойдет на окисление ртути? Можно ли взять для растворения ртути разбавленную серную кислоту?6. ОТЧЕТ
6.1 Форма отчета
Цель работы___________________________________________________
_______________________________________________________________
Название опыта_________________________________________________
Ход работы: (краткий конспект)___________________________________
1._____________________________________________________________
2._____________________________________________________________
3._____________________________________________________________
4._____________________________________________________________
и т. д.__________________________________________________________
Используемые реактивы: (перечислить реактивы, которые используете в опыте_________________________________________________________
________________________________________________________________
1.______________________________________________________________
2.______________________________________________________________
3.______________________________________________________________
4.______________________________________________________________
5.______________________________________________________________
Наблюдения по опыту № 1
________________________________________________________________________________________________________________________________
Наблюдения по опыту № 1_________________________________________
________________________________________________________________
________________________________________________________________
Наблюдения по опыту №3_________________________________________
________________________________________________________________
________________________________________________________________
Химические уравнения____________________________________________
_1.______________________________________________________________2.______________________________________________________________3._____________________________________________________________
Выводы по работе________________________________________________
1.______________________________________________________________
2.______________________________________________________________
Работу выполнил__________________________________________
Отчет принял_____________________________________________
«____»______________20___г.
7. СПИСОК ЛИТЕРАТУРЫ
Общая химия. – М.: ВШ, 2004. – 558с. Общая химия. – Л.: Химия, 2003. – 704с. Севастьянова, Г. К., Карнаухова. химия: Курс лекций. – Тюмень: ТюмГНГУ, 2009. – 212 с.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



