Са2+(водн)+2НСО3-(водн) ↔ СаСО3 (тв) +СО2(г) +Н2О(ж) (7)
Морская вода представляет собой концентрированный и сложный раствор, в котором ионы ближе друг к другу по сравнению с более разбавленными растворами. Между соседними ионами происходят электростатические взаимодействия, что приводит эти ионы в «неактивное» состояние. Мы заинтересованы в доступных или «активных» ионах и делаем поправку на указанный эффект, используя коэффициенты активности [4].
Активная концентрация ионов, или активность, становится важным понятием в концентрированных и сложных растворах типа морской воды. Ионы в концентрированном растворе находятся на достаточно близком расстоянии друг от друга, чтобы между ними происходили электростатические взаимодействия. Эти взаимодействия снижают эффективные концентрации способных участвовать в реакции ионов. Чтобы точно предсказать протекание химических реакций в концентрированных растворах, надо принимать в расчет уменьшение эффективной концентрации, что делается с помощью использования коэффициента активности (у):
Активность = концентрация · у. (8)
Из уравнения (8) видно, что единицы активности и концентрации пропорциональны; другими словами, у можно рассматривать как константу пропорциональности. Такие константы, значение которых изменяется от 0 до 1, можно рассчитать экспериментально или теоретически, и они хорошо известны для некоторых природных растворов. Однако измерение у в сложных растворах типа морской воды оказалось очень трудным. Для наших целей особенно важно, что по мере приближения ионной силы раствора к нулю величина у стремится к 1. Другими словами, в очень разбавленных растворах (например, дождевой воде) активность и концентрация практически равны [4].
Активность выражается в единицах моль • л-1, так же, как и концентрация. Активность обозначается а; результат умножения активностей ионов известен как произведение активностей ионов (ПАИ).
Отметим также, что термодинамические константы равновесия тоже измеряются в единицах активности. Поэтому измеренные концентрации любых химических форм должны быть переведены в активности перед тем, как их сравнивают с термодинамическими данными [4].
Коэффициенты активности крайне трудно измерить в таких сложных растворах, как морская вода, - считается, что они составляют около 0,26 для Са2+ и около 0,20 для карбонат-иона (CO32-). Измеренные концентрации Са2+ и CO32- на поверхности океана равны 0,01 и 0,00029 моль • л-1 соответственно, и таким образом, можно вычислить произведение активностей ионов (ПАИ):
ПАИ = а Са2+∙ а CO32- = 0,01·0,26∙0,00029·0,2 = 1,5∙10-7 моль2 ·л-2 (9)
Это значение намного больше, чем произведение растворимости кальцита (СаСО3), равное 4,5 ∙ 10-9 моль2 • л-2. Степень насыщения равна:
Степень насыщения ї = ПАИ/Кsp (10)
Значение ї, равное 1, означает насыщение, > 1 - пересыщение и < 1 - недонасыщение. Взяв величины для кальцита, приведенные выше, получим:
ї = ![]()
![]()
это означает, что морская вода пересыщена в отношении кальцита [4].
В этом подходе не учитываются эффекты образования ионных пар. Из возможности образования ионных пар следует, что около 90% имеющегося в морской воде кальция присутствует в виде свободных ионов, а оставшаяся часть представлена в ионными парами СSO40 и СаНСО3-. Для CO32- вычислено, что только около 10% существует в виде свободных ионов, а остальная часть присутствует в виде ионных пар с Мg2+, Са2+ и Na+. В результате учета этих поправок значение ПАИ уменьшается следующим образом:
ПАИ = 1,5 · 10-7 · 0,9 ∙0,1 = 1,35 ·10-8 моль2 · л-2 (11)
Теперь, вычислив состояние насыщения, имеем:
ї = ![]()
![]()
Отсюда следует, что поверхностная морская вода пересыщена в отношении кальцита в три раза. Обобщая, можно заключить, что поверхностная морская вода пересыщена в отношении кальцита, и можно ожидать спонтанного осаждения CO32-.
Данные полевых исследований отчасти противоположны предположениям, основанным на химии равновесий. Абиогенное осаждение СаСО3 представляется ограниченным и привязанным к географически и геохимически необычным условиям. Причины того, почему карбонаты неохотно выпадают из морской воды, до сих пор плохо поняты, но, по-видимому, включают в себя ингибирующие эффекты растворенных ионов и соединений. Даже в местах, где предполагается абиогенное выпадение, обычно трудно не принимать в расчет влияние посредничества микроорганизмов в процессе осаждения [3].
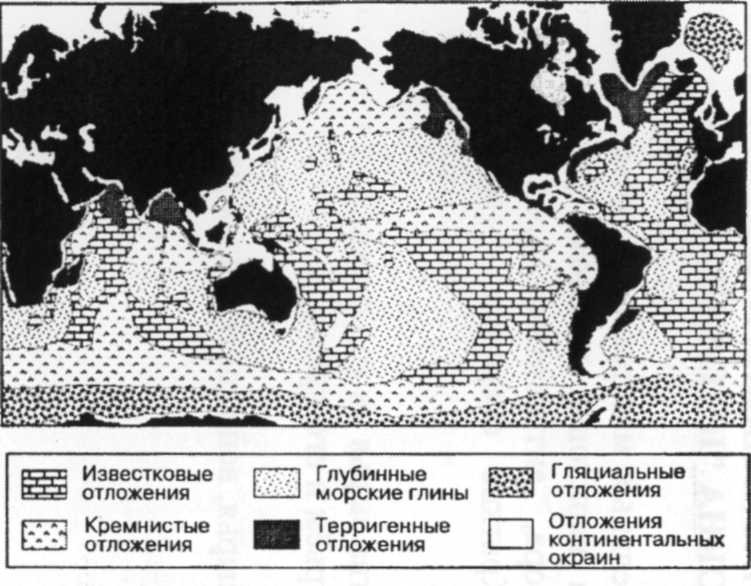
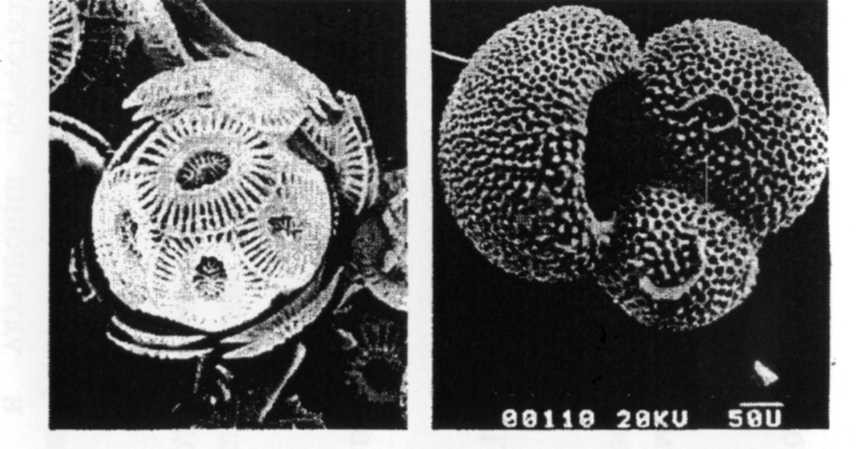
По мощности биологический вынос ионов Са2+ и НСО3-, синтезируемых в скелетах организмов, гораздо более существен. Заманчиво допустить, что такие заметные образования, как большие коралловые рифы тропических и субтропических океанов, и другие «скелетные» карбонаты морских мелководий представляют собой основные участки выноса. В самом деле, вероятно, что большие области континентальных шельфов в современных океанах, образовавшиеся во время поднятия уровня моря в последние 11000 лет, действительно составляют около 45 % глобальных отложений карбонатов. Однако можно показать, что в течение последних 150 миллионов лет скорее отложение карбонатов на глубине океанов было более существенным по объему, составляя между 65 и 80 % глобального поступления карбонатов. Эти глубинные морские отложения, в среднем около 0,5 км по толщине, покрывают примерно половину поверхности глубокого океанического дна (рис. 14). Богатые карбонатами илы состоят из скелетов фитопланктона (кокколитофорид) и зоопланктона (фора-минифер) (рис. 15). Несмотря на то, что эти морские организмы живут в поверхностных водах океанов, после смерти их скелеты опускаются вниз в столбе воды либо сами собой, либо в составе фекальных комочков зоопланктона – пеллетах [4].
К факторам, контролирующим распределение морских илов, частично относится доступность питательных веществ, которых должно быть достаточно для поддержания жизни значительных популяций фитопланктона. Однако более важным является растворение СаСОз по мере осаждения частичек в глубинные океанические воды. В глубинных водах океанов концентрации диоксида углерода (СО2) возрастают в результате разложения осажденного органического вещества. Падение температуры и увеличение давления также способствуют растворению СаСО3, благоприятствуя протеканию обратной
реакции в уравнении (7) [4].
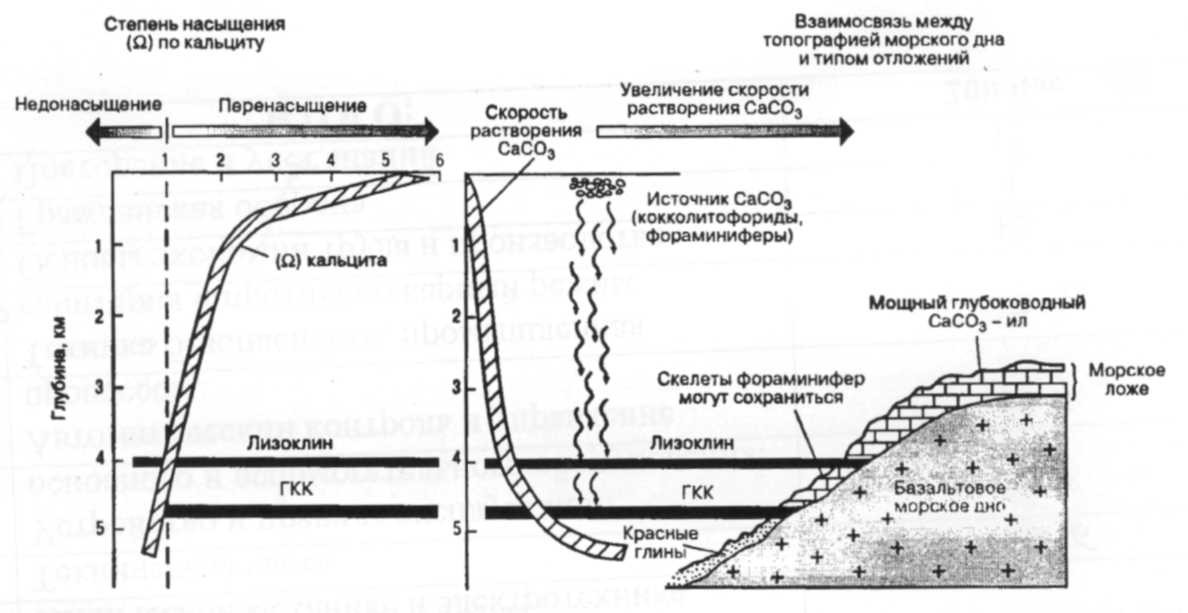
Путем картирования глубин существования карбонатных отложений на дне океанов стало возможным определить уровень, на котором скорость поступления биогенного СО32- уравновешивается скоростью его растворения. Эта глубина, известная как глубина компенсации кальцита (ГКК), различается в океанах Земли и зависит от степени недонасыщения СО32- в глубинных водах (рис. 16). В Атлантическом океане ГКК находится на глубине примерно 4,5 км; выше ГКК в Атлантике на глубине примерно 4 км находится критический уровень, называемый лизо-клином (рис. 16). Здесь скорость растворения кальцита заметно увеличивается и все, за исключением наиболее грубых частичек быстро растворяются. По оценкам, около 80% СаСОз, оседающего в глубинные воды, растворяется либо в процессе транспорта через столб воды, либо на морском дне. Вследствие этого отложения морских карбонатов сильнее распространены на более мелких участках глубинного дна океанов (рис. 16) или на топографических высотах, которые проецируются выше ГКК [4].
2.4.5. Опаловые силикаты
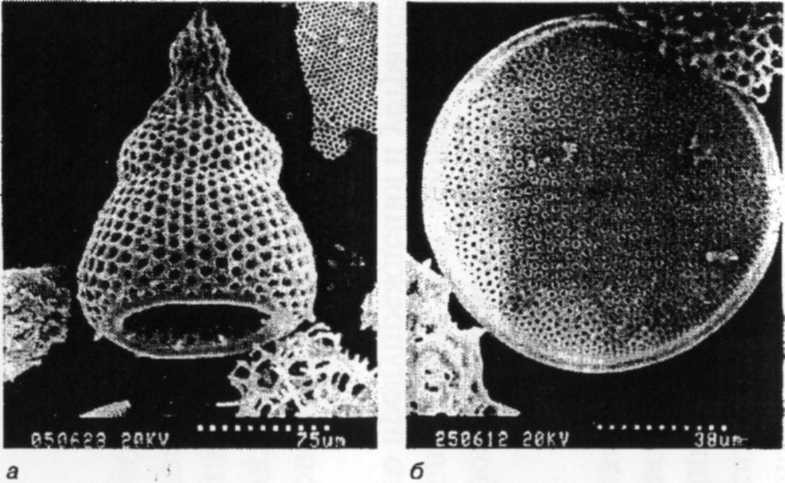
Опаловые силикаты (опал) - это разновидность продуцируемого биологически диоксида кремния (SiO4 • nН2O), выделяемого как скелетный материал морским фитопланктоном (диатомеями) и одной группой морского зоопланктона (радиоляриями) (рис. 17). Богатые опаловыми силикатами (Si04 ∙ nH2O) отложения покрывают около одной трети морского ложа, особенно в областях с высокими скоростями осадконакопления, привязанными к богатым питательными веществами водам восходящих течений, а также полярным морям, особенно вокруг Антарктики (рис. 14). Морская вода недонасыщена в отношении кремния и, по оценкам, 95% опаловых силикатов растворяется по мере погружения вниз по столбу воды или на границе раздела осадок/вода. Таким образом, сохранение опаловых силикатов происходит только там, где
они захораниваются в быстро накапливаемом осадке, ниже поверхности раздела осадок/вода. Последующее растворение опала в осадке приводит к насыщению поровых вод кремнием. Поровые воды не могут быстро перемешиваться с открытыми морскими водами, и насыщение предотвращает дальнейшее растворение опала. Высокие скорости осадконакопления в океанах могут быть вызваны высокими скоростями поступления минералов с континентов, но обычно причиной являются высокие скорости продуцирования их биологическими агентами. В областях с высокой продуктивностью диатомовые водоросли являются распространенным видом фитопланктона, что повышает значение таких областей как стоков для кремния. Биологический вынос кремния (Si) из морской воды рассчитан на основе содержания опала в отложениях и скоростей осадконакопления [3].
2.4.6. Сульфиды
После того как свободный кислород был потреблен, окисление органического вещества протекает с помощью набора микробиологически опосредованных реакций. Несмотря на то, что в морских отложениях небольшие количества нитратов (NO3-), марганца (Мn) и железа (Fe) пригодны как акцепторы электронов, значение их невелико по сравнению с SO42-, которого много в морской воде (табл. 2). При значении рН морской воды около 8 органическое вещество включается сульфатредуцирующими бактериями в обмен веществ [4].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




