Конечный результат заключается в образовании больших анионов, легко растворяющихся вследствие того, что заряд распределен по большому периметру иона. Общий характер растворимости элементов можно объяснить сточки зрения заряда и ионных радиусов (z/r) (рис. 4). Ионы с низкими значениями z/r высокорастворимы, образуют в растворе простые ионы, и ими обогащена фаза раствора речной воды по сравнению с фазой взвеси. Ионы со средними значениями z/r относительно нерастворимы и имеют сравнительно большие отношения частица: раствор в речной воде. Ионы с большими значениями z/r образуют комплексные оксианионы и снова становятся растворимыми [3].
2.1.2. Химия воды и режимы выветривания
Химия рек различна, и большинство различий обусловливается режимами выветривания.
Состав растворенных ионов в пресных водах зависит от:
- варьирующего состава дождевых осадков и сухих атмосферных выпадений;
- изменений в поступлениях в атмосферу вследствие эвапотранспирации;
- варьирующих вкладов от реакций выветривания и разложения органического вещества в почвах и породах и различного вовлечения в биологические процессы в почвах. Там, где присутствуют кристаллические породы или сильно выветрелые тропические почвы (т. е. в местах, где вклад от выветривания низок или исчерпан), химия растворенных веществ в пресных водах в основном зависит от природных поступлений в атмосферу, например, морских брызг и пыли, а также антропогенных газов, например SО2 [3].
Поступления морской соли, обычно называемые, цикличной солью, характерны для прибрежных областей. Небольшие количества морской соли, однако, присутствуют также в речной воде центральных континентальных областей, удаленных на тысячи километров от моря.
Поступления морской соли в целом имеют сходный, в основном натрий хлоридный (NaCl), химический состав с той морской солью, из которой они происходят. Таким образом, ионы натрия или хлора могут быть использованы в качестве меры поступления морских солей в речные воды[3].
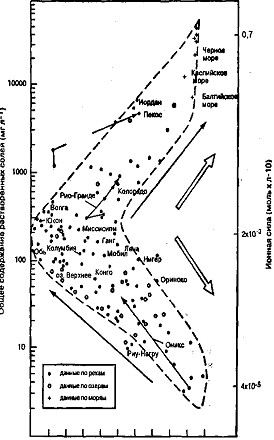
Роль морской воды как источника остальных ионов для дождевой воды можно оценить, рассчитав их относительное содержание по отношению к натрию и сравнив его с таким же отношением в морской воде. Такое сравнение можно распространить и на пресную воду, хотя здесь существует то осложнение, что некоторые ионы попадают в нее при выветривании. Если с самого начала не учитывать этого осложнения, то в областях, где поступления дождевой воды вносят большой вклад в химию пресной, доминирующим катионом, вероятнее всего, будет Na+. Если существенны процессы выветривания, основными растворенными ионами будут те растворимые элементы, которые поступают из местной породы и почвы. В отсутствие минералов-эвапоритов, которые являются второстепенными компонентами континентальной коры (рис.5) наиболее легко выветриваемыми породами являются известняки (СаСО3). Ион кальция, высвобождаемый в процессе растворения известняка, выступает в качестве индикатора такого процесса выветривания. Отсюда отношение Na+ : (Na+ + Са2+) можно использовать для разграничения источников ионов для пресной воды - дождевого и процессов
выветривания. Когда доминирующим катионом является натрий (существен вклад морской соли), значения Na+ : (Na+ + Са2+) приближаются к 1. Когда преобладает кальций (существен вклад процессов выветривания), значения Na+ : (Na+ + Са2+) приближаются к 0 [3].
Состав растворенных ионов в речной воде можно классифицировать, сравнивая значения Na+ : (Na+ + Са2+) с общим количеством ионов, присутствующих в растворе (рис. 5). Данные, представленные внизу справа на рис. 5, относятся к рекам с низкими концентрациями ионов и натрием как преобладающим катионом. Эти реки текут по кристаллической материнской породе (низкие скорости выветривания) или по сильно выветрелым каолинитовым тропическим почвам (низкий потенциал выветривания) [3].
Основные речные системы протекают по разнообразным типам пород, захватывая растворенные продукты реакций выветривания. Пресные воды, происходящие из областей с активными процессами выветривания, имеют наиболее высокие концентрации ионов, в них также увеличивается преобладание кальция над натрием. Эти реки нанесены вдоль направления А-А' на рис. 5 [3].
В аридных районах на химию основных растворенных ионов рек влияет испарение. Испарение увеличивает общее количество ионов в речной воде. Оно также вызывает осаждение из воды СаСО3 раньше, чем NaCl, поскольку последний более растворим. Из-за образования CaCO3 из воды удаляется ион кальция, что увеличивает отношение Na+ : (Na+ + Са2+). Данные для рек, на которые влияет испарение, нанесены вдоль диагонали В-В' на рис. 5, и состав их приближается к составу морской воды [3].
Классификация состава речной воды, приведенная на рис. 5, является упрощенной и не всегда соответствует действительности. Например, в результате выветривания полевых шпатов могут образовываться растворы с низкой ионной силой, но в то же время богатые натрием и кремнием, которые помещаются внизу справа на рис. 5. На состав рек может также влиять выветривание минералов-эвапоритов. Последние имеют очень высокие общие концентрации катионов и характеризуются высокими содержаниями натрия, хлора, кальция и сульфатов из-за выветривания минералов-эвапоритов - галита и гипса. Несмотря на эти отклонения, рис.5 остается удобным для сравнения факторов, контролирующих химию речной воды. Удивительно, что состав большинства крупных рек мира может быть рационально описан таким прямолинейным способом [3].
Наконец, напомним, что большинство почвенных вод, питающих реки и грунтовые воды, имеют околонейтральный рН и HCO3- в виде основного аниона. Это является результатом растворения СО2 в воде и кислотного гидролиза силикатов и карбонатов. Общее количество слабых анионов в воде часто относят к щелочности, и они поддерживают значение рН около 8 [3].
2.1.3. Кремний и алюминий
Кремний мобилизуется при выветривании силикатов и переносится в природных водах в виде недиссоциированной кремниевой кислоты, H4SiO4. Силикаты выветриваются медленно, поэтому скорости поступления (и концентрации) кремния в большинстве пресных вод очень низкие. Несмотря на это, в местах, где силикаты являются основным компонентом подстилающей породы или почвы, H4SiО4 может быть важной составляющей среди растворенных твердых веществ пресных вод [4].
Алюминий как правило не растворяется в процессах выветривания (табл.1), однако становится растворимым при низких и высоких значениях рН. В простейшем случае различаются три формы алюминия: растворимый Аl3+, преобладающий в кислых условиях, нерастворимый гидроксид алюминия [A1(OH)3], преобладающий в нейтральных условиях, и [Al (OH)3], преобладающий в щелочных условиях [4].
Таким образом, растворимость алюминия зависит от рН, он нерастворим в пределах значений рН 5-9, что включает большинство природных вод. Растворимость алюминия осложняется образованием частично диссоциированных форм А1(ОН)3 и комплексов между алюминием и органическим веществом. Понимание контроля за растворимостью алюминия важно, поскольку его токсичность может вызвать гибель рыбы в подкисленных пресных водах [4].
Подкисление пресных вод происходит в том случае, если скорость замещения почвенных катионов водородом (Н+) превышает скорость поступления катионов в результате выветривания. Реакции ионного обмена помогают поддерживать рН короткое время, но для более длительных периодов снабжение почвы катионами осуществляется из нижележащей подстилающей породы. Обычно дождевая вода имеет кислую реакцию, и почвенные воды дополнительно подкисляются из-за образования Н+ в результате разложения органического вещества. Таким образом, подкисление может быть природным процессом, хотя кислотные дожди сильно увеличили скорости этих процессов во многих районах земли [4].
Подкисление пресной воды особенно заметно в горных областях с большим количеством дождевых осадков (и, следовательно, высоким потоком кислоты), на крутых склонах (где результатом является короткое время пребывания воды в почве) и кристаллических породах, где медленны процессы выветривания и снабжения катионами. Несмотря на то, что кислотные дожди являются широко распространенным явлением, подкисленные пресные воды встречаются не так часто и контролируются как скоростью поступления из атмосферы, так и типом пород. В процессе всех реакций выветривания, за исключением окисления сульфидов, потребляются ионы водорода, смещая рН в нейтральную область. Следовательно, древние реки, дренирующие мощные, богатые катионами почвы низин, имеют более высокий рН и более низкие концентрации алюминия [4].
Хотя алюминий растворим при высоких рН, щелочные воды не распространены, поскольку они адсорбируют из атмосферы кислые газы, например С02 и S02. Однако реки с щелочной реакцией и подвижным алюминием известны. Промышленный процесс получения алюминия из боксита включает выщелачивание металла сильными растворами гидроксида натрия (NaOH). Значение рН для химии воды хорошо демонстрируется также процессами загрязнения грунтовых вод [4].
2.1.4. Биологические процессы
В ручьях и небольших реках биологическая активность в воде слабо влияет на ее химический состав, поскольку любые воздействия устраняются из-за быстрого течения. Напротив, в крупных реках и озерах со слабым течением основные изменения в химическом составе воды могут быть вызваны биологической активностью [3].
Все фотосинтезирующие растения поглощают свет и превращают его в химическую энергию с помощью молекулы хлорофилла. Освобождаемая энергия используется затем для превращения СО2 (или HCO3-) и воды в органическое вещество следующим образом:
свет
СН2О(тв) + О2(г) → СО2(г) + Н2О(ж) (3)
СН2О представляет собой обобщенную формулу для углеводного органического вещества. Протекание реакции, обозначенной уравнением, требует притока энергии (∆G° = +475 кДж • моль-1), что обеспечивается светом. В мелких пресных водоемах фотосинтез осуществляют крупные растения и дрейфующие микроскопические водоросли (фитопланктон), в то время как в глубоких озерах (и океанах) практически весь фотосинтез происходит только за счет фитопланктона. В процессе обратной реакции разложения органического вещества, т. е. окисления или дыхания, высвобождается энергия, которая поддерживает жизнь:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




