Степень выноса питательного вещества, которая может иметь место в дельте, проиллюстрирована для силикатов SiО2 (рис. 12). Здесь существует ряд параметров, значения которых свидетельствуют о роли фитопланктона в удалении питательных веществ. В основном удаление силикатов связано с
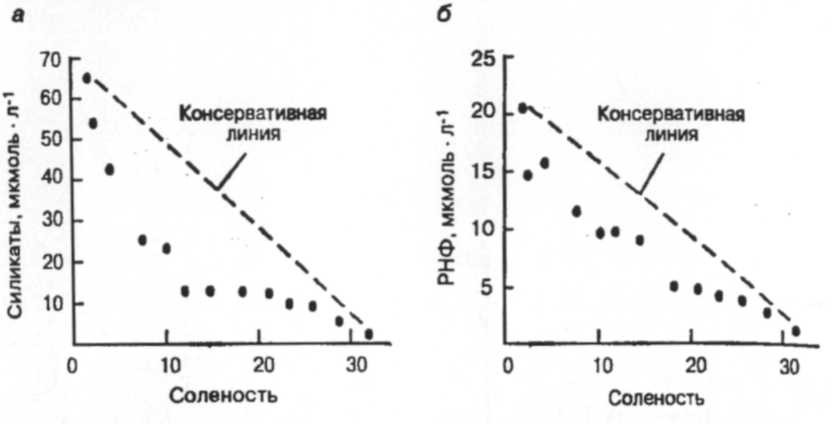
высокими концентрациями хлорофилла во взвешенных частицах, перенасыщением кислородом (возникающим в результате фотосинтеза) и выносом других питательных веществ. В зимний период, когда уровни хлорофилла низки и содержание кислорода падает до более низких уровней, удаление силикатов прекращается [3].
Процесс, в результате которого накапливаются отложения в дельтах, приводит к накоплению также частиц органического вещества. Если в дельте присутствуют большие количества его, скорости потребления кислорода вследствие аэробного процесса потребления органического вещества бактериями могут превысить скорость поступления кислорода. В результате уменьшаются концентрации растворенного кислорода.
Сброс сточных вод из городов часто приводит к низким или нулевым концентрациям растворенного кислорода [3].
2.3. Химия главных ионов в морской воде
Изучив химию среды в дельтах, обратимся теперь к глобальным химическим циклам в открытом океане. Начнем с положения, что химия основных ионов в морской воде отлична от химии поверхностных вод континентов (табл. 2). Существуют три основных свойства, отражающих это отличие [4].
Высокая ионная сила морской воды (рис. 5), которая содержит около 35 г · л-1 солей; Химический состав морской воды, с высоким содержанием Na+ и Сl - (табл.2); Удивительно постоянные относительные концентрации основных ионов морской воды во всех океанах Земли.Последнее свойство хорошо иллюстрируют данные, показывающие, что отношение К+ : Cl--, измеренное в океанических областях от Ледовитого океана до Черного моря, практически неизменно в пределах аналитических ошибок 0,0205 ± 0,0007 [4].
В океанах ионы бикарбоната (НСО3-) и Са2+ включены в биологический круговорот, приводящий к вертикальному градиенту их отношений по сравнению с другими основными ионами. Однако различия в отношениях невелики - менее 1 % для кальция. Существуют также данные, что состав основных ионов в морской воде изменялся лишь незначительно в течение многих миллионов лет, поэтому предполагается, что состав океанов контролируется очень долговременным геохимическим круговоротом [4].
Свидетельства о том, что соленость и ионный состав морской воды оставались примерно постоянными в течение по крайней мере последних 900 миллионов лет, были получены на основе изучения древних отложений морских эвапоритов. Эвапориты - это соли, которые выпали природным путем из испаряющейся морской воды в бассейнах, по большей части отрезанных от открытого океана.
В течение последних 900 миллионов лет морские эвапориты обычно идут в последовательности от секции гипс-ангидрит (CaSO4·2H2O-CaSO4 к галиту (NaCl). Горькие соли (названные так из-за их горького вкуса) выпадают на последних стадиях испарения и имеют варьирующий состав, включая магниевые соли, бромиды, хлорид калия (KCl) и более сложные соли, в зависимости от условий испарения (рис. 13) [4].
Порядок выпавших соединений такой же, какой наблюдается в современных морских звапоритах, и его можно воспроизвести опытным испарением морской воды. Эта последовательность осаждения солей устанавливает пределы возможных изменений в составе главных ионов в морской воде, поскольку изменения вне этих пределов имели бы результатом другие последовательности осаждения [4].
Рис.13. Последовательный ряд и приблизительные мощности слоев солей, осаждающихся при испарении 1 км морской воды
Ряд простых наблюдений дает некоторое представление о возможных изменениях. Например, удвоение концентрации иона кальция (Са2+) при существующей в настоящее время концентрации сульфат-иона (SO42-) не окажет влияния на последовательность осаждения, тогда как утроение концентрации Са2+ уже сделает это. Аналогично, уменьшение или увеличение вдвое существующей в настоящее время концентрации иона калия (К+) повлечет за собой образование некоторых очень необычных горьких солей, не наблюдаемых до сих пор в геологической летописи [3].
Представления об изменениях концентраций иона натрия (Na+) и хлора (Cl-) основаны на ископаемых отложениях галита. Общий объем известных отложений галита достигает около 30% от содержания NaCl в современных океанах. Если всю эту соль добавить в существующие океаны, соленость морской воды увеличилась бы примерно на 30%, что устанавливает верхний предел. Однако основные отложения галита достаточно хорошо распределяются по геологическому времени, и можно предположить, что никогда не было такого периода, чтобы все эти ионы были растворены в морской воде [4].
2.4. Химический круговорот главных ионов
Времена пребывания главных ионов в морской воде являются важным индикатором того пути, по которому происходит химический круговорот в океанах. Все эти времена пребывания очень продолжительны (от 104 до 108 лет) и близки или превышают значения для самой воды (3,8 • 104 лет). Длительные времена пребывания означают, что у океанских течений существует реальная возможность тщательного перемешивания воды и составляющих ее ионов. Это обеспечивает сглаживание изменений в отношениях ионов, возникающих в результате локальных процессов привноса или выноса. Именно большие времена пребывания ионов создают высокое постоянство ионных отношений в морской воде. Времена пребывания являются результатом высокой растворимости ионов и, следовательно, их отношений z/r. Остальные катионы с похожими отношениями также имеют длительные времена пребывания. (например, ион цезия (Cs2+), но они не относятся к главным в морской воде из-за их низкого содержания в земной коре. Интересным исключением является хлор. Его много в морской воде, у него большое время пребывания и тем не менее низкое содержание в земной коре. Большая часть этого С1- дегазировалась из мантии Земли в виде хлористого водорода (НС1) в очень ранний период истории Земли и с тех пор включена в круговорот эвапориты-гидросфера [4].
Более длительные времена пребывания у главных ионов, чем у воды, приводят к тому, что морская вода является более концентрированным раствором, чем речная. Однако различные ионные отношения в морской и речной воде указывают на то, что океаны - это не просто результат наполнения речной водой океанических бассейнов, даже если бы образовавшийся раствор был сконцентрирован путем испарения. Несмотря на то, что у всех главных ионов времена пребывания велики, они различаются более чем на четыре порядка по величине, показывая, что скорости выноса отдельных ионов различны. Поэтому должны действовать процессы, отличные от концентрирования путем испарения [4].
2.4.1. Потоки море - воздух
Потоки море - воздух у главных ионов вызваны разрывами пузырей и ударами волн на поверхности моря. В результате этих процессов морские соли выбрасываются в атмосферу, но основная их часть немедленно падает обратно в море. Некоторые соли, однако, переносятся в атмосфере на большие расстояния и вносят вклад в содержание солей в речной воде. Считается, что эти переносимые по воздуху морские соли имеют такой же относительный ионный состав, что и морская вода. С точки зрения глобальных запасов переносимые по воздуху морские соли являются важным стоком из морской воды только для Na+ и С1- [4].
2.4.2. Эвапориты
Испарение воды способствует осаждению составляющих ее солей, так называемых эвапоритных минералов, в последовательности, которую можно предсказать. Эта последовательность начинается с наименее растворимых солей и заканчивается наиболее растворимыми. Когда испарилась примерно половина (47 %) объема воды, выпадает СаСОз. В процессе последующего испарения и приблизительно четырехкратного увеличения солености выпадает CaSО4 ·2Н2О (гипс):
Са2+(водн)+SO42-(водн)+2Н2О(ж)↔ CaSО4 ·2Н2О(тв) (5)
Когда испарилось около 90% воды (Н2О), при концентрациях растворенных солей около 220 г · л-1, выпадает NaCl:
Na+(водн) + Cl-(водн) ↔ NaCl(тв) (6)
и, кроме того, начинают кристаллизоваться некоторые соли магния (Mg2+); если процессе испарения продолжается, выпадают высокорастворимые соли калия (К+).
Проблема с признанием испарения как процесса удаления ионов из морской воды заключается в том, что в настоящий момент существует очень немного сред, в которых минералы эвапоритов накапливаются в значительных количествах. Причина этого в том, что должны испариться огромные количества морской воды, прежде чем соли сконцентрируются настолько, чтобы начать осаждаться. Ясно, что это не может происходить в хорошо перемешанных открытых океанах, где чистая потеря воды в результате испарения примерно уравновешивается ее поступлением с континентальными поверхностными водами (речным притоком). Это означает, что концентрирование морской воды результате испарения может происходить только в областях аридного климата в бассейнах, большей частью изолированных от открытого океана и других источников поступления воды[4].
2.4.3. Катионный обмен
В процессе катионного обмена на глинистых минералах, перемещающихся из речной воды в морскую, удаляется около 26% от речного притока Na+ в океаны и существенны процессы удаления К+ и Мg2+. Глинистые минералы служат также заметным источником Са2+ в океаны, добавляя лишние 8% к притоку с реками. Однако эти временные значения вдвое больше долговременных величин из-за влияния необычайно высоких скоростей послеледникового привноса взвешенного твердого материала [4].
2.4.4. Осаждение карбонатов
Сложно точно рассчитать, когда морская вода пересыщена или близка к насыщению относительно СаСО3. Существует несколько подходов к решению проблемы, но все они основаны на следующем равновесном отношении, которое описывает осаждение (прямая реакция) или растворение (обратная реакция) СаСО3:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




