Этот процесс широко распространен в морских отложениях, но особенно важен в осадках на границе континентов, где накопление органического вещества наибольшее. Восстановление сульфатов протекает на такой глубине (изменяющейся от нескольких миллиметров до метров ниже границы раздела осадок/вода), где морской SO42- может быстро диффундировать или накачиваться организмами, обитающими в отложениях. В результате реакции образуется сульфид водорода (HS-), обладающий высокой реакционной способностью, большая часть которого диффундирует вверх и снова окисляется до SO42- кислородсодержащей морской водой на поверхности осадка. Однако около 10% HS - быстро осаждает растворимый Fe (II) в восстанавливающихся осадках, что приводит к накоплению моносульфида железа [4].
С течением времени моносульфиды железа превращаются в пирит (FeS2); процесс превращения изучен плохо, но, по-видимому, включает поступление серы (S) от промежуточных серосодержащих форм (например, полисульфидов, политионатов или тиосульфата), являющихся продуктами и реагентами в цикле востановления серы в микронишах.
Сульфит (SO32-) затем окисляется до SO42-. Осажденный пирит, образующийся как побочный продукт восстановления сульфатов в морских осадках, является главным стоком морского SO42-. Наличие пирита в древних морских отложениях показывает, что восстановление SО42- происходит уже сотни миллионов лет. В масштабе геологического времени вынос SО42- из морской воды в результате образования отложений пирита считается практически равным выносу его в результате осаждения эвапоритов.
В результате восстановления сульфатов образуется также HCO3- и этот анион медленно диффундирует из осадка в морскую воду, составляя около 7% от потока в океаны. Медленная диффузия означает также, что анион может накапливаться до настолько высоких концентраций в поровых водах осадков, что произведение активностей ионов Са2+ (из морской воды) и аниона превышает произведение растворимости СаСО3 [уравнение (10)]. Это приводит к выпадению СаСОз в осадке в виде ксенолитов (конкреций) [4].
2.4.7. Баланс запасов главных ионов морской воды
Запасы главных ионов в морской воде достаточно хорошо сбалансированы (т. е. приход равен расходу) для всех элементов, за исключением К+. Неопределенное количество К+, по-видимому, потребляется в процессе низкотемпературных реакций между базальтом и морской водой в дополнение к ионообменным реакциям, в результате которых может удаляться до 17% от современного потока К+ с реками. Дисбаланс в запасах К+, а также небольшие дисбалансы в запасах других элементов можно свести к нулю с помощью набора реакций, вероятно, протекающих между морской водой и океаническими отложениями [3].
Одна из возможностей - это «обратные реакции выветривания». При обратном выветривании сильно разрушенные глинистые минералы взаимодействуют с катионами, HCO3- и силикатами морской воды с образованием сложных, подобных глинистым минералам, силикатов. Примером реакции, касающейся проблемы К+, может быть следующая:
Разрушенный + К+(водн) + HCO3- (водн) +Н4SiО4(водн) →К + СО2(г) +Н2О(ж) (13)
алюмосиликат(тв) алюмосиликат(тв)
Из этой реакции видно, что обратное выветривание является строго противоположным реакциям выветривания на суше, в процессе которых потребляется СО2 и высвобождается HCO3-.
Другим процессом, который может вносить небольшой вклад в запасы К+, является фиксация К+ на глинистых минералах в результате реакций ионного обмена. В лабораторных экспериментах показано, что разрушенные слюды и иллиты, лишенные своего К+ в процессе выветривания, но сохранившие большую часть заряда слоя, способны необратимо фиксировать К+ из морской воды. Процесс включает в себя замещение гидратированных катионов в межслоевых пространствах дегидратированным К+, приводя к фиксации К+ на тех участках, на которых он расположен в слюдах. В общем, в этом процессе может удаляться около 10 % от речного потока К+ в океаны [3].
Некоторый вынос ионов из морской воды происходит в результате постоянного захоронения их в поровой воде отложений. Общий вынос главных ионов в этом процессе невелик и составляет менее 2 % от речного привноса для всех элементов, за исключением Na+ и С1-. Вынос в результате захоронения может быть значительным для Na+ и С1- (20-30 % от притока с реками), однако эти данные не точны [34.
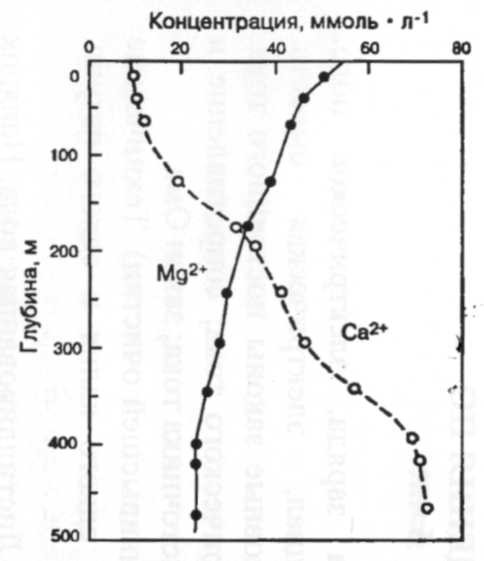
Морская вода, захороненная в морских отложениях, может взаимодействовать с их компонентами, особенно с тонкозернистым базальтовым вулканическим пеплом. Концентрации Са2+, Mg2+ и К+ в поровых водах морской коры на большой глубине свидетельствуют о выносе Mg2+ (и в меньшей степени К+) при зеркальном увеличении концентрации Са2+ в поровой воде (рис.18). На основе этих результатов можно предположить, что базальтовый пепел превращается в Mg2+- и К+-содержашие глинистые минералы одновременно с высвобождением Са2+ в поровые воды. Количественная значимость этого механизма в глобальном масштабе, вероятно, мала, однако хорошие данные редки [4].
2.4.8. Антропогенное воздействие на главные ионы
Последним затруднением, связанным с запасами главных ионов в морской воде, является то, что при их оценке рассматривается речной привнос в морскую воду природного происхождения. Антропогенные процессы могут изменять некоторые из этих потоков. Например, в результате человеческой деятельности поток переносимого рекой С1- может увеличиться более чем на 40% , а поток SO42- - удвоиться в основном из-за сжигания ископаемого топлива и окисления H2S, возникшего в результате загрязнения[3].
Человеческая деятельность влияет также на объем твердого стока, переносимого реками. Вырубка лесов и увеличившаяся сельскохозяйственная деятельность по всему миру делают поверхность земли более доступной эрозии. Влияние их на химию главных ионов морской воды заключается в основном в увеличившемся привносе твердого детрита на континентальные шельфы, что приводит к увеличению процессов ионного обмена и других взаимодействий твердое вещество - морская вода. Однако эта ситуация все еще изменчива; увеличение использования речных плотин снижает привнос осадков в океаны в настоящее время. Менее важным со стороны глобальных запасов, но существенным с экологической точки зрения является увеличение количества твердого стока в тропических реках, попадающего с детритом в меловые коралловые рифы береговых вод и приводящее к падению биологической продуктивности в результате снижения чистоты воды [3].
Заключение
Вода в своих трех состояниях - жидкость, лед и водяные пары - широко распространена на поверхности Земли и занимает объем 1,4 млрд. км3. Почти вся эта вода (> 97 %) находится в океанах, а большая часть из оставшейся образует полярные ледяные шапки и ледники (около 2 %). Континентальные пресные воды представляют менее 1 % общего объема, в основном это подземные воды (глубинные - 0,38 %, поверхностные - 0,30 %; озера - 0,01 %, почвенная влага - 0,005 %, реки -0,0001 %, биосфера - 0,00004%). Атмосфера содержит сравнительно мало воды (в виде паров) (0,001 %). В целом эти резервуары воды называют гидросферой [5].
Источник воды при образовании гидросферы неясен. Некоторые метеориты содержат до 20 % воды в связанных гидроксильных (ОН-) группах, в то же время бомбардирование прото-Земли кометами, обогащенными водяными парами, представляет другой возможный источник. Как бы это ни происходило, но когда поверхность Земли остыла до 100°С, водяные пары, дегазирующиеся из мантии, могли сконденсироваться. По существованию погруженных в воду осадочных пород известно, что океаны образовались около 3,8 • 109 лет назад [5].
Очень малое количество водяных паров проникает из атмосферы в космос, поскольку на высоте около 15 км низкие температуры вызывают их конденсацию и выпадание на более низкие уровни. Очень небольшое количество воды дегазируется в настоящее время из мантии. Исходя из этих наблюдений, можно предположить, что после основной фазы дегазации общий объем воды на земной поверхности мало изменялся в течение геологического времени [5].
Круговорот между резервуарами воды в гидросфере называется гидрологическим циклом. Хотя объем водяных паров, содержащихся в атмосфере, мал (около 0,013 · 106 км3), вода постоянно движется через этот резервуар. Она испаряется с поверхности океанов (0,423 ∙ 106 км3/год) и суши (0,073 • 106 км3 год) и переносится с воздушными массами (0,037 • 10б км3/год). Несмотря на короткое время пребывания в атмосфере (обычно 10 дней), среднее расстояние водопереноса составляет около 1000 км. Водяные пары затем возвращаются либо в океаны (0,386 • 106 км3/год), либо на континенты (0,110 • 10б км3/год) в виде снега или дождя. Большая часть дождевых осадков, попадающих на континенты, просачивается через отложения и пористые или раздробленные породы, образуя подземные воды (9,5 · 10б км3); остальная вода течет по поверхности в виде рек (0,13 • 106 км3) или вновь испаряется в атмосферу. Поскольку общее количество воды в гидросфере постоянно во времени, процессы испарения и осаждения должны быть сбалансированы для Земли в целом, несмотря на большие локальные различия между гумидными и аридными регионами [5].
Быстрый перенос воды в атмосфере обусловливается поступающим солнечным излучением. Почти все излучение, достигающее коры, идет на испарение жидкой воды и образование атмосферных водяных паров. Энергия, используемая для этого преобразования, которая затем содержится в парах, называется скрытой теплотой испарения. Большая часть из оставшегося излучения поглощается корой, причем эффективность этого процесса уменьшается с увеличением широты, в основном из-за сферической формы Земли. Солнечные лучи нагревают поверхность Земли под углом 90° на экваторе, но с увеличением широты под все меньшими углами, приближаясь к 0° на полюсах. Таким образом, одинаковое количество излучения распространяется на большие площади в высоких широтах по сравнению с экватором. Изменение с широтой количества поступающего излучения не сбалансировано противоположным явлением излучения с поверхности Земли, таким образом, результатом является общий радиационный дисбаланс. Однако полюса не становятся все более холодными, а экватор - теплее, поскольку тепло перемещается в направлении полюсов с теплыми океаническими течениями, а также существует направленное к полюсам движение теплого воздуха и скрытой теплоты испарения водяных паров [5].
Список использованных источников
Эдельштейн, материков: учеб. пособие/. – М.: Издательский дом «Академия», 2005. – 304 с. ISBN 5-7695-2176-7
Давыдов, гидрология:учеб./ , , /под ред. и . – Л.: Гидрометеоиздат, 1993. – 455 с.: ил. ISBN 5-56-075-8
Андруз, Дж. Введение в химию окружающей среды: [пер. с англ.]/ Дж. Андруз [и др.]. – М.: Мир, 1999. – 271 с., ил. ISBN 5-03-003289-4
Никаноров, : учеб./. - Л.: Гидрометеоиздат, 1989. – 348 с.: ил. ISBN 5-286-00138-6
Голдовская, окружающей среды:учеб./. – М.: Мир, 2005. – 296 с.: ил. ISBN 5-03-003649-0

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




