2. Каков физический смысл константы химического равновесия? От каких факторов она зависит?
3. Сформулируйте общий принцип смещения равновесия (принцип Ле Шателье).
4. Напишите выражение для константы химического равновесия для следующих обратимых процессов:
2NO2 « 2NO + O2 FeO(тв) + H2(г) « Fe(тв) + H2O (пар)
СаСО3 (тв) « СаО (тв) + СО2 С(тв) + Н2О (пар) « Н2(г)+ СО(г)
5. В какую сторону сместится равновесие при:
- увеличении давления;
- увеличении объема системы;
- повышении температуры в следующих обратимых реакциях:
2SO2 + O2 « 2SO3 DH = -196 кДж
Н2 + Br2 « 2HBr DH = -73,2 кДж
2N2 + O2 « 2N2О DН = +163 кДж
II. Лабораторная работа
«Смещение химического равновесия при изменении концентрации реагирующих веществ»
Цель работы
Определить направление смещения химического равновесия при изменении концентрации исходных и конечных веществ.
Сущность методики
Реакция протекает по уравнению:
FeCl3 + 3KSCN Û Fe(SCN)3 + 3 KCl
Образующийся в реакции роданид железа (III) окрашен в красный цвет, интенсивность окраски зависит от его концентрации. Смещение равновесия наблюдают по изменению интенсивности окраски раствора.
ПРИБОРЫ И РЕАКТИВЫ
Штатив с пробирками, насыщенные растворы FeCl3 и KSCN (или NH4SCN), кристаллический KCl.
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
В пробирку налейте 2-3 капли FeCl3 и 1-2 капли KSCN. Полученный раствор разбавьте дистиллированной водой до 3/4 пробирки, перемешайте и разлейте в 4 пробирки. В 1-ю пробирку добавьте 3 капли раствора FeCl3 , во 2-ю - 3 капли раствора KSCN, в 3-ю - немного кристаллического KCl, а 4-ю - оставьте для сравнения. Отметьте изменение интенсивности окраски раствора в каждой из 3-х пробирок по сравнению с 4-й и наблюдения запишите в таблицу.
Добавленное вещество | Изменение интенсивности окраски | Направление смещения равновесия |
Обсуждение результатов
1. В таблице отметьте направление смещения равновесия в каждом из рассмотренных случаев.
2. Напишите выражение константы равновесия для данной реакции.
3. Объясните направление смещения равновесия в каждом случае на основании:
а) изменения скорости прямой и обратной реакции;
б) постоянства величины константы равновесия;
в) принципа Ле-Шателье.
4. Сделайте общий вывод о влиянии концентраций исходных веществ и продуктов реакции на направление смещения равновесия.
5. Ответьте на вопросы:
а) добавление, какого из реагирующих веществ приводит к наибольшему изменению окраски раствора и почему?
б) изменились ли равновесные концентрации реагентов при смещении равновесия?
в) изменение, каких внешних условий может привести к изменению величины константы равновесия в рассмотренной системе?
выполнения работы
В 3 пробирки налейте по 1 мл раствора NaCl разной концентрации, согласно таблице. В каждую пробирку внесите по 1 капле крови, встряхните и оставьте на 5-10 мин.
Опишите в таблице наблюдаемые различия.
№ пробирки | Растворы NaCI | Кровь | Внеш-ний эффект | ||
Концентрация,% | Объем, мл | Вид раствора | |||
1 | 0,2 | 1 | Гипотонический | 1 капля | |
2 | 0,9 | 1 | 1 капля | ||
3 | 4,0 | 1 | 1 капля |
Обсуждение полученных результатов
1. Нарисуйте схему осмоса, происходящего в каждом из трех растворов.
2. Объясните, что происходит с эритроцитом в каждом растворе.
3. К какому случаю относится термин «лаковая кровь»?
4. Сделайте вывод.
ТЕМА: «РАСТВОРЫ ЭЛЕКТРОЛИТОВ. СИЛЬНЫЕ И СЛАБЫЕ ЭЛЕКТРОЛИТЫ. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ.
ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ, рН»
ЗНАЧЕНИЕ ТЕМЫ
От присутствия электролитов в организме зависит величина осмотического давления, возникновение биопотенциалов, протекание окислительно-восстановительных реакций, кислотность физиологических жидкостей, они предохраняют организм от обезвоживания.
I. Выполните упражнения (САРС)
1. Для следующих электролитов: CuCl2, Ba(OH)2, KHS, H2SO3, MgOHCl напишите уравнения диссоциации
2. Из приведенных кислот назовите сильные и напишите для них уравнение диссоциации:
HCN, HNO3, H2S, HNO2, HCl, H2CO3, HClO4.
3. - Что такое константа кислотности?
- Используя значения Ка для приведенных ниже кислот укажите, какая кислота диссоциирует лучше (какая кислота сильнее).
- Напишите для нее уравнение диссоциации и выражение Ка.
- азотистая кислота и циановодородная (синильная) кислота;
- уксусная кислота и фтороводородная (плавиковая) кислота;
4. Что такое рКа? Используя значение рКа, укажите, какая кислота сильнее:
- уксусная кислота и хлоруксусная кислота (рКа = 2,9);
- муравьиная кислота (рКа = 3,74) и уксусная кислота;
5. Как влияет на диссоциацию угольной кислоты добавление:
а) HCl б) NаОН
6. Вычислите концентрацию ионов водорода в водном растворе, если концентрация гидроксид-ионов равна:
а) 10-4 моль/л б) 3,2 ´ 10-6 моль/л.
7. Вычислите рН растворов, в которых концентрация ионов водорода равна:
а) 10-2 моль/л; б) 4,6 ´ 10-4 моль/л; в) 9,3 ´ 10-10 моль/л
Укажите характер среды.
8. Кислотность желудочного сока равна 0,047 моль/л. Рассчитайте его рН.
9. Яблочный сок имеет рН = 3,76. Вычислите концентрацию ионов водорода в нем.
10. Вычислите концентрацию ионов Н+ в плазме крови здорового человека (рН = 7,40) и больного ацидозом (рН = 7,30).
11. Рассчитайте концентрацию ионов ОН - в артериальной крови (рН = 7,36).
II Лабораторная работа.
«Водородный показатель среды, рН»
Цель работы
1. Научиться определять рН растворов индикаторным и потенциометрическим методами:
а) индикаторными: - с помощью растворов индикаторов;
- с помощью универсального индикатора;
б) потенциометрическим: - с помощью рН-метра (иономера).
2.Оценить возможности каждого метода.
СУЩНОСТЬ МЕТОДИКИ.
рН раствора можно измерять либо индикаторным, либо ионометрическим (потенциометрическим) методами.
Индикаторный метод основан на использовании кислотно-основных индикаторов – веществ, изменяющих свою окраску в зависимости от рН раствора. Такие индикаторы – это слабые органические кислоты (или основания), у которых окраска нейтральной и заряженной формы различна, а диссоциация протекает по уравнению:
HInd « H+ + Ind-
Нейтральная Заряженная
форма рН = рКа форма
окраска 1 переходная окраска 2
окраска
По принципу Ле Шателье, изменение концентрации ионов Н+ (изменение рН) смещает равновесие процесса диссоциации индикатора в сторону той или иной формы. Для каждого индикатора эта зависимость от рН определяется величиной его константы диссоциации (Ка или рКа). При рН = рКа концентрации молекулярной и ионной формы одинаковы.
Промежуток между двумя значениями рН, в котором происходит различимое глазом изменение окраски его раствора, называется интервалом перехода окраски индикатора.
Интервалы перехода ОКРАСКИ
КИСЛоТНО-ОСНОВНЫХ индикаторов
Индикатор | Окраска В кислой среде | Окраска В щелочной среде | Интервал перехода индикатора |
Метилоранж | Красная | Желтая | 3,1 - 4,4 |
Метилрот | Красная | Желтая | 4,2 - 6,2 |
Лакмус | Красная | Синяя | 5,0 - 8,0 |
Фенолфталеин | Бесцветная | Малиновая | 8,3 - 10,0 |
С помощью данного индикатора количественно оценить величину рН можно только в его области перехода. В других случаях возможна лишь качественная оценка характера среды – кислая (рН<7) или щелочная (рН>7).
Часто для приближенного определения рН используют так называемый универсальный индикатор - в виде раствора или в виде пропитанных им бумажек. Универсальный индикатор представляет собой смесь нескольких простых индикаторов (состав приводится в справочниках и некоторых учебниках), подобранных так, чтобы окраска ее изменилась в широком интервале значения рН (например, от 1 до 10). С помощью универсального индикатора можно определить рН с точностью до одной единицы рН.. Особенно удобной в практике является универсальная индикаторная бумага, к которой прилагается цветная шкала, показывающая, какие окраски соответствуют различным значениям рН.. Наиболее точно рН можно определить с помощью потенциометрического метода (до 0,01 ед. рН).
ОБОРУДОВАНИЕ И РЕАКТИВЫ
Штатив с пробирками, растворы индикаторов: метиловый оранжевый, лакмус, фенолфталеин, универсальная индикаторная бумага, иономер, стандартные растворы с известным значением рН (рН = 2, 4, 6, 9, 12), биологические жидкости: желудочный сок, желчь в склянках с пипеткой.
Опыт 1. Исследование зависимости окраски кислотно-основных индикаторов от рН растворов
Из имеющихся растворов с известными значениями рН необходимо выбрать для каждого индикатора три раствора так, чтобы рН двух из них соответствовал значениям до и после интервала перехода окраски индикатора, а рН третьего должен лежать в пределах этого интервала.
Налейте в 3 пробирки по 1 мл раствора и добавьте по 1-2 капли индикатора, окраску растворов запишите в таблицу.
Сделайте вывод о том, какие значения рН можно достаточно точно определить с помощью растворов: индикаторов.
Индикатор | № раствора | рН | Окраска раствора |
Метиловый оранжевый | 1 | ||
2 | |||
3 | |||
Лакмус | 1 | ||
2 | |||
3 | |||
Фенолфталеин | 1 | ||
2 | |||
3 |
Опыт 2. Определение рН биологических жидкостей с помощью универсального индикатора.
С помощью пипетки нанесите каплю исследуемой жидкости на полоску универсальной индикаторной бумаги.
Сравните окраску влажного участка бумаги с колориметрической шкалой рН.
Определите рН исследуемого раствора и запишите его значение.
Рассчитайте концентрацию ионов Н+ в литре каждой из биологических жидкостей (желудочный сок, желчь, слюна).
Опыт 3. Определение рН биологических жидкостей с помощью рН-метра
Перед началом работы убедитесь, что электроды погружены в стаканчик с водой примерно на 1,5 см.
- включите прибор в сеть, загорается индикаторная лампочка;
- установите переключатель «род работы» в положение «рН», а переключатель «размах» в положение 15;
- дайте прибору прогреться 15 минут.
- исследуемый раствор налейте в чистый стаканчик;
- замените стаканчик с водой на стаканчик с исследуемым раствором, соблюдая ту же глубину погружения электродов;
- после остановки стрелки прибора определите значение рН по нижней шкале с точностью до 0,1 единицы рН.
Для более точного определения рН
- необходимо установить переключатель «размах» в положение «3», а переключатель «диапазон измерений» в положение, соответствующее измеренному значению рН (например, измеренное значение рН = 5,2, переключатель «диапазон измерений» устанавливается в положение 4¸9);
- после установления стрелки по верхней шкале в соответствии с выбранным диапазоном измерений определите точное значение рН с точностью до 0,01 единицы рН..
ВЫВОДЫ ПО ОПЫТАМ 2 И 3.
1. Сделайте вывод о характере среды в каждой жидкости.
2. Какова точность каждого метода?
3. Объясните, в чем преимущества применения
- универсального индикатора перед растворами индикаторов;
- рН-метра.
ТЕМА: «БУФЕРНЫЕ РАСТВОРЫ».
ЗНАЧЕНИЕ ТЕМЫ:
Буферные системы в организме поддерживают кислотно-основное равновесие, то есть постоянное соотношение концентраций Н+-ионов и ОН-ионов, от которого зависит протекание ферментативных биохимических реакций.
I. Выполните упражнения (САРС)
1. В воду пробулькивали газообразный SО2. Какое вещество надо добавить к образовавшемуся водному раствору, чтобы получить буферный раствор? Напишите его состав и механизм буферного действия.
2. Вычислите рН ацетатной буферной системы, полученной смешением 200 мл раствора ацетата натрия с молярной концентрацией 0,4 моль/л и 500 мл уксусной кислоты с концентрацией 0,1 моль/л. Какая буферная емкость: кислотная или основная выше в этом растворе?
3. Аммиачный буферный раствор получен смешиванием 500 мл 0,2 М раствора NH4ОН и 200 мл 0,4 М раствора NH4Cl.
- Какая среда в этом растворе: кислая или щелочная?
- Рассчитайте значение рН.
- Какая буферная емкость выше – кислотная или основная?
4. Угольная кислота существует только в растворе за счет растворения углекислого газа. Ее концентрацию можно выразить через парциальное давление углекислого газа (рСО2) и коэффициент растворимости СО2 в жидких средах (S).
[H2CO3] = pCO2 ´ S
Тогда формула для расчета значения рН гидрокарбонатной системы имеет вид:
рН = рКа + lg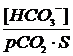 или рН = 6,1 + lg
или рН = 6,1 + lg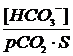
Рассчитайте рН гидрокарбонатной буферной системы, если рСО2 = 40 мм. рт. ст, S = 0,03, а концентрация гидрокарбонат-иона равна 2,4´10-2 моль/л.
5. В водных растворах a-аминокислоты, в зависимости от рН среды, существуют в виде: катиона, нейтральной биполярной молекулы и аниона. На примере аминокислоты глицин (Н2N-СН2-СООН) составьте кислотную и основную буферные системы и запишите механизм их буферного действия.
6. Рассчитайте величину кислотной буферной емкости, если при добавлении
4 мл 0,5 н раствора Н2SО4 к 50 мл буферного раствора, его рН изменился от
4,2 до 3,5.
II. Лабораторная работа.
«Приготовление буферных растворов, исследование их свойств и определение буферной емкости»
ЦЕЛЬ РАБОТЫ
1. Приготовить буферные растворы с определенным значением рН и изучить их свойства.
2. Рассчитать значение рН приготовленных буферных растворов и сравнить полученные значения с экспериментальными.
3. Определить буферную емкость по кислоте приготовленных буферных систем.
ПРИБОТЫ И РЕАКТИВЫ
рН-метр, стаканчики для измерения рН – 2 шт., бюретки, пипетки, цилиндр на 25 мл, колбы для приготовления и разбавления растворов. Исходные растворы:
уксусная кислота, С = 0,2 моль/л
натрий ацетат, С = 0,2 моль/л
соляная кислота, С = 0,1 моль/л
Опыт 1. Приготовление буферного раствора. Изучение влияния разбавления на его свойства.
1. Приготовьте три ацетатных буферных раствора объемом по 40 мл с соотношением:
Раствор | CH3COOH | CH3CONa | Vк, мл | Vc, мл |
1 | 1 | 3 | ||
2 | 1 | 1 | ||
3 | 3 | 1 |
Эти растворы в дальнейшем считайте концентрированными.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



