2. Отмерьте мерной пробиркой или цилиндром 10 мл раствора, вылейте его в стаканчик для измерения рН и прибавьте к нему 20 мл Н2О. Получим разбавленный раствор: Vконц = 30 мл Vразб = 30 мл
3.Измерьте величину рН приготовленных растворов концентрированных и разбавленных (рНэкс.) и результаты занесите в таблицу.
№ буферного раствора | I | II | III | Дист вода | |||
Состав буферного раствора Кислота: соль | 1:3 | 1:1 | 3:1 | ||||
конц. | Разб. | конц. | Разб. | конц. | разб. | ||
1.рНтеор. | |||||||
2.рНэксп. | |||||||
3.Добавление HCl (0,1 н) рНэксп. к | |||||||
4.DРн | |||||||
5.Вкисл. |
Опыт 2. Исследование влияния добавления сильной кислоты к буферному раствору. Определение буферной емкости по кислоте (Вк).
1.Добавьте:
к 30 мл концентрированного буферного раствора 2 мл HCl;
к 30 мл разбавленного буферного раствора 1 мл HCl.
Измерьте величину рН этих растворов (рНэксп. к), значение запишите в таблицу.
2.Для сравнения возьмите 30 мл дистиллированной воды и измерьте величину рН до и после добавления к ней 1 мл HCl.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ И ВЫВОДЫ
1.Рассчитайте и внесите в таблицу:
- значения рН приготовленных буферных растворов (рНтеор.)
- отклонения рН, вызванные добавлением кислоты:
DрН = |pHэксп. к – рКэксп.|;
- величину кислотной буферной емкости.
2.В выводе отметьте:
- что сделано в работе?
- от чего зависит рН раствора и как зависит?
- о влиянии разбавления на величину рН;
- что такое кислотная буферная емкость?
- от чего зависит кислотная буферная емкость? Как зависит?
ТЕМА «ГЕТЕРОГЕННЫЕ РАВНОВЕСИЯ И ПРОЦЕССЫ.
УСЛОВИЯ ОБРАЗОВАНИЯ И РАСТВОРЕНИЯ ОСАДКОВ
В РАСТВОРАХ МАЛОРАСТВОРИМЫХ ЭЛЕКТРОЛИТОВ»
ЗНАЧЕНИЕ ТЕМЫ
Произведение растворимости – одно из важнейших понятий, которые количественно характеризуют состояние равновесия в гетерогенных системах, т. е. процессы, протекающие с образованием труднорастворимых соединений. Подобные процессы имеют место и в живых организмах, например, образование нерастворимых соединений (камней) приводит к возникновению желчекаменной или почечнокаменной болезни. Лечение их может быть более эффективным с привлечением теории гетерогенных равновесий.
I. Выполните упражнения (САРС)
1. Имеется три стакана, содержащих системы:
а) вода + сахар б) вода + NaCl в) вода + АgCl
- В каком из них может установиться гетерогенное равновесие? Изобразите его схематично.
- Какую из систем можно охарактеризовать константой растворимости КS (ПР)? Напишите ее выражение.
2. Пользуясь величинами ПР, определите, какой осадитель лучше выбрать: (NH4)2SO4, (NH4)2CO3 или (NH4)2C2O4 (оксалат), чтобы наиболее полно осадить из раствора ион Са2+?
ПРCaSO![]() = 6,3 ´10-5 ПРСаСО
= 6,3 ´10-5 ПРСаСО![]() = 4,8 ´ 10-9 ПРСаС
= 4,8 ´ 10-9 ПРСаС![]() = 2,6 ´ 109.
= 2,6 ´ 109.
3. Напишите математическое выражение ПР для сульфата кальция; гидроксида алюминия; карбоната свинца(II); фосфата свинца(II); сульфида серебра.
4. Приготовлены насыщенные водные растворы солей: СаSО4, SrSО4 и ВаSО4 (Т = const). Объясните, в растворе, какой соли молярная концентрация катионов будет выше.
ПРВаSO![]() = 1,1 ´ 10-10 ПРSrSO
= 1,1 ´ 10-10 ПРSrSO![]() = 1,6 ´ 10-9 ПРСаSO
= 1,6 ´ 10-9 ПРСаSO![]() = 6,1 ´ 10-5
= 6,1 ´ 10-5
Условия образования осадка
Осадок труднорастворимого электролита образуется при химических реакциях только тогда, когда произведение концентраций его ионов превысит величину константы растворимости этого соединения, т. е. в пресыщенном растворе. [А+] . [В-] > ПРАВ |
5. Выясните, образуется ли осадок АgCl, если к 5 мл 0,1 М раствора АgNO3 прибавить 5 мл 0,05 М раствора HCl.
ПРAgCl = 1,6 ´ 10-10.
6. ПРСаСО = 4,8 ´ 10-9. Выпадет ли осадок при сливании равных объемов 0,05 М раствора Са(NО3)2 и 0,001 M раствора (NН4)2СО3?
= 4,8 ´ 10-9. Выпадет ли осадок при сливании равных объемов 0,05 М раствора Са(NО3)2 и 0,001 M раствора (NН4)2СО3?
Растворение осадка
Например: растворение гидроксида магния под действием соляной кислоты: (осадок) Мg(ОН)2 « Mg2+ + 2OH- (раствор) добавление 2НСl « 2Сl - + 2Н+ 2Н2О – слабый электролит |
7. Объясните причину растворения оксалата кальция СаС2О4 в соляной кислоте.
8. Почему сульфат бария не растворяется в соляной кислоте желудка при рентгенологических исследованиях?
9. Объясните причину растворения Fе(ОН)3 в соляной кислоте.
ТЕМА: « КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ».
ЗНАЧЕНИЕ ТЕМЫ
Комплексные соединения играют большую роль в процессах жизнедеятельности. В живых организмах присутствуют комплексные соединения многих биогенных металлов с белками, витаминами и другими веществами, играющими роль ферментов и выполняющими специфические функции в обмене веществ. Комплексные соединения применяют в качестве лекарственных средств. На комплексообразовании основано выведение токсических веществ. Комплексообразование используют для консервации донорской крови и т. д.
I. Выполните упражнения (САРС)
1. Для приведенных комплексных соединений (КС):
1) [Cr(NH3)4(NO2)2]Cl; 2) [Ni(CO)5]; 3) NH4[Pb(H2O)(NO2)3].
- укажите внутреннюю и внешнюю сферы;
- напишите уравнение первичной диссоциации;
- охарактеризуйте состав внутренней сферы по плану:
а) заряд внутренней сферы и тип комплексной частицы по этому заряду;
б) комплексообразователь и его степень окисления;
в) лиганды и их заряд;
г) координационное число;
- назовите КС.
2. Напишите формулы КС:
1) тринитротриамминкобальт; 2) бромид гексаамминосмия (III);
3) бромотринитроплатинат (II) калия.
3. Напишите уравнения первичной и вторичной диссоциации КС и выражения для их констант нестойкости:
1) [Cr(H2O)6](NO3)3; 2) Ca3[Co(CN)6]2.
4. Выпишите из таблицы значения констант нестойкости следующих комплексов и укажите, какой из них наиболее устойчив:
1) [Cd(CN)4]2-; 2) [Cu(CN)4]2-; 3) [Ni (CN)4]2-; 4) [Zn(CN)4]2-.
5. Напишите структурную формулу хелатного комплекса Cu2+ с глицерином.
6. Напишите уравнения реакций образования комплексных соединений:
1) [Ni(NH3)4]Cl2; 2) K2[HgI4]; 3) H2[SnCl6].
7. При взаимодействии раствора [Cu(NH3)4]Cl2 с раствором KCN образуется соль K2[Cu(CN)4]. Напишите уравнение реакции и объясните причину ее протекания.
II. Лабораторная работа.
«Получение комплексных соединений и изучение их устойчивости»
ЦЕЛЬ РАБОТЫ
1. Получить комплексные соединения.
2. Изучить условия образования и разрушения КС.
ПРИБОРЫ И РЕАКТИВЫ
Пробирки
Растворы: сульфата никеля (II), гидроксида аммония, серной кислоты.
Получение комплексного соединения никеля и его разрушение
а) К 1 мл раствора сульфата никеля (II) в пробирке добавьте по каплям концентрированный раствор аммиака. Наблюдайте выпадение осадка основной соли (NiOH)2SO4. Добавьте к нему избыток аммиака. Что наблюдается?
х у
Изобразите схему происходящих превращений А ¾® В ¾® С, учитывая, что в аммиачном комплексе к. ч.(Ni2+) = 6. Укажите изменение окраски.
б) Добавьте к полученному раствору по каплям раствор серной кислоты. Как изменяется окраска раствора? Напишите уравнение реакции в ионном виде и объясните причину разрушения аммиачного комплекса Ni(II) под действием кислоты, используя для этого значения Кн.
Напишите формулы комплексных соединений, укажите их состав, приведите уравнения первичной и вторичной диссоциации, выражение Кн и название комплексных солей.
В выводе укажите условия образования и разрушения комплексных соединений.
ТЕМА: «ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ПРОЦЕССЫ».
ЗНАЧЕНИЕ ТЕМЫ
Окислительно-восстановительные реакции относятся к самому распространенному типу реакций и играют исключительно важную роль в жизнедеятельности организмов. С ними связано окисление питательных веществ в организме, усвоение некоторых лекарственных препаратов, эти реакции используются при синтезе и аналитическом испытании фармпрепаратов и санитарно-гигиенической практике и антисептике.
I. Выполните упражнения (САРС)
1. Укажите, какие процессы происходят при переходах: окисление или восстановление.
СО ® СО2 О2 ® Н2О2 NО2- ® NO
Br2 ®2HBr HNO3 ® HNO2 SO42- ® SO32-
2. Из перечисленных частиц составьте сопряженные ОВ пары:
Cu2+, H+, Cu+, H2, J2, H-, J-
3. Пользуясь значениями ОВ потенциалов, определите, какие частицы являются более сильными:
а) окислителями: Br2 и J2. б) восстановителями: К и Сu.
4. Имеются две взаимодействующие ОВ-пары. Укажите:
- окислитель;
- восстановитель;
- величину ЭДС;
- составьте уравнение ОВ-реакции в ионном виде.
а) Fe3+ + e ® Fe2+ j0 = +0,77 В
Br2 + 2e ® 2Br - j0 = +1,09 В
б) ClO - + 2H+ + 2e ® Cl - + H2O j0 = +1,49 В
Sn4+ + 2e ® Sn2+ j0 = +0,13 В
5. Для приведенных ОВ реакций:
- определите элементы, изменяющие степень окисления;
- выпишите из таблицы сопряженные ОВ пары и значения их ОВ потенциалов;
- укажите окислитель и восстановитель;
- рассчитайте величину ЭДС;
- определите направление ОВ реакции.
1) SnCl4 + FeCl2«SnCl2 + FeCl3
2) HCl + H2SO4 « Cl2 + H2SO3 + H2O
3) K2S + KMnO4 + H2SO4 « S + MnSO4 + K2SO4 + H2O
6. С помощью, каких из перечисленных восстановителей: KJ, H2S, H2, можно восстановить олово (IV) в олово (II)?
II. Лабораторная работа.
«Изучение факторов, влияющих на направление и глубину протекания окислительно-восстановительных реакций»
ЦЕЛЬ РАБОТЫ
Изучить окислительно-восстановительные свойства веществ, встречающихся в медицинской практике, и влияние условий на протекание ОВ-реакций.
ОБОРУДОВАНИЕ И РЕАКТИВЫ
Штатив с коническими пробирками, растворы: серной кислоты (2н), гидроксида натрия или калия (2н), перманганата калия (0.05н), сульфита натрия или калия (0.5н), иодида калия (0.5н), пероксида водорода (3%-ый); крахмальный клейстер.
Опыт 1. Влияние среды на протекание окислительно-восстановительных процессов
Взаимодействие перманганата калия с сульфитом натрия
В три пробирки внесите по 3-4 капли раствора KMnO4. В одну пробирку добавьте 2-3 капли 2н. раствора серной кислоты, во вторую - столько же воды, в третью - такое же количество раствора щелочи. Во все три пробирки внесите по каплям свежеприготовленный раствор Na2SO3. Наблюдайте изменение окраски растворов, учитывая, что в растворe MnO4--ион - фиолетового цвета; Mn2+ - бесцветен; MnO2 - темно-коричневый осадок; MnO42- - зеленого цвета.
Опыт 2. Окислительно-восстановительная двойственность некоторых соединений
Окисление и восстановление пероксидом водорода
В одну пробирку налейте 1 мл раствора KMnO4, 1 мл 2н раствора серной кислоты и по каплям прибавьте Н2О2 до обесцвечивания раствора. Наблюдайте выделение пузырьков газа.
В другую пробирку налейте 1 мл раствора КI, 1 мл 2н. раствора серной кислоты и по каплям прибавьте Н2О2. Для обнаружения свободного иода добавьте 0,5 мл крахмала.
Вариант оформления протокола:
1. Название и цель работы.
2. В опытах 1 и 2 заполните схемы, в которых укажите: окислитель и восстановитель, характер среды, окраску раствора до и после реакции и продукт, за счет которого произошло это изменение окраски:
H2SO4 Окраска раствора Продукт реакции
|
| ||
 | |||

![]()
![]() + H2O
+ H2O
|

3. Составьте уравнения реакций, выписав из справочных таблиц полуреакции и значения j°, учитывая характер среды.
4. В выводе к опыту 1 укажите:
а) почему KMnO4 может быть только окислителем, в какой среде его окислительные свойства наибольшие и почему?
б) для каких целей в медицине применяют перманганат калия и в каких условиях его лучше всего использовать?
5. В выводе к опыту 2 ответьте на вопросы:
а) почему Н2О2 способен проявлять ОВ-двойственность?
б) в каких реакциях Н2О2 является окислителем, а в каких – восстановителем?
Для написания уравнений ОВ реакций можно воспользоваться следующими значениями потенциалов сопряженных ОВ пар:
MnO4- + e ® MnO42- MnO4- + 2H2O + 3e ® MnO2 + 4OH - MnO4- + 8H+ + 5e ® Mn2+ + 4H2O SO42- + 2H+ + 2e ® SO32- + H2O SO42- + H2O + 2e ® SO32- + 2OH - H2O2 + 2H+ + 2e ® 2H2O O2 + 2H+ + 2e ® H2O2 J2 + 2e ® 2J- | j0 = 0,56 В j0 = 0,60 В j0 = 1,51 В j0 = 0,17 В j0 = -0,75 В j0 = 1,78 В j0 = 0,68 В j0 = 0,54 В |
ТЕМА: «ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ. АДСОРБЦИЯ»
ЗНАЧЕНИЕ ТЕМЫ.
Адсорбция – одно из поверхностных явлений, протекающих на межфазной поверхности самопроизвольно и уменьшающих избыточную поверхностную энергию. Примерами адсорбции в биологических системах, имеющих огромные межфазные поверхности, являются: избирательная адсорбция токсинов различными тканями, избирательная адсорбция антител на поверхности чужеродных белков – антигенов (явление иммунитета), изменение скорости оседания эритроцитов – СОЭ – при патологических процессах, участие желчных кислот – ПАВ – в процессе пищеварения и др.
В медицине на явлениях адсорбции основаны детоксикационная терапия – гемосорбция, лечение желудочно-кишечных отравлений и метеоризма активированным углем (карболеном), использование противогаза, получение детского питания из коровьего молока (ионообменная адсорбция), хроматография в клиническом анализе и др.
I Выполните упражнения (САРС)
1. Запишите определение: какие гетерогенные системы называют дисперсными. Приведите 5 примеров дисперсных систем.
2. При дроблении камня образуется пыль. Куда «исчезла» затраченная на дробление энергия?
3. Рассчитайте величину избыточной поверхностной энергии эритроцитов, содержащихся в крови взрослого человека, если известно, что их суммарная площадь поверхности составляет 3000 м2, а поверхностное натяжение эритроцита равно 1,5·10-3 Дж/м2
Система «Г - Ж»
4. 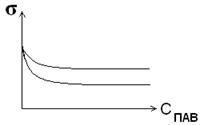 На графике приведены изотермы поверхностного натяжения водных растворов двух повехностно-активных веществ: пентанола-1 и гексанола-1:
На графике приведены изотермы поверхностного натяжения водных растворов двух повехностно-активных веществ: пентанола-1 и гексанола-1:
- покажите на графике σ Н2О.
- как влияют ПАВ на поверхностное натяжение растворителя?
- приведите схематично изображение структуры молекулы ПАВ.
- изобразите частокол Лэнгмюра, образовавшийся в этой системе.
- подпишите, какому веществу соответствует каждая изотерма, согласно правилу Дюкло-Траубе.
5. Используя уравнение Гиббса, рассчитайте адсорбцию желчи из ее водного раствора (Г, моль/м2) и постройте изотерму адсорбции по следующим данным (Т = 298 К):
Сравновесная, моль/л | 0,10 | 0,30 | 0,50 | 0,50 |
Поверхностная активность ∆σ/∆C·10-3Дж/м2 | -82 | -53 | -35 | -26 |
Сформулируйте закономерность: как влияет концентрация ПАВ в растворе на адсорбцию его в поверхностном слое жидкости?
Система «Г - Т»
6. Приведите примеры сорбентов, применяемых в медицине.
7. При изучении адсорбции аммиака на активированном угле при 20°С и 40°С получили следующие изотермы адсорбции:
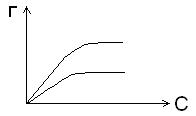 - укажите Г∞ для каждого случая. Что это означает?
- укажите Г∞ для каждого случая. Что это означает?
- подпишите, какой температуре соответствует каждая изотерма.
- сформулируйте, как зависит адсорбция газа от температуры и почему.
- что произойдет, если уголь с адсобированным на нем газом нагреть до 70°С?
8.  При пропускании воздуха через слой медных опилок на их поверхности образовался оксид меди (II): Cu + 1/2O2 CuO
При пропускании воздуха через слой медных опилок на их поверхности образовался оксид меди (II): Cu + 1/2O2 CuO
- какой вид адсорбции: физическая или хемосорбция, имеет место для кислорода и азота, входящих в состав воздуха?
- что произойдет, если адсорбцию проводить при 70°С?
9. Для чего в коробки с обувью кладут пакетики с силикагелем?
Система «Ж - Т»
молекулярная адсорбция
10. Укажите полярности приведенных адсорбентов и жидкостей:
адсорбент растворитель
1. оксид алюминия а. вода
2. уголь б. бензол
3. полиэтилен в. спирт
4. стекло г. гексан
Изобразите взаимодействие (смачивание, несмачивание) спирта с поверхностью активированного угля.
11. Приведите формулировку правила Ребиндера для молекулярной адсорбции. Используя это правило и соответствующие схемы, подберите адсорбенты (из приведенных в задании 10):
а) для осветления растительного масла;
б) для очистки спирта от сивушных масел.
12. В раствор уксусной кислоты с концентрацией 0,1 моль/л поместили 0,5 г порошка активированного угля и оставили на 30 мин. Как экспериментально можно обнаружить её адсорбцию на твёрдом адсорбенте?
ионная адсорбция
13. В смесь электролитов: хлорид натрия и иодида калия, между которыми не происходит химической реакции, поместили кристаллик малорастворимого иодида серебра. Используя правило Панета-Фаянса для избирательной ионной адсорбции, определите:
- какие ионы будут адсорбироваться на поверхности кристалла (являются потенциалообразующими)?
- как заряжается поверхность при их адсорбции?
14. К раствору хлорида кальция добавляют раствор соды – карбоната натрия. Какой электролит следует взять в избытке, чтобы поверхность образовавшегося осадка карбоната кальция стала заряженной отрицательно за счёт адсорбции потенциалообразующих ионов?
15. ![]()
![]()
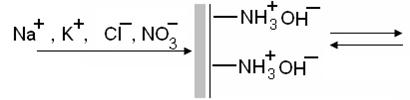 Водный раствор, содержащий смесь ионов: Na+, K+, Cl, NO3 пропускали черз колонку, заполненную гранулами адсорбента-ионита, приведенного на схеме:
Водный раствор, содержащий смесь ионов: Na+, K+, Cl, NO3 пропускали черз колонку, заполненную гранулами адсорбента-ионита, приведенного на схеме:
- приведите вид системы после адсорбции;
- какой это вид ионита: катионит или анионит?
16. Содержание ионов Ca2+ можно определить методом ионного обмена. Для этого водный раствор, содержащий ионы Ca2+, пропускают через колонку с ионитом в Н+-форме.
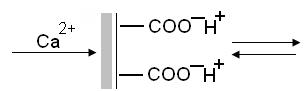
- допишите схему ионного обмена.
- какой это вид ионита?
- чем надо оттитровать жидкость, вытекающую из колонки, чтобы затем рассчитать количество Ca2+ в исследуемом растворе?
ЛАБОРАТОРНАЯ РАБОТА
«Изучение адсорбции органического красителя фуксина из раствора»
ЦЕЛЬ РАБОТЫ:
1.Ознакомиться с процессом адсорбции красителя на активированном угле.
ВЫПОЛНЕНИЕ РАБОТЫ:
В пробирку с 5 мл водного раствора красителя фуксина (какого он цвета?) добавьте шпателем небольшое количество активированного угля, закрытую пробкой пробирку встряхните и содержимое её профильтруйте. Отметьте окраску фильтрата. На ту же воронку с фильтром, содержащим активированный уголь с адсорбированным фуксином, вылейте несколько миллилитров ацетона. Что вы наблюдаете? Объясните.
В ВЫВОДе ОТМЕТЬТЕ:
1. Что сделано в работе (по пунктам, см. заголовок и цель работы)?
2. К какому виду адсорбции относится адсорбция красителя на активированному угле?
ТЕМА: «КОЛЛОИДНЫЕ СИСТЕМЫ»
ЗНАЧЕНИЕ ТЕМЫ:
Система приобретает коллоидные свойства, когда хотя бы одно из измерений частицы находится в области дисперсности м. В организме – это клеточные мембраны, нервные и мышечные волокна, гены, вирусы. Сложнейшей коллоидной системой является кровь, в которую входят золи фосфата кальция, холестерина, билирубина, уратов, жиров, фосфолипидов; газовые эмульсии О2, N2, СО2; суспензии форменных элементов крови – эритроцитов, тромбоцитов, лейкоцитов и др. Будущему врачу необходимо знать свойства коллоидных систем при освоении клинических дисциплин.
I Выполните упражнения (САРС)
1. Напишите формулу мицеллы золя, полученного по реакции хлорида бария с карбонатом калия в избытке ВаСl2.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



