2. Золь бромида серебра получен при смешении 20 мл раствора нитрата серебра с концентрацией 0,008 моль/л и 30 мл раствора НВr концентрации 0,006 моль/л. К какому электроду будет перемещаться гранула при электрофорезе?
3. Напишите формулу мицеллы положительно заряженного золя сульфида цинка, полученного по реакции хлорида цинка и сульфида натрия. Какой реактив взят в избытке?
4. Напишите мицеллу золя, полученного при взаимодействии хлорида бария и сульфата натрия. Какой из электролитов взят в избытке, если при электрофорезе гранулы перемещаются к аноду.
5. Золь получен добавлением 10 мл 0,001 н раствора NH4CNS к 20 мл 0,0003 н раствора AgNO3. Какой ион будет вызывать коагуляцию этого золя при добавлении к нему раствора СаСl2.
6. Золь карбоната магния был получен по реакции сульфата магния с содой, в избытке сульфата магния. Напишите формулу мицеллы. Какие из электролитов: KCl, Fe2(SO4)3, СаСl2, AlCl3, Na3PO4, будут иметь пороги коагуляции для полученного золя: а) одинаковые; б) разные; в) наименьший.
7. Коагуляция 15 мл золя гексацианоферрата (II) меди (II) наступила при добавлении к нему 3 мл 0,002 н раствора Na2SO4. Рассчитайте порог коагуляции этого электролита по формуле: Ск = 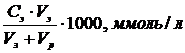 .
.
8. Золь AgI образовался при смешении KI и AgNO3. Для него пороги коагуляции электролитов, С(ммоль/л): Са(NO3)2 = 315; NaCl = 300; AlCl3 = 330. Определите, какой знак заряда имеет гранула. Какой из электролитов KI или AgNO3 взят в избытке? Напишите формулу мицеллы.
9. Золь кремниевой кислоты был получен при действии на силикат натрия соляной кислоты. Пороги коагуляции электролитов (ммоль/л) для данного золя оказались равны: для NaCl 51,0; для MgCl2 0,717; для AlCl3 0,093. Определите знак заряда гранулы (правила Шульце-Гарди) и напишите формулу мицеллы золя.
10. Золи каких веществ: гидроксида железа (III), кремниевой кислоты, бромида серебра (положительный золь), иодида серебра (отрицательный золь) следует смешать, чтобы произошла взаимная коагуляция?
ЛАБОРАТОРНАЯ РАБОТА
«Получение коллоидных растворов и изучение их свойств»
ЦЕЛЬ РАБОТЫ:
1. Получить коллоидные растворы методом химической конденсации.
2. Определить знак заряда золя (гранулы) капиллярным методом.
Опыт 1. Получение золя берлинской лазури
В двух пробирках получите коллоидные растворы берлинской лазури, смешивая:
1 пробирка: 2 мл 2% раствора K4[Fe(CN)6] и при встряхивании 2 мл 0,1% раствора FeCl3;
2 пробирка: 2 мл 2% раствора FeCl3 и 1 мл 0,1% раствора K4[Fe(CN)6].
ПРИМЕЧАНИЕ: полученные растворы оставьте для следующего опыта.
Опыт 2. Определение знака заряда золей (гранул) капиллярным методом
На листок фильтровальной бумаги нанесите каплю исследуемого золя или красителя. После всасывания капли положительно заряженные золи и основные красители дают окрашенное в центре и бесцветное по краям пятно; отрицательно заряженные золи и кислые красители дают равномерно до краев окрашенное пятно. Объясняется это явление тем, что отрицательно заряженная по отношению к воде бумага адсорбирует положительные частицы и не адсорбирует отрицательные. Определите знак заряда частиц золей гидроксида железа (III) и берлинской лазури.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ И ВЫВОДЫ К ОПЫТАМ 1 и 2:
1. Отметьте внешний вид и окраски золей, полученных в опыте 1.
2. Нарисуйте или приклейте листочки фильтровальной бумаги и укажите знак заряда гранулы каждого из золей.
3. Сравните знаки заряда гранул, определенные экспериментально в опыте 2, с теоретическими из формул мицелл.
4. В выводах укажите, каким методом получены коллоидные растворы.
5. Объясните, почему в опыте 1 из одних и тех же веществ получены два разных золя берлинской лазури.
биохимии и клинической биохимии для постановки диагноза и контроля за лечением.
ПОТЕНЦИОМЕТРИЯ
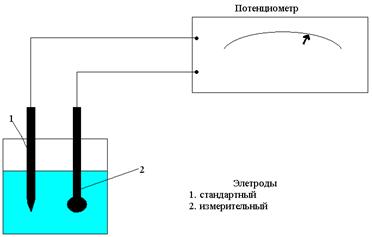
Потенциометрия – это электрохимический метод анализа, основанный на измерении ЭДС гальванического элемента, составленного из двух электродов, один из которых, называемый стандартным, имеет постоянный потенциал, а у второго электрода – измерительного, потенциал изменяется в зависимости от концентрации анализируемого иона (например, Н+). Таким образом ЭДС гальванического элемента зависит только от концентрации анализируемого иона. При рН-метрии шкала сразу отградуирована в единицах рН.
Для определения величины рН обычно используют в качестве стандартного (вспомогательного) электрода – хлор-серебряный электрод, а в качестве измерительного – стеклянный электрод.
Потенциометрическое титрование – это титриметрический метод анализа, в котором точка эквивалентности определяется с помощью прибора, по изменению (в ходе титрования) ЭДС гальванической цепи, содержащей анализируемый раствор.
При потенциометрическом титровании оба электрода погружены в титруемый раствор. Изменение концентрации анализируемого иона сопровождается изменением потенциала измерительного электрода. около точки эквивалентности происходит скачок потенциала, который фиксируется прибором. Следовательно, измерительный электрод служит индикатором титрования и называется также индикаторным.
ЛАБОРАТОРНАЯ РАБОТА
«Потенциометрическое титрование»
ЦЕЛЬ РАБОТЫ:
1. Определить точную концентрацию раствора соляной кислоты методом потенциометрического титрования стандартным раствором щелочи.
2. Построить интегральную и дифференциальную кривые титрования.
3. По кривым титрования определить эквивалентный объём щёлочи и рассчитать концентрацию кислоты в растворе.
Определение концентрации кислоты в растворе потенциометрическим титрованием основано на титровании раствора кислоты стандартным раствором щелочи и определении изменения рН раствора в процессе титрования. При этом протекает реакция:
Н+ + ОН - ® Н2О (для сильной кислоты)
СН3СООН + ОН - ® СН3СОО - + Н2О (для слабой кислоты)
Порядок работы
1. В стакан для титрования отмерьте мерной пипеткой 20 мл исследуемого раствора кислоты.
2. Поставьте стакан на столик датчика и погрузите в раствор электроды на глубину не менее, чем на 2 см.
3. Подготовьте к работе бюретку по всем правилам, заполнив ее стандартным раствором щелочи. Установите носик бюретки таким образом, чтобы он был направлен в стакан, не касаясь электродов и раствора.
4. Измерьте значение рН исходного раствора с помощью прибора. Для этого
а). Включите прибор, нажав клавишу «ВКЛ». Войдите в режим «рН-метр-иономер».
б) Нажмите клавишу «ТК» Появится надпись «ввод температуры (ручной хх. х или автомат). Кнопками◄► установите «Ручной».
в) Нажмите клавишу «ИЗМ», а затем «ТК». Для возврата в прежний режим, нажать кнопку «ОТМ».
г).При дальнейшем измерении пользоваться только кнопками «ИЗМ» и «ТК».
5.Добавляйте из бюретки титрант порциями по 0,2 мл. После каждого добавления титранта раствор в стаканчики перемешивайте, осторожно двигая стакан вокруг электрода. Снимите показания прибора и запишите значение рН в таблицу.
В процессе титрования вначале изменение рН происходит медленно, потом наступает резкое изменение рН (скачок рН), которое снова сменяется плавным изменением рН. После того, как изменение рН снова стало замедленным, титрование заканчите (еще 3 – 4 измерения).
По окончании титрования электроды промыть дистиллированной водой и погрузить в раствор хлорида калия, нажать клавишу «ОТКЛ».
ФОРМА ОТЧЕТА
(предполагается запись 10-15 измерений)
Таблица. Результаты титрования
VNaOH | DV | рH | DpH | DpH/DV |
Здесь VNaOH – объем прибавленного стандартного раствора щелочи;
DV – изменение объема NaOH (между двумя ближайшими измерениями);
рН – измеренное значение рН;
DpH – изменение рН между соседними измерениями.
По результатам титрования постройте интегральную кривую в координатах рН - VNaOH. Для точного определения точки эквивалентности начертите дифференциальную кривую титрования в координатах DpH/DV - VNaOH.
Точка, соответствующая максимуму на дифференциальной кривой, является точкой эквивалентности. По положению этой точки определите эквивалентный объем стандартного раствора щелочи, пошедшей на нейтрализацию кислоты.
Расчет проводят по закону эквивалентов:
![]()
Сн(к)×V(к) = Сн(щ) × Vщ
где Сн(к) и V(к) – концентрация и объем раствора кислоты, моль/л и мл;
Сн(щ) и Vщ – концентрация и объем раствора щелочи, моль/л и мл.
В выводе укажите:
1. Что сделано в работе.
2. Условия анализа (прибор «рН-метр - иономер «Эксперт-001-03»», температура раствора, концентрация стандартного раствора щелочи, объем анализируемого раствора кислоты).
3. Концентрацию HCl в анализируемом растворе
4. Рассчитайте относительную ошибку определения, узнав у преподавателя истинную концентрацию кислоты в Вашем растворе.
5. Преимущества потенциометрического титрования перед обычным индикаторным.
6. Отличия потенциометрического титрования от обычного.
ФОТОКОЛОРИМЕТРИЯ
Введение
Колориметрией называют методы количественного анализа, основанные на сравнении окраски исследуемого раствора с окраской раствора, концентрация вещества в котором точно известна («коло» – цвет, окраска).
Раствор с точно известной концентрацией, применяемый для сравнения, называется стандартным.
Преимуществами этого метода являются:
1. Высокая чувствительность, что позволяет использовать его для определения микроколичеств (следов, примесей), когда другие методы не эффективны;
2. Быстрота;
3. Простота методики.
Для определения концентрации неокрашенных соединений методом колориметрии используют химические реакции, при которых определяемое вещество превращается в окрашенное соединение, вызывающее изменение окраски анализируемого раствора.
Зависимость между интенсивностью окраски и содержанием в нем окрашенного вещества описывается законом Бугера-Ламберта-Бера:
I = I010-elC или после логарифмирования lg(I0/I) = e×l×С
Величину lg(I0/I) = Д называют оптической плотностью раствора.
Она пропорциональна концентрации окрашенного вещества и толщине слоя раствора. Отношение интенсивности монохроматического потока излучения, прошедшего через окрашенный раствор, к интенсивности первоначального потока I/I0 = T называют прозрачностью или пропусканием Д = - lgT.
Интенсивность окраски растворов оценивается либо визуально, либо фотоколориметрически с помощью прибора фотоколориметра, имеющего фотоэлемент, преобразующий световую энергию в электрическую. Возникающий ток регистрируется чувствительным микроамперметром.
Точность фотоколориметрирования увеличивается при использовании монохроматических светофильтров, позволяющих выделить из сложного излучения ту спектральную область, в которой расположен максимум поглощения в спектре исследуемого вещества.
При массовых анализах для определения концентрации исследуемого раствора пользуются калибровочной кривой, построенной измерением оптической плотности стандартных растворов с постепенно возрастающими концентрациями определяемого вещества.
Фотоколориметры (ФЭК) существуют двух типов: 1) с одним фотоэлементом, когда на пути светового потока поочередно устанавливается эталон и исследуемый раствор; 2) с двумя фотоэлементами, где сравниваются интенсивности двух световых потоков, один из которых проходит через окрашенный раствор, а другой – через контрольный раствор.
ЛАБОРАТОРНАЯ РАБОТА
«Определение содержания ионов Cu2+
методом фотоэлектроколориметрии»
ЦЕЛЬ РАБОТЫ:
1. Освоить работу на фотоэлектроколориметре КФК З0-ЗОМЗ.
2. Определить концентрацию ионов Сu2+ в анализируемом растворе с помощью фотоколориметрии, используя метод калибровочного графика.
Ион меди Cu2+ входит в ядра клеток живых организмов, где участвует в окислительно-восстановительных процессах клетки. Для ее определения можно использовать комплекс, имеющий интенсивный синий цвет и образующийся по реакции:
Cu2+ + 4NH4OH = [Cu(NH3)4]2+ + 4H2O
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ:
1. Приготовление стандартной серии растворов.
Из исходного стандартного раствора CuSO4×5H2O, с концентрацией ионов меди 1 мг/л, (содержащего 3,9297 г CuSO4×5H2O и 4 мл конц. H2SO4 в 1 л раствора) готовят серию рабочих стандартных растворов комплексной соли [Cu(NH3)4]SO4 (приготовлены предварительно лаборантом)
Оптическую плотность растворов определяют в кюветах рабочей длины 1(2) см при красном светофильтре. Затем строят калибровочный график в координатах: оптическая плотность-концентрация.
При правильной работе градуировочный график подтвердит применимость закона Бэра, если будет представлять прямую линию.
2. Определение меди в исследуемом растворе.
а)К исследуемому раствору, выданному лаборантом в мерной колбе на 50,0 мл, прибавьте по каплям разбавленный NH4OH до появления мути, затем добавьте 10 мл NH4OH, долейте воду до метки и перемешайте.
б)Определите оптическую плотность анализируемого раствора, пользуясь кюветой в 1(2) см и красным светофильтром. Найдите по градуировочному графику концентрацию Cu2+ в 1 мл исследуемого раствора и рассчитайте концентрацию в моль/л.
в) Узнайте у преподавателя истинную концентрацию ионов Cu2+ в Вашем растворе, рассчитайте относительную ошибку определения.
Порядок работы на фотометре КФК – 03 – 01 – «ЗОМЗ»

Внешний вид фотометра представлен на рисунке. Прибор выполнен в виде одного блока. На металлическом основании 1 закреплены отдельные узлы, которые закрываются кожухом 2. Кюветное отделение закрывается съёмной крышкой 3. Ввод в световой пучок одной или другой кюветы осуществляется перемещением ручки 4 до упора влево или вправо. При установке ручки до упора влево в световой пучок вводится «холостая» проба (растворитель или контрольный раствор), при установке ручки до упора вправо – исследуемый раствор. При открытой крышке кюветного отделения шторка автоматически перекрывает световой поток. Ручка 5 служит для поворота дифракционной решетки и установки требуемой длины волны.
Подготовка прибора к работе
Для установления рабочего режима и обеспечения стабильной работы фотометр необходимо предварительно включить и выдержать не менее 30 мин. с момента включения.
Следите за тем, чтобы на прибор не попадали прямые солнечные лучи.
При работе с кюветами держите их за рёбра!
Измерение оптической плотности
1. Установите в кюветное отделение кюветы с «холостым» и исследуемым растворами: «холостой» - в дальнее гнездо, исследуемый – в ближнее. Измерение оптической плотности стандартных растворов начните с раствора с самой низкой концентрацией.
2. Ручку перемещения кювет установите в крайнее левое положение. При этом в световой пучок вводится «холостая» проба.
3. Закройте крышку кюветного отделения.
4. Клавишей «D» выберите режим измерения « А – оптическая плотность».
5. Нажмите клавишу «#».
На индикаторе отобразится надпись «Градуировка», через 3-5 с она исчезнет и вместо нее появится
«Измерение», « А = 0,000 ± 0,002 »
Если значение «0,000» отобразилось с большим отклонением, повторно нажмите клавишу «#».
6. Ручку перемещения кювет установите вправо до упора. При этом в световой пучок вводится исследуемый раствор. На индикаторе отображается значение его оптической плотности. Запишите данные в таблицу.
7. Повторите операции 2–5 три раза. Значение оптической плотности исследуемого раствора определяется как среднее арифметическое из полученных данных.
В ВЫВОДЕ УКАЖИТЕ:
1. Что сделано в работе?
2. Условия фотоколориметрического анализа (прибор, толщину кюветы, светофильтр)
3. Приведите найденную концентрацию ионов Cu2+ в анализируемом растворе №… и относительную ошибку измерения.
4. Дайте ответы на следующие вопросы:
1) В чем состоит принцип метода фотоколориметрии?
2) Как называют раствор с точно известной концентрацией в этом методе?
3) В чем преимущества использования метода колориметрии?
4) Какие химические реакции можно использовать в этом методе?
5) Как определяют концентрацию исследуемого раствора при массовых фотоколориметрических анализах?
6) Приведите примеры использования фотоколориметрии в клинических лабораториях.
ТЕМА «БИОГЕННЫЕ ЭЛЕМЕНТЫ»
ЗНАЧЕНИЕ ТЕМЫ:
Биогенные элементы необходимы для построения и жизнедеятельности различных клеток и организмов. Основу живых систем составляют так называемые органогены: C, H, O, N, P, S, из которых состоят углеводы, жиры, белки и нуклеиновые кислоты; и «неорганические микроэлементы»: Ca, Cl, Mg, K, Na. С недостатком или избыточным накоплением различных биогенных элементов связано немало заболеваний, т. к. при этом нарушается гомеостаз. Широко используют различные элементы и их соединения в качестве лекарственных средств. Изучение биологической роли химических элементов, выявление взаимосвязи обмена этих элементов и других биологически активных веществ ферментов, гормонов, витаминов – способствует созданию новых лекарственных средств и разработке оптимальных режимов их дозирования.
1. Занятие проводится в форме конференции.
2. Выступление должно быть оформлено на компьютере в виде презентации (программа Microsoft Power Point). При выступлении используется мультимедиа проектор.
3. Продолжительность выступления должна быть 9 – 10 минут.
4. На первом слайде печатается название доклада, фамилии авторов, номер группы, год.
5. В конце доклада приводится слайд с библиографическим описанием литературных источников, в том числе и адрес в Интернете.
6. Собранные группами сведения необходимо обработать:
- обобщить;
- систематизировать,
- найти закономерности;
- привести формулы соединений;
- использовать схемы, графики, рисунки (с подписями), а не только фотографии продуктов.
7. Конференция посвящена биогенным элементам, поэтому внимание должно быть уделено биологической роли элемента, заболеваниям при избытке и недостатке его, а не истории его открытия или промышленному использованию.
8. Слайд должен быть кратким и информативным, не перегруженным текстом.
9.Текст доклада в распечатанном виде сдается преподавателю вместе с диске9той или диском.
Приложение
ТЕРМОДИНАМИЧЕСКИЕ КОНСТАНТЫ ВЕЩЕСТВ
Вещество | Состояние | DН°298 кДж/моль | S°298 Дж/моль•К | DG°298 кДж/моль | Вещество | Состояние | DН°298 кДж/моль | S°298 Дж/моль•К | DG°298 кДж/моль |
BaO | Т | -553.9 | 70.5 | -525.4 | Н2 | г | 0 | 130.7 | 0 |
BaO2 | Т | -630.6 | - | - | Н2О | ж | -286.0 | 70.0 | -237.4 |
Al2(SO4)3 | Т | -3434 | 239.2 | -3101 | Н2О | г | -241.9 | 188.9 | -228.8 |
СН4 | Г | -74.9 | 186.4 | -50.9 | Н+ | р | 0 | 0 | 0 |
С2Н2 | Г | 226.7 | 200.8 | 209.2 | ОН- | р | -230.2 | -10.9 | -157.4 |
С2Н4 | Г | 52.3 | 219.4 | 68.1 | H2SO4 | ж | -811 | 156.9 | -690.3 |
С2Н6 | Г | -84.7 | 229.5 | -32.9 | MgO | Т | -601 | 26.9 | -569.6 |
С6Н6 | Ж | 82.09 | 26,9 | 124.5 | Mg(NO3)2 | Т | -790 | 164 | -690 |
С2Н5ОН | Ж | -277.7 | 160.7 | -174.8 | NH3 | г | -46.2 | 192.6 | - 16.7 |
СН3СООН | Ж | -487.0 | 159.8 | -392.4 | NH4Cl | Т | -315.0 | 96.0 | - |
СО | Г | -110.6 | 197.7 | -137.2 | NH4NO3 | Т | -366.0 | 151.0 | - |
СО2 | Г | -393.8 | 213.8 | -394.6 | (NH4)2SO4 | Т | -1181.0 | 220.0 | -901.3 |
BaCO3 | Т | -1202 | 112.1 | -1139 | N2 | Г | 0 | 192.0 | 0 |
Са | Т | 0 | 41.6 | 0 | N2O | Г | 81.6 | 220.0 | - |
СаСО3 | Т | -1207.7 | 91.6 | -1129.6 | NO | Г | 90.4 | 210.6 | 86.7 |
СаО | Т | -635 | 39.7 | -603.6 | NO2 | Г | 33.8 | 240.5 | 51.8 |
Са(ОН)2 | Т | -986.8 | 83.4 | -699.2 | HNO3 | Ж | -173.0 | 156.2 | -79.9 |
СаНРО4•2Н2О | Т | -2403 | 189.0 | -215.3 | Na2O | Т | -430.6 | 71.1 | -376.6 |
CH3OH | Ж | -238.5 | 126.8 | -166.2 | NaHCO3 | Т | -914.0 | 102.0 | -852 |
HCl | Г | -92.4 | 186.9 | -94.5 | О2 | Г | 0 | 205.0 | 0 |
CuSO4 | Т | -771.4 | 109.3 | -662.2 | Pb(NO3)2 | Т | -451.7 | 217.9 | -256.9 |
CuO | Т | -162.1 | 42.7 | -129.5 | Р4О10 | Т | -2984.0 | 228.8 | -2697.8 |
CuCO3 | Т | -595.4 | 92.9 | -518.3 | Н3РО4 | Ж | -1271.9 | 200.8 | -1147.2 |
Cu(NO3)2 | Т | -307.1 | 193.0 | -114.2 | PbS | Т | 94.3 | 91.2 | -92.7 |
Fe2O3 | Т | -822.7 | 87.5 | -740.8 | Глюкоза | Т | -1273.0 | - | -919.5 |
CH3CHO | Ж | -166.0 | 264.2 | -- | ZnS | т | -205.4 | 57.7 | -200.7 |
Fe | Т | 0 | 27.2 | 0 | SO2 | Г | -297.2 | 248.2 | -300.4 |
PbO | Т | -219 | 66,1 | -189,1 | KCl | Т | -436,6 | 82,6 | -409 |
С | Т | 0 | 5.7 | 0 | Al2O3 | Т | -1676 | 50,9 | -1582 |
FeO | Т | -263.7 | 58.8 | - | SO3 | Г | -376.2 | 256.4 | -370.0 |
KСlO3 | Т | -514 | 151,6 | -425,5 |
Таблица 2

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



