Министерство здравоохранения Российской Федерации.
Кировская государственная медицинская академия.
Общая химия
Методическое руководство
для аудиторной работы студентов
стоматологического факультета.
Киров-2009
УДК 546.
Печатается по решению редакционно - издательского совета Кировской государственной медицинской академии протокол №_____ от « » _______200__ г.
Общая химия. Методическое руководство для аудиторной работы студентов./ Сост. , Киров: Кировская государственная медицинская академия. 2009. – 61 с.
Методическое пособие предназначено для аудиторной работы студентов стоматологического факультета по общей химии. Оно составлено в соответствии с рабочей программой от 2009 года и включает для каждой темы задание для самостоятельной аудиторной работы студентов (САРС), описание лабораторной работы, контрольные вопросы. В конце приведены необходимые справочные материалы.
Рецензент:
д. м.н., профессор, зав. кафедрой
биологической химии Кировской ГМА
– Киров, 2009.
компьютерный набор:
ПРАВИЛА ВЫЖИВАНИЯ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ
- Если в руках у вас жидкое – не разлейте, порошкообразное – не рассыпьте, газообразное – не выпустите наружу.
- Если включили – выключите.
- Если открыли – закройте.
- Если разобрали – соберите.
- Если вы не можете собрать – позовите на помощь умельца.
- Если вы не разбирали – не вздумайте собирать.
- Если вы одолжили что-нибудь – верните.
- Если вы пользуетесь чем-либо, держите в чистоте и порядке.
- Если привели что-либо в беспорядок – восстановите статус кво.
- Если вы сдвинули что-нибудь – верните на место.
- Если вы хотите воспользоваться чем-либо, принадлежащим другому, попросите разрешения.
- Если вы не знаете, как это действует, ради Бога, не трогайте.
- Если вас это не касается – не вмешивайтесь.
- Если вы не знаете, как это делается – сразу спросите.
- Если не можете что-либо понять – почешите в затылке.
- Если все же не поймете, то и не пытайтесь.
- Если вы горите на работе, постарайтесь, чтобы у вас ничего не загорелось.
- Если у вас что-либо взорвалось, проверьте, остались ли вы живы.
- Если не усвоили этих правил, не входите в лабораторию.
ТЕМА: «ВВОДНОЕ ЗАНЯТИЕ.
ПРАВИЛА РАБОТЫ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ.
КОЛИЧЕСТВЕННЫЙ АНАЛИЗ.
ОСНОВЫ ТИТРИМЕТРИЧЕСКОГО (ОБЪЕМНОГО) АНАЛИЗА»
ЗНАЧЕНИЕ ТЕМЫ
Знание важнейших методов и приемов количественного анализа необходимо будущему врачу, поскольку в медицинской практике количественный анализ широко применяется при исследовании крови, мочи, желудочного сока, лекарственных препаратов, пищевых продуктов и т. д.
I. Выполните упражнения (САРС)
1. Вычислите молярную концентрацию эквивалентов растворов, содержащих:
а) 1,25 моль эквивалентов Ва(ОН)2 в 250 мл раствора Ва(ОН)2;
б) 1,5 г СН3СООН в 50 мл раствора СН3СООН;
в) 42,6 г Na2SO4 в 2,5 л раствора Na2SO4.
2. В мерной колбе на 500 мл приготовили раствор питьевой соды. На титрование 10,00 мл этого раствора израсходовали 15,30 мл раствора НСl с концентрацией 0,1063моль/л.
Рассчитайте:
- какова молярная концентрация эквивалентов в растворе соды?
- титр этого раствора.
- массу соды в приготовленном растворе.
II. Лабораторная работа.
«Определение содержания сильной кислоты в водном растворе методом кислотно-основного титрования».
ЦЕЛЬ РАБОТЫ
1. Овладеть методикой титрования.
2. Определить точную концентрацию раствора кислоты методом кислотно-основного титрования.
ОБОРУДОВАНИЕ И РЕАКТИВЫ
Бюретки вместимостью 25 см3 в штативе, воронка, колба коническая для титрования вместимостью 250 см3, колба для слива, пипетка мерная вместимостью 10 см3, резиновая груша, колба для переноса растворов.
Раствор тетрабората натрия с точно известной концентрацией, анализируемый раствор соляной кислоты, раствор индикатора – метилоранжа в капельнице.
СУЩНОСТЬ МЕТОДИКИ
Раствор HCl с точной концентрацией нельзя приготовить по точной массе исходного вещества из-за его летучести. Поэтому раствор HCl готовят приблизительной концентрации разбавлением концентрированного раствора, а затем определяют его точную концентрацию (стандартизируют) путем титрования. Для этого надо иметь первичный стандарт – раствор основания с точно известной концентрацией. Его готовят по точной навеске. Веществом, наиболее удобным в качестве первичного стандарта для HCl является тетраборат натрия, Nа2В4О7 . 10Н2О (бура) – соль сильного основания и слабой кислоты.
УРАВНЕНИЕ РЕАКЦИИ
Na2B4O7 . 10H2O + 2HCl ® 2NaCl + 4H3BO3 + 5H2O
ХОД РАБОТЫ
1. Подготовка бюретки к работе.
- Бюретка установлена в штативе строго вертикально. Выливают из бюретки воду и ополаскивают ее изнутри небольшой порцией соляной кислоты, пользуясь воронкой.
- Заполняют кончик бюретки, «носик», раствором, чтобы не было пузырьков воздуха.
- Заполняют бюретку раствором несколько выше нулевого деления и убирают воронку, так как с нее может капать раствор.
- Выпуская лишний раствор, заполняют бюретку до нулевой отметки (по нижнему краю мениска).
- Кладут на основание штатива листок белой бумаги.
2. Подготовка пробы раствора Nа2В4О7 для титрования.
- Из общей склянки с раствором тетрабората натрия отливают в колбу для переноса раствора ~ 50 см3 раствора буры.
- Для ополаскивания пипетки в нее с помощью груши засасывают из колбы раствор тетрабората выше метки и выливают его в колбу для слива.
- В колбу для титрования переносят 10.00 мл раствора тетерабората натрия, соблюдая все правила обращения с пипеткой (раствор набирают с помощью груши, пипетку держат вертикально, закрывая отверстие указательным пальцем (рис. 1), раствор в колбу выливается самотеком, а не выдувают, последнюю каплю удаляют, прикасаясь концом пипетки к стенке колбы).
- Добавляют в колбу 1 каплю раствора метилоранжа. Окраска раствора желтая.
3. Проведение титрования.
- Ставят колбу с раствором тетрабората натрия под бюретку. Первое титрование носит ориентировочный характер. Добавляют раствор из бюретки небольшими порциями, постоянно перемешивая содержимое колбы (лучше правой рукой).
- Титрование заканчивают, когда произойдет изменение окраски из желтой в оранжевую, записывают результат титрования с точностью до 0,05 мл.
- Содержимое колбы выливают в раковину, колбу ополаскивают водой и вносят с помощью пипетки новую порцию раствора Nа2В4О7 и индикатор.
- Последующие титрования проводят более точно. Для этого из бюретки в колбу быстро добавляют основной объем титранта, а последние порции добавляют по каплям, внимательно следя за изменением окраски раствора. Титрование прекращают, когда изменение окраски происходит при добавлении всего одной капли.
- Титрование повторяют до тех пор, пока не будет получено три сходящихся результата (то есть отличающиеся не более чем на 0,20 мл). Титрование каждый раз начинают с нулевой отметки.
РЕЗУЛЬТАТЫ ТИТРОВАНИЯ (ОБРАЗЕЦ)
Анализируемый раствор: HCl » 0,1 н. Выдан лаборантом.
![]() Титрованный раствор (стандартный): Nа2В4ОН2О. Приготовлен лаборантом. СН = 0,0961 мль/л.
Титрованный раствор (стандартный): Nа2В4ОН2О. Приготовлен лаборантом. СН = 0,0961 мль/л.
HCl Nа2В4О7
индикатор: метилоранж
СК = ? V1 = 10,30 мл V2 = 10,25 мл V3 = 10,30 мл По бюретке | Сб = 0,0961 моль/л Vб = 10,00 мл (пипеткой) |
Vср. = 10,28 мл |
Расчет:
1) Объем раствора HCl, пошедший на титрование, находят как среднее арифметическое их трех сходящихся результатов (точность – до 0,01мл).
2) Для вычисления концентрации раствора HCl используют закон эквивалентов:
C (HCl) . V (HCl) = C (Na2B4O7) . V (Na2B4O7)
C (HCl) = 
T (HCl) = ![]()
Вариант оформления протокола:
Название работы.
Цель работы.
Сущность работы и уравнение реакции.
Результаты титрования и расчет СН и Т(HCl).
Вывод, в котором указывают, что сделано в работе, и найденные СН (HCl) с точностью 4-5 знаков после запятой и Т (HCl) с точностью 5-6 знаков после запятой.
ОСНОВНЫЕ РАСЧЕТНЫЕ ФОРМУЛЫ, ИСПОЛЬЗУЕМЫЕ В ТИТРИМЕТРИЧЕСКОМ АНАЛИЗЕ
1. Фактор эквивалентности.
f (кислоты) = 
f (основания) = 
f (соли) = 
2. Молярная масса эквивалентов вещества.
М э (или Э) = f. М = ![]() . М
. М
3. Число моль вещества Число моль эквивалентов вещества
n = | nэ = nэ = С (э) . V nэ = |
4. Молярная концентрация Молярная концентрация эквивалента
С (х) = ![]()
![]() С (э) =
С (э) = ![]()
5. Масса вещества
m = n. М m = nэ. f. M
m = С (э) . f. M. V
m= C (э) . Э. V
6. Титр раствора
Т = ![]()
Т = ![]()
7. Закон эквивалентов
nА = nB
САVА = СВ. VВ.
ТЕМА: «ТИТРИМЕТРИЧЕСКИЙ (ОБЪЕМНЫЙ) АНАЛИЗ.
КИСЛОТНО-ОСНОВНОЕ ТИТРОВАНИЕ».
I. Выполните упражнения (САРС)
1. В запаянной ампуле находилось 0,1 моль-эквивалент едкого кали. Из него в мерной колбе приготовили 500 мл раствора (приготовление из фиксанала). Какова молярная концентрация эквивалента приготовленного раствора?
2. В мерной колбе на 100 мл растворили 0,56 г КОН, и раствор довели до метки. Какова молярная концентрация эквивалента полученного раствора?
3. В мерной колбе на 50 мл приготовили 0,01 н раствор Na2CO3. Сколько моль эквивалентов соды содержится в этом растворе? Сколько граммов?
4. Сколько миллилитров 0,5 н НСl эквивалентны 4 г NаОН?
5. Чему равен титр раствора, если 500 мл его содержат 0,01 моль NаОН?
6. Не проводя расчета, скажите, сколько 0,1 н раствора НСl потребуется на титрование 5 мл 0,1 н раствора КОН. Ответ поясните.
7. На титрование пробы раствора щелочи израсходовано 15 мл 0,02 н раствора НСl. Сколько миллимоль эквивалентов щелочи прореагировало с кислотой?
II. Лабораторная работа.
«Определение содержания соды в контрольном препарате».
Работа 1. Приготовление рабочего раствора соляной кислоты.
Примерные задания студентам:
«Приготовить 250 мл 0,1 н раствора НСl из концентрированного раствора плотностью 1,179 г/мл».
РЕШЕНИЕ:
1. С помощью таблицы по плотности определяют массовую долю исходного раствора. Плотности 1,179 г/мл соответствует 36% раствор НСl.
2. Определяем содержание НСl в 250 мл 0,1 н раствора:
m = Cн.![]() ∙ М∙ V = 0,1∙1∙36,5∙0,25 = 0,9125г НСl
∙ М∙ V = 0,1∙1∙36,5∙0,25 = 0,9125г НСl
3. Определяем, какая масса концентрированной кислоты содержит 0,9125 г НСl:
100 г 36% раствора содержится 36 г НСl
х г – 0,9125 г НСl
х = 2,53 г НСl.
4. Взвешивать кислоту неудобно, поэтому находим объем раствора кислоты:
V = ![]() 2,1 мл 36% раствора НСl
2,1 мл 36% раствора НСl
5. Отмерим этот объем концентрированной кислоты маленькой градуированной пробиркой, перельем этот раствор в мерную колбу и разбавим дистиллированной водой до 250 мл. Дистиллированную воду добавляем до метки с помощью пипетки. Тщательно перемешаем полученный раствор.
Кислота соляная, разведенная (8,2 – 8,4%) используется внутрь в каплях в микстурах (часть с пепсином) при недостаточности кислотности желудочного сока. При гипохромных анемиях вместе с препаратами железа она способствует улучшению всасывания и использования железа.
Работа 2. Стандартизация рабочего раствора соляной кислоты.
ЦЕЛЬ РАБОТЫ:
Научится стандартизировать – определять точную концентрацию рабочего раствора и проводить расчеты с использованием закона эквивалентов.
Веществом, наиболее удобным для установки титра соляной кислоты считают тетраборат натрия Na2B4O7 . 10H2O:
Na2B4O7 . 10H2O + 2HCl = 2NaCl + 4H3BO3 + 5H2O
Титрование ведут с индикатором метиловым оранжевым путем приливания кислоты из бюретки к раствору тетрабората натрия.
1. Тщательно вымытую бюретку промыть небольшой порцией соляной кислоты для удаления остатков воды. Пользуясь воронкой, наполнить бюретку соляной кислотой так, чтобы мениск ее был несколько выше нулевого деления. Заполнить раствором оттянутую трубку, вытеснить из нее пузырьки воздуха. Затем убрать воронку, т. к. с нее может капать раствор, и, выпуская лишнюю кислоту, установить нижний край мениска на нулевом делении. В таком состоянии бюретка подготовлена к работе.
2. Чистой пипеткой отмерить 10,00 мл раствора тетрабората натрия в коническую колбу для титрования. Не следует выдувать из пипетки последнюю каплю жидкости, а только прикоснуться концом ее к стенке колбы. Прилить к раствору тетрабората 1 каплю метилоранжа.
3. На основание штатива положить лист белой бумаги. Подставить колбу с раствором тетрабората натрия под бюретку и приступать к титрованию с соблюдением всех правил. Надо добиться того, чтобы желтая окраска метилоранжа переходила в бледно-розовую от одной избыточной капли кислоты. Титрование повторять до получения сходящихся результатов, т. е. пока отсчеты будут отличаться друг от друга не более чем на 0, 20 мл. Все результаты титрования записывать в тетрадь. Титровать не менее трех раз. Титрование необходимо начинать каждый раз с нулевой отметки.
4. Результат титрования записать по образцу, приведенному ниже, с.10.
Работа 3. Определение содержания Na2CO3.
Получить у преподавателя контрольный раствор соды в мерной колбе и записать в тетради его номер.
Довести объем раствора дистиллированной водой до метки и тщательно перемешать. Промыть пипетку раствором соды, затем 10,0 мл контрольного раствора перенести промытой пипеткой в коническую колбу, прибавить 1 каплю метилоранжа и титровать рабочим раствором соляной кислоты до перехода желтой окраски индикатора в бледно-розовую от одной капли кислоты. Титровать до получения сходящихся результатов не менее 3 раз.
Из сходящихся результатов взять среднее значение.
Вычислить сначала молярную концентрацию эквивалента раствора соды, а затем массу Na2CO3 в контрольном растворе, т. е. в 50 мл.
Оформите результаты титрования по образцу, с. 10.
В выводе отразите итог проделанной работы.
ТЕМА: «КОЛИЧЕСТВЕННЫЙ АНАЛИЗ. ОКСИДИМЕТРИЯ.
МЕТОД ПЕРМАНГАНАТОМЕТРИИ»
I Выполните упражнения (САРС)
В уравнениях окислительно-восстановительных реакций найдите:
- окислитель и восстановитель;
- коэффициенты;
- факторы эквивалентности окислителя и восстановителя и молярную массу их эквивалентов.
а) HNO3 + H2S = NO + S + H2O
б) K2MnO4 + Cl2 = KMnO4 + KCl
I. Лабораторная работа.
«Стандартизация раствора перманганата калия. Определение концентрации пероксида водорода методом перманганатометрии».
ЦЕЛЬ РАБОТЫ
1) Стандартизировать раствор перманганата калия с помощью щавелевой кислоты (или оксалата натрия).
2) Определить точную концентрацию пероксида водорода в контрольном растворе методом перманганатометрии.
ОБОРУДОВАНИЕ И РЕАКТИВЫ
Бюретки вместимостью 25 см3 в штативе, воронки, мерные пипетки вместимостью 5 см3, колбы конические для титрования вместимостью 250 см3, колбы для слива, резиновая груша, колбы для переноса растворов, мерные пробирки на 10 см3, мерный цилиндр вместимостью 30 см3, мерная колба вместимостью 50 см3, плитка.
Раствор перманганата калия, раствор щавелевой кислоты или оксалата натрия с точно известной концентрацией, раствор 2н серной кислоты, мерная колба с пробой пероксида водорода.
СУЩНОСТЬ МЕТОДИКИ
Перманганатометрическое титрование основано на том, что KMnO4 является сильным окислителем в кислой среде и вступает в реакции со многими восстановителями.
Раствор KMnO4 нельзя приготовить, исходя из точной массы вещества, так как в нем всегда содержится примесь MnO2, а в водном растворе MnO4- окисляет органические примеси и саму воду. Поэтому раствор KMnO4 готовят приблизительной концентрации, выдерживают его 10-12 дней в темной склянке, а затем стандартизируют, используя в качестве первичного стандарта щавелевую кислоту или оксалат натрия.
ОСОБЕННОСТИ ПЕРМАНГАНАТОМЕТРИИ:
1. Титрование проводят в кислой среде (в присутствии Н2SО4), в которой Mn+7 переходит в бесцветный ион Mn2+, проявляя наибольшую окислительную способность.
2. Для фиксирования точки эквивалентности не требуется индикатор. При достижении точки эквивалентности первая избыточная капля раствора KMnO4 окрашивает титруемый раствор в розовый цвет, что и является сигналом для прекращения титрования.
3. Для ускорения титрования его проводят при нагревании.
Опыт № 1. Стандартизация раствора перманганата калия по щавелевой кислоте (Н2С2О4) или оксалату натрия (Na2С2О4).
Определение основано на реакции:
2KMnO4 + 5Н2С2О4 + 3Н2SО4 = K2SO4 + 2MnSO4 + 10CO2 + 8Н2О
 восстановиС2 Ое ® 2СО2 – окисляется
восстановиС2 Ое ® 2СО2 – окисляется
окислитель 2 MnО 4- + 8Н+ + 5ё ® Mn2+ + 4Н2О
f (KMnO4) = ?
Выполнение работы.
1. Заполните бюретку раствором KMnO4.
2. Возьмите пипеткой 5 мл 0,02 н раствора Н2С2О4 и перенесите его в колбу для титрования.
3. Добавьте мерной пробиркой 4-5 мл 2 н Н2SО4.
4. Нагрейте раствор до 70-800С (не допуская кипения).
5. Горячий раствор титруйте перманганатом калия:
а) отсчет показаний бюретки ведите по верхнему (!) краю мениска;
б) титрование производите по каплям, при непрерывном помешивании. Каждую следующую каплю добавляйте после того, как обесцветилась предыдущая;
в) титрование прекратите, когда избыточная капля KMnO4 придаст раствору бледную розовую окраску, не исчезающую в течение 1-2 мин.
6. Титрование повторите 3 раза.
Результаты титрования оформите обычным образом, с. 6. Рассчитайте Сн и Т раствора перманганата калия.
Опыт № 2. Определение концентрации пероксида водорода в аптечном препарате.
Уравнение реакции:
 2 KMnO4 + 5Н2О2 + 3H2SO4 = K2SO4 + 2MnSO4 + 5O2 + 8H2O
2 KMnO4 + 5Н2О2 + 3H2SO4 = K2SO4 + 2MnSO4 + 5O2 + 8H2O
окислитель 2 Mn7+ + 5e ® Mn2+ восстанавливается
восстановиО - - 2е ® О2 окисляется
f (Н2О2) = ?
Ход работы.
1. Получите у преподавателя мерную колбу с пробой пероксида водорода и запишите её номер. Доведите объем раствора до метки дистиллированной водой. Закройте колбу пробкой и перемешайте. 5 мл полученного раствора перенесите пипеткой в колбу для титрования, добавьте мерной пробиркой 5 мл 2 н Н2SО4 и мерным цилиндром 30 мл дистиллированной воды.
2. Титруйте рабочим раствором KMnO4 до слабо-розовой окраски.
3. Титрование повторите 3 раза.
Результаты титрования оформите обычным образом, с. 10. Рассчитайте
СН и Т раствора пероксида водорода.
Узнав у преподавателя истинную концентрацию раствора Н2О2, рассчитайте относительную ошибку определения.
В выводе отметьте, что сделано в работе и какие получены результаты.
Ответьте на вопросы:
- Как определяется точка эквивалентности в перманганатометрии?
- Почему титрование проводят в кислой среде и при нагревании?
ТЕМА: «ЭНЕРГЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
(ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА)»
ЗНАЧЕНИЕ ТЕМЫ
Живые организмы получают энергию за счет химических реакций окисления питательных веществ. Превращение этой энергии в живой клетке подчиняется тем же законам термодинамики, что и в неживой природе. Первый закон термодинамики дает возможность рассчитать теплоту, выделяемую или поглощаемую при химических реакциях. Второй закон позволяет предсказать возможность самопроизвольного протекания химической реакции.
I. Выполните упражнения.
САРС
1. Сколько тепла выделится при сгорании 2,24 л этилена (н. у.).
(ответ: DН = - 141,9 кДж).
2. Рассчитайте тепловой эффект реакции этерификации и определите, экзо - или эндотермическим является этот процесс образования сложного эфира (DН0обр(СН3СООС2Н5) = -469,5 кДж/моль).
С2Н5ОН (ж) + СН3СООН (ж) ® СН3СООС2Н5 (ж) + Н2О (ж)
(ответ: DН = 9,2 кДж/моль)
3. В организме человека процесс метаболизма глюкозы при достаточном количестве кислорода протекает до СО2 и Н2О:
С6Н12О6 + 6О2 ® 6СО2 +6Н2О,
а при недостатке кислорода – до молочной кислоты:
С6Н12О6 ® 2СН3СН – СООН
ê
ОН
Определите, в каком случае эффективнее усваиваются углеводы (DН0обр молочной кислоты = -673 кДж/моль).
(ответ: DН1 = -2805 кДж/моль; DН2 = -73 кДж/моль)
4. DН0растворения SrCl2 и SrCl2· 6H2O составляют – 47,6 и + 30,9кДж/моль. Вычислите DН0гидратации SrCl2
5. В 100 г трески содержится 11,6 г белка и 0,3 г жира. Рассчитайте энергию, которая выделится при усвоении порции трески 228 г?
(ответ: 475,6 кДж)
6. Подсчитано, что бегущий человек среднего веса затрачивает 160 ккал на 1 км. Какое количество пшеничного хлеба, содержащего 7% белка, 1% жиров и 64% углеводов, обладает калорийностью, позволяющей пробежать 5 км?
(ответ: 273 г)
7.Не выполняя расчета, оцените, как изменится энтропия для следующих реакций: а) N2 (г) + 3Н2 (г) ® 2NH3 (г);
б) SO2 (г) + Cl2 (г) ® SO2Cl2 (г);
в) С6H12O6 (р) ® 2CO2 (г) + 2С2H5ОН (ж);
г) С6Н12 (ж) + 9О2 (г) ® 6СО2 (г) + 6Н2О (ж);
д) Fe2O3 (тв) +3CO (г) ® 2Fe (тв) + 3CO2 (г).
8. Вычислите стандартное изменение энергии Гиббса и определите возможность самопроизвольного протекания реакции при стандартной температуре 298К.
Fe2O3 (тв) +3CO (г) = 2Fe (тв) + 3CO2 (г)
(ответ: -31,4 кДж/моль)
9. Вычислив DG, определите возможность протекания реакции при 9000С
2SO2 + O2 = 2SO3
Какой фактор, энтальпийный или энтропийный, определяет направление процесса?
(ответ: 63,7 кДж)
II. Лабораторная работа.
«Определение энтальпии реакции нейтрализации»
Цель работы
Определить экспериментально энтальпию реакции нейтрализации сильной кислоты щелочью.
Сущность методики
Определение теплоты, выделяемой или поглощаемой при протекании химического процесса, осуществляется с помощью калориметра.
Калориметр - это устройство, в котором количество теплоты, выделяемое или поглощаемое в ходе процесса, измеряется по изменению температуры калориметра. Калориметр состоит из двух сосудов - внешнего и внутреннего, пространство между которыми представляет воздушную изотермическую оболочку для предотвращения потерь теплоты. Крышка внутреннего сосуда снабжена отверстиями для ручной мешалки, воронки для введения веществ, термометра для измерения температуры.
Оборудование и реактивы
Калориметр, цилиндры на 25 мл (2 шт.), весы, растворы соляной и азотной кислот, гидроксидов натрия и калия с концентрацией 2 моль/л, мензурка на 100 мл, дистиллированная вода, соли КСl и Na2CO3.
Опыт 1. Определение энтальпии нейтрализации сильной кислоты щелочью
Варианты | 1 | 2 | 3 | 4 |
Кислота | HCl | HCl | HNO3 | HNO3 |
Щелочь | NaOH | KOH | NaOH | KOH |
Расчет теоретического значения энтальпии нейтрализации
Уравнение реакции нейтрализации:
HCl (p) + NaOH (p) ® NaCl (p) + H2O (ж)
H+(р) + OH-(р) ® H2O (ж)
Расчет энтальпии нейтрализации сильной кислоты щелочью ведется по краткому ионному уравнению, которое отражает сущность взаимодействия сильных электролитов.
Выполнение работы
1. Взвесьте внутренний сухой стакан калориметра с точностью до 0,1 г.
2. Налейте в него 25 мл 2н. раствора кислоты и измерьте начальную температуру раствора.
3. Быстро прилейте 25 мл 2н. раствора щелочи, перемешайте и определите конечную температуру смеси - наивысшую температуру раствора.
4. Данные начальной и конечной температуры занесите в таблицу.
Оформление результатов
1. Рассчитайте количество теплоты, которое выделилось при нейтрализации и пошло на нагревание смеси, по формуле:
Q1 = Cp · rp · V ·Dt
где: V - суммарный объем раствора, мл;
rp - плотность раствора, для разбавленных растворов принимается равной плотности воды, т. е. 1 г/мл;
Сp - удельная теплоемкость раствора, равная 3,5 Дж/(г×К);
Dt = ( t кон - t нач ) - разность температур.
Таблица 1
tн | tк | Dt | Теплота, пошедшая на нагревание смеси | Теплота, пошедшая на нагревание стакана | |||||
Vp | rp | Cp | Q1 | m | C | Q2 | |||
2. Рассчитайте количество теплоты, пошедшее на нагревание стакана, по формуле:
Q2 = C · m · Dt
где: m - масса стакана, г;
С - удельная теплоемкость стекла, равная 0,838 Дж/(г×К)
3. Рассчитайте экспериментальную энтальпию реакции нейтрализации
одного моль эквивалентов кислоты. Повышение температуры в калориметре свидетельствует о том, что энтальпия системы уменьшилась.
![]()
где nэ - число моль эквивалентов кислоты, взятое для реакции, которое рассчитывают по формуле: nэ = СНСl . VHCl
4. Сравните полученный результат с рассчитанным теоретическим значением и вычислите относительную ошибку опыта.
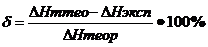
В выводе ответьте на следующие вопросы
1. По изменению температуры опыта укажите, экзо - или эндотермической является реакция нейтрализации сильной кислоты щелочью? Какой знак имеет энтальпия этой реакции?
2. Выпишите значения энтальпии нейтрализации, полученные Вашими товарищами в других сочетаниях «кислота-щелочь». Объясните, почему энтальпия нейтрализации сильной кислоты щелочью не зависит от природы кислоты или щелочи и является величиной постоянной.
ТЕМА: «КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ»
ЗНАЧЕНИЕ ТЕМЫ
Общие принципы химической кинетики применимы и к биохимическим ферментативным реакциям. Понятие о скорости химических реакций и о влиянии на нее различных факторов (концентрации реагирующих веществ, температуры, рН среды, катализаторов) необходимо врачу, поскольку на скорость биохимических реакций оказывают влияние лекарственные препараты, от скорости ферментативных реакций зависит интенсивность обмена веществ в организме и т. д.
I. Выполните упражнения.
А. Скорость химических реакций.
1. В процессе газового разложения NО2 по уравнению 2NO2 = 2NО + О2, концентрация NО2 в начальный момент времени была 0,01 моль/л, а через 120 секунд она стала равной 0,0016 моль/л. Найдите среднюю скорость реакции. Изобразите кинетические кривые для NО2 и О2.
2. Напишите математическое выражение для скоростей следующих химических реакций:
N2 г + O2 г = 2NOг
Ca т + Cl2 г = CaCl2 т
2C т + O2 г = 2CO г
3. Во сколько раз изменится скорость реакции 2SO2 (г) + O2 (г) = 2SO3 (г)
1) если увеличить концентрацию кислорода в 2 раза;
2) если увеличить концентрацию SO2 в 2 раза;
3) если одновременно увеличить концентрации О2 и SО2 в 2 раза?
4. Как зависит скорость химической реакции от температуры? Что показывает температурный коэффициент скорости химической реакции?
5. Во сколько раз изменится (уменьшится, увеличится) скорость химической реакции при изменении температуры от 700 до 200, если температурный коэффициент равен 2?
Б. Химическое равновесие.
1. Какие реакции называются обратимыми?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



