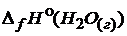 = -241,8
= -241,8  ;
; 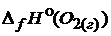 = 0.
= 0.
По следствию из закона Гесса:
Для данной реакции
![]() = (4 ∙
= (4 ∙ 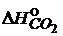 + 6 ∙
+ 6 ∙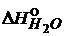 ) – (2 ∙
) – (2 ∙ ![]() + 7 ∙
+ 7 ∙ ![]() ).
).
Подставляем табличные данные:
![]() = (4 ∙ (-393,5) + 6 ∙(-241,8)) – (2 ∙ (-84,7) + 7 ∙0) = -2855,4 кДж
= (4 ∙ (-393,5) + 6 ∙(-241,8)) – (2 ∙ (-84,7) + 7 ∙0) = -2855,4 кДж
Т. к. < 0, то реакция – экзотермическая (с выделением энергии) и термохимическое уравнение имеет вид:
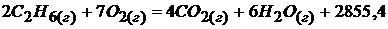 кДж
кДж
Если сгорает 2 моля , то выделяется 2855,4 кДж энергии (по уравнению реакции).
Объем 2 молей составляет 22,4 дм3 ∙ 2 = 44,8 дм3 (при нормальных условиях).
Составим пропорцию:
44,8 л – 2855,4 кДж
5 л – Х
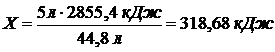
Ответ: при сгорании 5 литров этана выделяется 318,68 кДж теплоты.
Задача 3. Рассчитать изменение стандартной энтропии в реакции синтеза аммиака 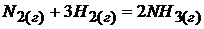 .
.
Решение. В таблице находим значения стандартных абсолютных энтропий:
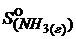 = 193 Дж ∙ моль─1К─1;
= 193 Дж ∙ моль─1К─1;
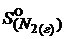 = 192 Дж ∙ моль─1К─1;
= 192 Дж ∙ моль─1К─1;
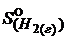 = 131 Дж ∙ моль─1К─1;
= 131 Дж ∙ моль─1К─1;
![]() = 2 ∙ 193 – 192 – 3 ∙ 131 = -195 Дж ∙ К─1
= 2 ∙ 193 – 192 – 3 ∙ 131 = -195 Дж ∙ К─1
В рассмотренном примере энтропия уменьшается. Этого можно было ожидать, если учесть, что в результате реакции уменьшается объем газообразных веществ, а, следовательно, неупорядоченность в системе.
Задача 4. Определить, возможна ли данная реакция при стандартных условиях, если нет, то при какой температуре она начнет протекать.
Решение. Чтобы ответить на вопрос о возможности протекания процесса при данных условиях, необходимо найти значение изменения энергии Гиббса химической реакции. Если эта величина отрицательна, то прямой процесс возможен, если положительна, то прямой процесс не возможен, а возможен обратный. Энергия Гиббса связана с другими термодинамическими величинами следующей зависимостью:
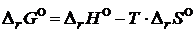
Энтальпия (![]() ) и энтропия реакции (
) и энтропия реакции (![]() ) находятся по следствиям из закона Гесса. Т – абсолютная температура, К. Она связана с температурой по шкале Цельсия (tºC) следующим образом: Т = (tºC + 273)К.
) находятся по следствиям из закона Гесса. Т – абсолютная температура, К. Она связана с температурой по шкале Цельсия (tºC) следующим образом: Т = (tºC + 273)К.
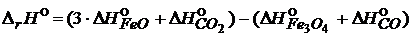
![]() = (3 ∙ (-263,7) + (-393,5)) – ((-1117,7) + (-110,5)) = 43,6 кДж
= (3 ∙ (-263,7) + (-393,5)) – ((-1117,7) + (-110,5)) = 43,6 кДж
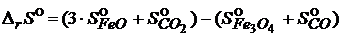 =
=
= (3 ∙ 58,8 + 213,6) – (151,5 + 197,4) = 41,4
По условию задачи необходимо определить возможность процесса при стандартных условиях, что соответствует температуре Т = 298 К.
![]() = 43600 Дж – 298 К ∙ 41,4
= 43600 Дж – 298 К ∙ 41,4 ![]() = 31352,2 Дж > 0
= 31352,2 Дж > 0
Следовательно, прямой процесс при Т = 298 К невозможен.
Найдём температуру, при которой ![]() .
.
Решаем неравенство:
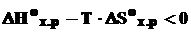 .
.
43600 – 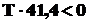
43600 < ![]()
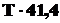 > 43600
> 43600
T > 43600/41,4
T > 1053,14 K
Критическая (равновесная) температура данного процесса 1053,14 К.
Ответ: реакция не возможна при стандартных условиях, а идёт только при T > 1053,14 К.
Задача 5. Реакция восстановления 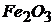 водородом протекает по уравнению
водородом протекает по уравнению ![]() ; ∆Н = +96,61 кДж.
; ∆Н = +96,61 кДж.
Возможна ли эта реакция при стандартных условиях, если изменение энтропии ∆S = 0,1387 ? При какой температуре начнется восстановление 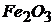 ?
?
Решение. Вычисляем ![]() реакции:
реакции:
∆G = ∆H – T ∙∆ S = 96,61 – 298 ∙0,1387 = +55,28 кДж
Так как ∆G > 0, то реакция при стандартных условиях невозможна; наоборот, при этих условиях идет обратная реакция окисления железа (коррозия). Найдем температуру, при которой ∆G = 0:
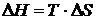 ;
;
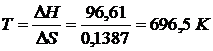 .
.
Следовательно, при температуре ≈ 696,5 К начнется реакция восстановления  . Иногда эту температуру называют температурой начала реакции.
. Иногда эту температуру называют температурой начала реакции.
Ответ: при стандартных условиях реакция невозможна. Восстановление ![]() начнется при 696,5 К.
начнется при 696,5 К.
Связь между изменением свободной энергии Гиббса и константой равновесия выражается уравнением изотермы химической реакции:
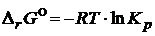 ,
,
где значения кинетической константы равновесия системы при разных температурах соотносятся согласно:
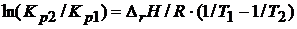
Это выражение позволяет вычислить константу равновесия при одной температуре, если известны значение константы равновесия при другой температуре и тепловой эффект реакции ![]() .
.
2.2. Химическая кинетика
2.2.1. Закон действия масс (закон Гультберга-Вааге)
Закон определяет зависимость скорости химической реакции от концентраций реагирующих веществ. Этот закон называется также основным кинетическим законом.
Пусть уравнение реакции имеет вид:
аА + bВ... = сС + dD,
где буквами a, b, c, d обозначены стехиометрические коэффициенты в уравнении реакции (они могут принимать значения 1, 2, 3, 4...), буквами A, B, C, D – формулы веществ, участвующих в процессе (исходные веществ – слева А и В, и продукты реакции – справа С и D могут быть любыми). Тогда скорость реакции согласно основному кинетическому закону определяется как:
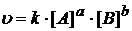 ,
,
где – скорость химической реакции получения C и D из веществ А и В; [A] и [B] – молярные концентрации веществ A и B, единица измерения – 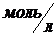 или
или  ; a и b – коэффициенты из уравнения реакции становятся показателями степени; k – константа скорости; она равна скорости реакции при одномолярных концентрациях веществ. Уравнение скорости называется кинетическим уравнением.
; a и b – коэффициенты из уравнения реакции становятся показателями степени; k – константа скорости; она равна скорости реакции при одномолярных концентрациях веществ. Уравнение скорости называется кинетическим уравнением.
2.2.2. Влияние температуры на скорость реакции
Шведским учёным С. Аррениусом установлена зависимость константы скорости реакции (а значит и скорости реакции) от температуры. Полученное им уравнение названо его именем:
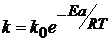 или
или 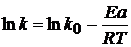 ,
,
где k0 – предэксионенциальный множитель; R – универсальная газовая постоянная (8,31 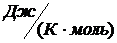 ); Еа – энергия активации реакции (
); Еа – энергия активации реакции (![]() ).
).
Энергия активации реакции – это избыточное количество энергии, которой должны обладать молекулы для того, чтобы их столкновение могло привести к образованию нового вещества (продукта реакции). Значение Еа определяется природой реакции и лежит в пределах 40─400 кДж/моль.
Используя зависимость Аррениуса для определения константы скорости реакции при разных температурах, можно получить уравнение, позволяющее определить либо энергию активации (при известных константах скорости), либо рассчитать отношение констант скорости при двух температурах:
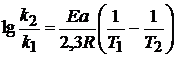 .
.
Здесь k1 и k2 – константы скорости реакции при температурах Т1 и Т2 соответственно; коэффициент 2,3 появляется при переходе от натурального логарифма (ln) и десятичному (lg).
Аппроксимируя сложную зависимость Аррениуса более простой, голландский учёный Вант-Гофф предложил правило, согласно которому повышение температуры на каждые 100С повышает скорость реакции в несколько раз. Это означает, что с ростом температуры увеличивается константа скорости реакции:
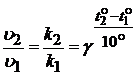 ,
,
где ![]() и
и ![]() – скорости реакции при температурах
– скорости реакции при температурах ![]() и
и ![]() соответственно; k1 и k2 – константы скорости реакции при температурах
соответственно; k1 и k2 – константы скорости реакции при температурах ![]() и
и ![]() ;
; ![]() (гамма) – температурный коэффициент скорости химической реакции. Он показывает, во сколько раз увеличится скорость реакции при повышении температуры на каждые 10°С. Для большинства реакций температурный коэффициент принимает значения от 1,5 до 4.
(гамма) – температурный коэффициент скорости химической реакции. Он показывает, во сколько раз увеличится скорость реакции при повышении температуры на каждые 10°С. Для большинства реакций температурный коэффициент принимает значения от 1,5 до 4.
Согласно правилу Вант-Гоффа величина ![]() для каждой реакции имеет своё значение. Однако на практике это не всегда выполняется. Обычно значение температурного коэффициента уменьшается при повышении температуры. В связи с этим правило рекомендуют использовать лишь для узких диапазонов температур, т. к. в этом случае изменением величины
для каждой реакции имеет своё значение. Однако на практике это не всегда выполняется. Обычно значение температурного коэффициента уменьшается при повышении температуры. В связи с этим правило рекомендуют использовать лишь для узких диапазонов температур, т. к. в этом случае изменением величины ![]() можно пренебречь.
можно пренебречь.
2.2.3. Химическое равновесие. Константа равновесия
В некоторых системах возможны противоположно направленные реакции (обратимые системы):
aA + bB ↔ cC + dD.
В таких системах возможно установление химического равновесия. Это значит, что скорость прямой и обратной реакций выравниваются. Признаком такого состояния системы служит постоянство всех ее свойств во времени, обусловленное постоянством концентраций всех ее компонентов.
Кинетическое уравнение обратимой реакции должно включать в себе уравнения, описывающие скорость как прямой, так и обратной реакции.
Состояние равновесия характеризуется константой равновесия (![]() ):
):
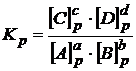 ,
,
где ![]() – равновесные концентрации веществ в системе.
– равновесные концентрации веществ в системе.
Кроме равновесных концентраций для обратимых реакций различают начальные концентрации веществ (![]() ), а также
), а также ![]() – израсходованное (прореагировавшее) количество вещества в единицах концентрации. Это то количество вещества из единицы объема, которое расходуется на образование продуктов.
– израсходованное (прореагировавшее) количество вещества в единицах концентрации. Это то количество вещества из единицы объема, которое расходуется на образование продуктов.
Соотношение между этими концентрациями можно выразить следующим образом:
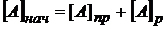
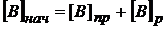
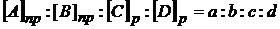 .
.
2.2.4. Смещение химического равновесия. Принцип Ле Шателье
Принцип Ле Шателье определяет, какой процесс (прямой или обратный) будет протекать с большей скоростью при изменениях температуры, концентрации, давления или объема системы.
· При повышении температуры равновесие смещается в сторону эндотермической реакции, а при понижении – в сторону экзотермической реакции.
· При повышении давления (уменьшении объема) равновесие смещается – в сторону образования меньшего числа молекул газообразных веществ и наоборот.
· При увеличении концентрации любого из веществ равновесие смещается в сторону расхода этого вещества, при уменьшении концентрации – наоборот, в сторону образования вещества.
2.2.5. Примеры решения задач
Задача № 1. Некоторое количество диоксида азота (NO2) подверглось разложению до монооксида азота (NO) и кислорода. Равновесие в системе 2NO2 ![]() 2NO + O2 установилось при следующих концентрациях: [NO2] = 0,6
2NO + O2 установилось при следующих концентрациях: [NO2] = 0,6 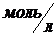 , [NO] = 0,24
, [NO] = 0,24 ![]() . Найти константу равновесия и исходную концентрацию NO2.
. Найти константу равновесия и исходную концентрацию NO2.
Решение:
Выражение константы равновесия для данной системы
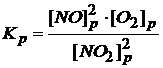
По условию задачи: 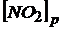 = 0,6
= 0,6 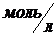 и
и ![]() = 0,24
= 0,24 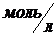 . Найдем
. Найдем ![]() и
и ![]() из соотношения
из соотношения
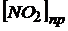 :
: 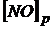 :
: ![]() = 2 : 2 : 1
= 2 : 2 : 1
0,24 : 0,24 : 0,12 = 2 : 2 : 1 (по коэффициентам в уравнении реакции)
Получаем 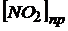 = 0,24
= 0,24 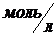 ,
, ![]() = 0,12
= 0,12 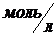 .
.
Подставляем ![]() = 0,12
= 0,12 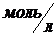 в выражение константы равновесия
в выражение константы равновесия
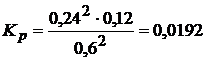
Исходная концентрация NO2
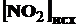 =
= 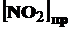 +
+ 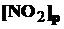
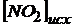 = 0,24 + 0,6 = 0,84
= 0,24 + 0,6 = 0,84 
Ответ: ![]() = 0,0192,
= 0,0192, ![]() = 0,84
= 0,84 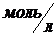 .
.
Задача №2. Константа скорости реакции ![]() равна 0,8. Начальные концентрации веществ А и В равны соответственно 3,5 и 1,9
равна 0,8. Начальные концентрации веществ А и В равны соответственно 3,5 и 1,9 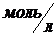 . В результате реакции концентрация вещества В составила 0,5
. В результате реакции концентрация вещества В составила 0,5 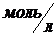 . Какой стала концентрация вещества А и чему равна скорость данной реакции?
. Какой стала концентрация вещества А и чему равна скорость данной реакции?
Решение:
Зависимость скорости реакции от концентрации определяется законом действия масс:
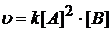 .
.
Чтобы определить скорость реакции, когда [B] = 0,5 ![]() , надо знать концентрацию вещества А в этот момент времени. Константа скорости k = 0,8.
, надо знать концентрацию вещества А в этот момент времени. Константа скорости k = 0,8.
Т. к. вещества В было 1,9 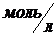 до реакции, а после реакции осталось 0,5
до реакции, а после реакции осталось 0,5 ![]() , то израсходовалось на образование продуктов реакции (вещество С)
, то израсходовалось на образование продуктов реакции (вещество С)
1,9 – 0,5 = 1,4 ![]() .
.
Реакция идет в следующем соотношении:
из двух молей вещества А и 1 моля вещества В образуется 1 моль вещества С. Другими словами из 2 · х вещества А и х вещества В образуется х вещества С, поэтому, зная, что прореагировало вещества B = 1,4 = х, можно найти сколько прореагировало вещества А, 2х = 2,8 ![]() . Тогда концентрация вещества А станет 3,5 – 2,8 = 0,7
. Тогда концентрация вещества А станет 3,5 – 2,8 = 0,7 ![]() .
.
Концентрация в-в, моль/л Состояние | А | В | С |
Исходное | 3,5 | 1,9 | - |
Прореагировало веществ | 2х = 2,8 | х = 1,4 | - |
Конечное | 0,7 | 0,5 | х = 1,4 |
![]() = 0,8 · 0,72 · 0,5 = 0,196
= 0,8 · 0,72 · 0,5 = 0,196
Ответ: [А] = 0,7 ![]() ,
, ![]() = 0,196.
= 0,196.
Задача № 3. Укажите все пути, которыми можно повысить выход аммиака по уравнению 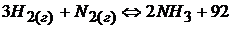 кДж
кДж
Решение:
Для повышения выхода аммиака (NH3) надо сместить равновесие в прямом направлении. На смещение химического равновесия влияют три фактора:
1) Изменение концентрации реагирующих веществ. Чтобы сместить равновесие в прямом направлении надо увеличить концентрации исходных веществ и уменьшить концентрации продуктов реакции. В данном процессе [H2] ↑, [N2] ↑, [NH3] ↓
2) Изменить температуру. Т. к реакция получения аммиака экзотермическая (идет с выделением тепла), то температуру надо понизить (по принципу Ле Шателье).
3) Изменить давление (объем). Этот фактор может сместить равновесие в системе, содержащей газообразные вещества. Если все вещества твердые и жидкие, то этот фактор не влияет на смещение равновесия. Определим число молекул газообразных веществ в прямой (3 + 1 = 4) и обратной (2) реакциях. Т. к. прямая реакция идет с уменьшением объема (4 > 2), то необходимо увеличить давление (уменьшить объем).
Задача № 4. Как измениться скорость прямой реакции
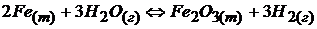 , если увеличить давление в 2 раза.
, если увеличить давление в 2 раза.
Решение: По закону действия масс V = k [Fe]2 · [H2O]3, т. к. концентрация твердого вещества [Fe] = const, то перемножив константы k и [Fe]2 получим новую k’, т. е. V = k,[H2O]3
Увеличение давления в 2 раза (уменьшение объема в 2 раза) приводит к увеличению концентрации газообразных веществ в 2 раза. Тогда V1 = k’·(2[H2O])3 = 8k’ · [H2O]3
Найдем изменение скорости, т. е.
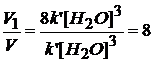
Ответ: скорость увеличится в 8 раз.
Задача № 5
Скорость реакции при -50°С равна 3. Чему равна скорость этой реакции при + 20°С, если температурный коэффициент ![]() = 2,3 ?
= 2,3 ?
Решение:
Соотношение скоростей реакции при разных температурах дает правило Вант – Гоффа.
![]() = -50°С
= -50°С 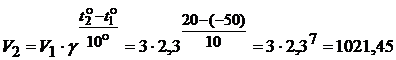
V1 = 3
![]() = + 20°С
= + 20°С
![]() = 2,3
= 2,3
![]()
V2 - ?
Ответ: скорость реакции при t = + 20°С равна 1021,45.
Задача №6
Обратимая реакция выражается уравнением А + В ↔ С + Д, константа равновесия Кр = 1. Начальные концентрации [А] = 2 моль/л; [В] = 3 моль/л. Вычислить равновесные концентрации веществ А, В, С, Д.
Решение:
[А]нач = 2 моль/л Для данной реакции выражение
[В]нач = 3 моль/л 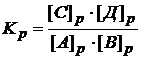
Кр =1 Найдём соотношение концентраций
табличным способом

[А]р, [В]р, [С]р, [Д]р -?
Концентрация в-в, моль/л | А | В | С | Д |
Исходная концентрация | 2 | 3 | 0 | 0 |
Изменение концентрации | -X | -X | +X | +X |
Равновесная концентрация | 2-X | 3-X | 0+X | 0+X |
Из уравнения реакции видно, что из Х моль веществ А и Х моль веществ В получается Х моль вещества С и Х моль вещества Д (все коэффициенты в уравнении реакции единичны). Тогда, зная начальную концентрацию веществ А и сколько прореагировало (Х) можно найти сколько осталось.
[А]р = [А]нач - [А]пр = 2 – Х.
Аналогично находим [В]р = 3 – Х.
Подставляем значения равновесных концентраций в выражение константы равновесия и решаем данное уравнение относительно Х.
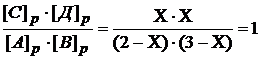
Х·Х = 1· (2 – Х) · (3 – Х)
Х2 = 6 – 2Х – 3Х + Х2
Х2 = Х2 – 5Х + 6
5Х – 6 = 0
Х = 6/5 = 1,2
Зная Х, находим все равновесные концентрации:
[А]р = 2 – Х = 2 – 1,2 = 0,8 моль/л
[В]р = 3 – Х = 3 – 1,2 = 1,8 моль/л

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |



