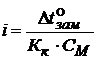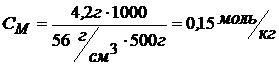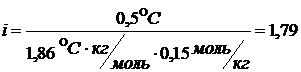[С]р = [Д]р = Х = 1,2 моль/л
Ответ: [А]р = 0,8 моль/л, [В]р = 1,8 моль/л, [С]р = [Д]р = 1,2 моль/л.
Задача 7. Энергия активации разложения NO2
2NO2 2NO + O2
равна 111 кДж/моль. Во сколько раз увеличится константа скорости реакции при повышении температуры с 300 до 400 К?
Решение. Из уравнения Аррениуса следует связь энергии активации и констант скорости:
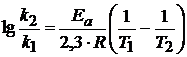
![]() = 111 кДж/моль,
= 111 кДж/моль,
R = 8,314 Дж/(моль ∙ К) – газовая константа,
k1 и k2 константы скорости при температурах 300 и 400 К.
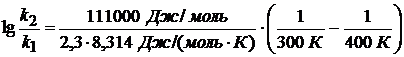

Ответ: константа скорости увеличится в 69183 раза.
3. РАСТВОРЫ И РЕАКЦИИ В ВОДНЫХ РАСТВОРАХ
Раствором называется твёрдая или жидкая гомогенная (однородная) система, состоящая из двух или более компонентов.
3.1. Концентрации растворов
Необходимыми компонентами раствора являются растворитель и растворённое вещество, например, растворённый в воде сахар.
В одном растворителе может находиться несколько растворённых веществ. Например, в воде растворены сахар, соль и уксусная кислота.
Количество растворённого вещества в определённом количестве раствора или растворителя, которое может колебаться в очень широких пределах, называется концентрацией раствора.
3.1.1. Способы задания концентрации растворов
Существует несколько способов выражения концентрации растворов.
Массовая доля растворённого вещества или процентная концентрация (![]() ). Определяется количеством массовых единиц вещества в 100 массовых единицах раствора.
). Определяется количеством массовых единиц вещества в 100 массовых единицах раствора.
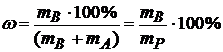 ,
,
где ![]() - масса растворённого вещества;
- масса растворённого вещества; ![]() - масса растворителя;
- масса растворителя;
![]() =
= ![]() +
+ ![]() - масса раствора.
- масса раствора.
Масса может быть определена как произведение плотности раствора на его объём:
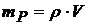
![]() - плотность раствора (г
- плотность раствора (г![]() )
)
V – объём раствора (![]() )
)
![]() (H2O)=1г/см3
(H2O)=1г/см3
Например, в 5%-й растворе 5 г растворённого вещества присутствует в 100 г раствора. Для такого раствора ![]() = 5 г,
= 5 г, ![]() = 100 г – 5 г =95 г.
= 100 г – 5 г =95 г.
Молярная концентрация (молярность) раствора (![]() ). Определяется количеством растворённого вещества (моль) в 1
). Определяется количеством растворённого вещества (моль) в 1 ![]() раствора.
раствора.
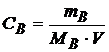 (
( , или
, или 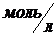 , или М)
, или М)
где ![]() - молярная масса вещества, г/моль; V – объем раствора,
- молярная масса вещества, г/моль; V – объем раствора, ![]()
Например, запись: 0,2M HCl означает, что 0,2 моль HCl растворено в 1 ![]() раствора.
раствора.
Для «чайников»: молярная масса растворённого вещества определяется химическим составом вещества. Например, молекула серной кислоты ![]() образована двумя атомами водорода, одним атомом серы и четырьмя атомами кислорода. Взяв атомные массы этих элементов из таблицы , можно найти молярную массу серной кислоты.
образована двумя атомами водорода, одним атомом серы и четырьмя атомами кислорода. Взяв атомные массы этих элементов из таблицы , можно найти молярную массу серной кислоты. ![]() =
= ![]() = 98 г/моль.
= 98 г/моль.
Молярная концентрация эквивалентов вещества (эквивалентная концентрация, нормальная концентрация, нормальность раствора) (![]() или
или ![]() ). Определяется количеством эквивалентов вещества (в моль-экв) в 1
). Определяется количеством эквивалентов вещества (в моль-экв) в 1 ![]() раствора.
раствора.
![]() =
= 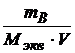 (
(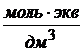 или условно Н)
или условно Н)
Например, запись: 0,5Н 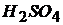 означает, что 0,5 моль эквивалентов серной кислоты содержится в 1
означает, что 0,5 моль эквивалентов серной кислоты содержится в 1 ![]() раствора.
раствора.
Под молярной массой эквивалентов вещества понимают такое его количество, которое соединяется с одним молем атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Например, для соединений HCl, ![]() молярные массы эквивалентов равны соответственно М (HCl), 0,5 М(
молярные массы эквивалентов равны соответственно М (HCl), 0,5 М(![]() ).
).
Молярная масса эквивалента кислоты – это частное от деления молярной массы кислоты на количество ионов водорода, участвующих в реакции:
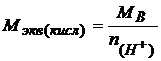 .
.
Например: 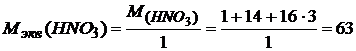 г/
г/![]() ;
;
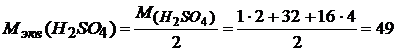 г/
г/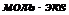 .
.
Молярная масса эквивалентов основания – это частное деления молярной массы основания на количество гидроксид-ионов в формуле основания:
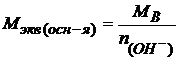
Например: 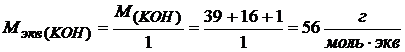
![]()
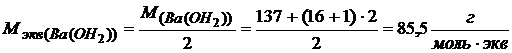
Молярная масса эквивалентов соли – это частное от деления молярной массы соли на произведение валентности металла соли на количество частиц металла в формуле соли:
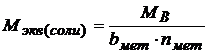
Например: 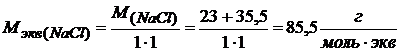

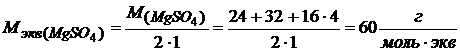
Моляльная концентрация (моляльность раствора)(![]() ). Определяется количеством растворённого вещества (моль) в 1кг растворителя.
). Определяется количеством растворённого вещества (моль) в 1кг растворителя.
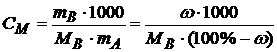 (
(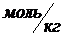 )
)
Титр раствора (Т). Определяется массой растворённого вещества в 1 ![]() раствора.
раствора.
Т= ![]() (
(![]() или
или ![]() ).
).
3.1.2. Закон эквивалентов
Закон эквивалентов утверждает, что если два раствора взаимодействуют между собой в эквивалентных количествах, то зная концентрацию одного из растворов и прореагировавшие объемы обоих растворов, можно рассчитать концентрацию второго раствора по соотношению:
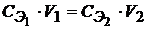 .
.
3.1.3. Пример решения задачи
Дан раствор серной кислоты с концентрацией 10%. Плотность данного раствора равна 1,075 г/![]() . Рассчитать моляльную, молярную концентрацию эквивалентов, концентрацию раствора.
. Рассчитать моляльную, молярную концентрацию эквивалентов, концентрацию раствора.
Решение:
Рассчитаем молярную концентрацию. Для этого произвольно выберем объём раствора.
Пусть V=1![]() =1000
=1000 ![]() , масса этого раствора
, масса этого раствора 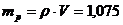 г/
г/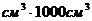 = 1075
= 1075
Так как для раствора ![]() = 10%, то масса кислоты составляет 10% от массы раствора:
= 10%, то масса кислоты составляет 10% от массы раствора:
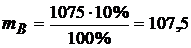 г.
г.
Отсюда:
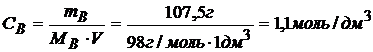 (М)
(М)
Рассчитаем моляльную концентрацию. Так как мы взяли 1![]() раствора, масса которого 107,5 г, а масса кислоты в этом объеме 107,5 г, то масса растворителя (воды):
раствора, масса которого 107,5 г, а масса кислоты в этом объеме 107,5 г, то масса растворителя (воды):
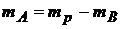
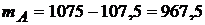 г
г
Рассчитаем эквивалентную концентрацию:
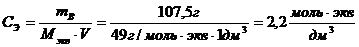 (H)
(H)
Рассчитаем титр раствора:
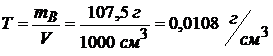 .
.
Ответ: моляльная концентрация составила 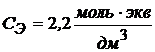 ; молярная концентрация получилась
; молярная концентрация получилась ![]() ; титр раствора -
; титр раствора - 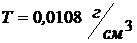 .
.
3.2. Теория растворов
3.2.1. Давление пара растворов
При данной температуре давление насыщенного пара над каждой жидкостью – величина постоянная. Французский физик Рауль установил, что давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем при той же температуре (I закон Рауля). Математическим выражением закона является уравнение:
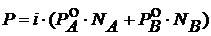 ,
,
где ![]() – давление насыщенного пара над чистым растворителем;
– давление насыщенного пара над чистым растворителем; ![]() – давление насыщенного пара над растворенным веществом; NA – мольная доля вещества растворителя; NB – мольная доля растворенного вещества.
– давление насыщенного пара над растворенным веществом; NA – мольная доля вещества растворителя; NB – мольная доля растворенного вещества.
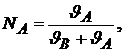
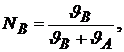
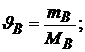
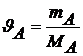 .
.
![]() – количество растворенного вещества (моль);
– количество растворенного вещества (моль);
![]() – количество растворителя (моль);
– количество растворителя (моль);
mB – масса растворённого в растворе вещества (г);
МВ – молярная масса вещества (г/моль);
mА – масса растворителя в растворе (г);
МА – молярная масса вещества растворителя (г/моль);
i – изотонический коэффициент раствора.
i = 1 для растворов неэлектролитов (такими являются большинство органических соединений, например, сахароза С12Н22О11, глюкоза С6Н12О6, глицерин С3Н8О3 и т. п.).
1 < i < n для растворов электролитов (соли, кислоты, основания), где n – число ионов, на которые диссоциирует молекула растворенного электоролита.
Например для: AgNO3 Ag+ + n = 2
H2SO4 ![]() 2H+ +
2H+ +![]() n = 3
n = 3
FeCl3 ![]() Fe3+ + 3Cl─ n = 4
Fe3+ + 3Cl─ n = 4
Al2(SO4)3 2Al3+ + 3![]() n = 5
n = 5
Чем меньше концентрация раствора, тем ближе значение i к значению n. При увеличении концентрации значение i уменьшается.
Если растворенное вещество – не летучее, то для него ![]() = 0 и выражение для I закона Рауля принимает вид:
= 0 и выражение для I закона Рауля принимает вид:
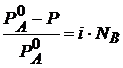 .
.
3.2.2. Кипение и замерзание растворов
Температура кипения раствора всегда выше, а температура его замерзания всегда ниже, чем для чистого вещества растворителя. Рауль установил, что понижение температуры замерзания раствора (![]() ) и повышение температуры его кипения (
) и повышение температуры его кипения (![]() ) пропорциональны мольно-массовой концентрации раствора. Это соотношение называется II законом Рауля и математически определяется как:
) пропорциональны мольно-массовой концентрации раствора. Это соотношение называется II законом Рауля и математически определяется как:
∆t°кип = t°кип р-ра - t°кип р-ля = i · kэ · СМ;
∆t°зам = t°зам р-ля - t°зам р-ра = i · kк · СМ;
где t°кип р-ра – температура кипения раствора;
t°кип р-ля – температура кипения растворителя (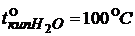 );
);
t°зам р-ра – температура замерзания раствора;
t°зам р-ля – температура замерзания растворителя (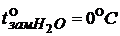 );
);
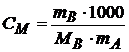 (моль/кг) – моляльная концентрация раствора;
(моль/кг) – моляльная концентрация раствора;
![]() – эбулиоскопическая постоянная вещества растворителя;
– эбулиоскопическая постоянная вещества растворителя;
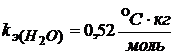 (для растворителя – воды);
(для растворителя – воды);
![]() – криоскопическая постоянная вещества растворителя;
– криоскопическая постоянная вещества растворителя;
 (для растворителя – воды).
(для растворителя – воды).
3.2.3. Осмос. Осмотическое давление
Односторонняя диффузия вещества растворителя через полупроницаемую мембрану называется осмосом. Давление, обеспечивающее такое перемещение называется осмотическим (![]() ). Голландский физико-химик Вант-Гофф показал зависимость величины осмотического давления от концентрации и температуры раствора:
). Голландский физико-химик Вант-Гофф показал зависимость величины осмотического давления от концентрации и температуры раствора:
Pосм = i · CB · R · T кПа,
где Pосм – осмотическое давление (760 мм. рт. столба = 1 атм. = 101,325 кПа); CB – молярная концентрация (молярность) раствора; R – универсальная газовая постоянная; Т – абсолютная температура (К).
T = t°С + 273 (t° – температура в шкале Цельсия).
3.2.4. Количественные характеристики растворов электролитов. Закон растворения
Все электролиты в зависимости от степени диссоциации (![]() ) делятся на сильные, слабые и электролиты средней силы. Степень диссоциации определяется как:
) делятся на сильные, слабые и электролиты средней силы. Степень диссоциации определяется как:
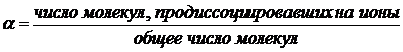
![]() ≥ 0,33 для сильных электролитов. К сильным электролитам относятся сильные кислоты (HCl, HClO3, HClO4, HBr, HI, HIO3, H2SO4, HNO3, H2CrO4, H2Cr2O7, HMnO4, H2MnO4), сильные основания (NaOH, KOH, Ca(OH)2, Ba(OH)2, LiOH) и растворы солей.
≥ 0,33 для сильных электролитов. К сильным электролитам относятся сильные кислоты (HCl, HClO3, HClO4, HBr, HI, HIO3, H2SO4, HNO3, H2CrO4, H2Cr2O7, HMnO4, H2MnO4), сильные основания (NaOH, KOH, Ca(OH)2, Ba(OH)2, LiOH) и растворы солей.
Диссоциация сильных электролитов характеризуется кажущейся степенью диссоциации:
 (в отн. единицах, если умножить на 100%, то в %).
(в отн. единицах, если умножить на 100%, то в %).
![]() < 0,02 для слабых электролитов. К слабым электролитам относятся слабые кислоты (HF, HClO, HClO2, HNO2, H2S, H2SO3, H2S2O3, H3PO4, H2CO3, HCN, CH3COOH и др.), слабые основания (NH4OH, Fe(OH)2, Zn(OH)2, Cu(OH)2, Pb(OH)2, Mg(OH)2 и т. д.) и растворы некоторых солей, например HgCl2, Fe(CNS)3.
< 0,02 для слабых электролитов. К слабым электролитам относятся слабые кислоты (HF, HClO, HClO2, HNO2, H2S, H2SO3, H2S2O3, H3PO4, H2CO3, HCN, CH3COOH и др.), слабые основания (NH4OH, Fe(OH)2, Zn(OH)2, Cu(OH)2, Pb(OH)2, Mg(OH)2 и т. д.) и растворы некоторых солей, например HgCl2, Fe(CNS)3.
Электролиты с 0,02 ≤ ![]() < 0,33 являются электролитами средней силы. Таких веществ не много. Типичным примером является фтористоводородная (плавиковая) кислота HF.
< 0,33 являются электролитами средней силы. Таких веществ не много. Типичным примером является фтористоводородная (плавиковая) кислота HF.
Кинетическая константа равновесия процесса диссоциации слабого электролита называется его константой диссоциации (![]() ).
). ![]() – справочная характеристика вещества слабого электролита.
– справочная характеристика вещества слабого электролита.
Степень диссоциации слабого электролита связана с его константой диссоциации законом разбавления (законом Оствальда):
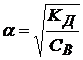
При ступенчатой диссоциации электролита каждая ступень характеризуется своей константой диссоциации и значением степени диссоциации:
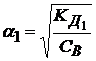 (I ступень диссоциации)
(I ступень диссоциации)
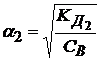 (II ступень диссоциации)
(II ступень диссоциации)
Типичная ошибка: поиск ![]() и использование закона растворения для сильных электролитов.
и использование закона растворения для сильных электролитов.
3.2.5. Произведение растворимости. Условие образования осадка
Для веществ труднорастворимых электролитов существует количественная мера их растворимости – произведение растворимости (ПР).
ПР – это произведение в насыщенном растворе молярных концентраций ионов, на которые диссоциирует молекула труднорастворимого электролита. Значения произведений растворимости труднорастворимых веществ (при комнатной температуре) приведены в справочных таблицах. Например,
для AgCl Ag+ + Cl─, ПР = [Ag+]Н ∙ [Cl─]Н = 1,78 ∙ 10─10;
для BiI3 Bi3++ 3I─, ПР = = 8,1 ∙ 10─19.
Индекс «н» у символа концентрации определяет отношение концентрации к насыщенному раствору. Таким образом для любого труднорастворимого вещества состава AnBm, диссоциирующего по схеме:
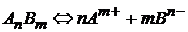 ,
,
ПР = .
Поскольку осадок выпадает из пересыщенных растворов, то условием образования осадка является превышение произведения молярных концентраций ионов труднорастворимого вещества в конкретном растворе над величиной ПР, т. е. 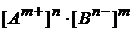 > ПР(AnBm)таб.
> ПР(AnBm)таб.
3.2.6. Примеры решения задач
Задача № 1.
Найти степень диссоциации гидроксида калия, если раствор, содержащий 4,2 г вещества и 0,5 дм3 воды, замерзает при -0,5°С.
Дано: mB = 4,2 г Vводы = 0,5 дм3 t°зам р-ра = - 0,5°С - αкаж - ? | Решение: КОН → К+ + ОН - → n = 2 – сильный электролит
∆t°зам = i · kк · СМ
∆t°зам = 0°C – (-0,5°C) = 0,5°C
MKOH = 39 + 16 + 1 = 56 г/моль
1<1,79<2
|
Ответ: кажущаяся степень диссоциации 0,79 или 79%.
Задача № 2
Определить степень диссоциации уксусной кислоты в 0,5 М растворе.
Дано: СВ = 0,5 М = 0,5 моль/дм3
α - ? | Решение: СН3СООН – слабая кислота Для слабых электролитов В приложении 3 находим значение константы диссоциации для уксусной кислоты КД = 1,74 · 10─5
|
Ответ: степень диссоциации 5,9 · 10─3.
Задача № 3
Выпадет ли осадок, если смешать 3 см3 0,000005 М раствора серной кислоты и 4 см3 0,00002 М раствора хлорида бария.
Решение:
H2SO4 + BaCl2 = BaSO4 ↓ + 2HCl
3 см3 + 4 см3 = 7 см3
Осадок выпадет в том случае, если концентрация получившегося в ходе реакции сульфата бария больше, чем в насыщенном растворе.
BaSO4 →Ba2+ + ![]()
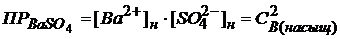 ,т. к.
,т. к. 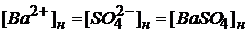
ПРтаб = 1,1 · 10─10 (значение взято в приложении 4)
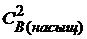 = 1,1 · 10─10
= 1,1 · 10─10
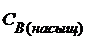 = 1,05 · 10─5 моль/дм3
= 1,05 · 10─5 моль/дм3
Найдем концентрации ионов бария и сульфат – ионов. Ионы бария содержатся в 4 см3 0,00002 М раствора хлорида бария, при добавлении 3 см3 0,000005 М раствора серной кислоты объем стал равен 7 см3 и концентрация ионов бария
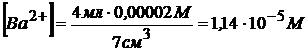
Концентрацию сульфат – ионов находим аналогично
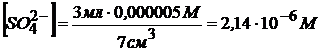
т. к. 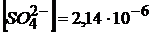 <СВ (насыщ) = 1,05 · 10─5 М осадок не выпадет.
<СВ (насыщ) = 1,05 · 10─5 М осадок не выпадет.
Ответ: осадок не выпадет
Задача № 4
В каком объеме может быть растворено 3 г иодида свинца (II).
Решение:
Чтобы найти объем насыщенного раствора PbI2, в котором содержится 3 г соли, надо знать концентрацию насыщенного раствора.
PbI2 → Pb2+ + 2I─
CB(насыщ) CB(насыщ) 2CB(насыщ)
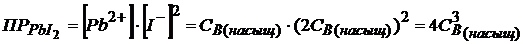
ПРтаб = 1,1 · 10─9 (значение взято в приложении 4)
4![]() = 1,1 · 10─9
= 1,1 · 10─9
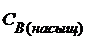 = 6,5 · 10─4 моль/дм3
= 6,5 · 10─4 моль/дм3
 ,
,
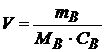
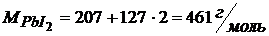
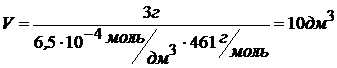
Ответ: 3 г иодида свинца можно растворить в 10 дм3 раствора.
Задача № 5
Степень диссоциации 0,1 Н раствора карбоната натрия при 0°С равна 70%. Вычислить осмотическое давление раствора.
Дано: Решение:
Na2CO3 По закону Вант-Гоффа
CЭ = 0,1 H
t º= 0ºC Росм = i · CB · R · T
αкаж = 70% = 0,7 R = 8,314 Дж/моль∙ К (универсальная газовая постоянная)
![]() T = t° + 273 = 0 + 273 = 273 K
T = t° + 273 = 0 + 273 = 273 K
Росм - ? СВ – молярная концентрация раствора, а в
условиях задачи дана нормальная концентрация, поэтому необходимо выполнить следующий расчет.
 , а
, а 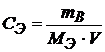 , поэтому
, поэтому
СВ · МВ = СЭ · МЭ, а 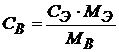
Найдем молярную и эквивалентную массу карбоната натрия
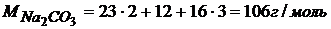
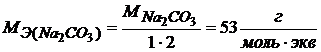 , где
, где

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |