СБОРНИК ОПИСАНИЙ ЛАБОРАТОРНЫХ РАБОТ
Лабораторная работа № 1
Приготовление раствора и определение его концентрации титрованием
Цель работы:
1. Приобретение навыков приготовления растворов из более концентрированного раствора.
2. Ознакомление с титрованием растворов.
Выполните расчет:
определите, сколько миллилитров раствора серной кислоты (концентрацией 12%, плотностью 1,083 г/мл) потребуется для приготовления 100 мл раствора ![]() заданной нормальности. Нормальная концентрация раствора задается преподавателем каждому студенту.
заданной нормальности. Нормальная концентрация раствора задается преподавателем каждому студенту.
Ход работы:
1. Приготовьте раствор серной кислоты. Для этого налейте в плоскодонную колбу объемом 100 мл небольшое количество (20-50 мл) дистиллированной воды. Налейте в мерительную пробирку рассчитанное количество миллилитров 12% серной кислоты и перелейте ее в колбу с водой. Закройте колбу притертой пробкой и, встряхивая колбу, перемешайте раствор. Долейте дистиллированную воду до калибровочной риски колбы (100 мл).
2. В каждую из двух конических колб налейте по 20 мл приготовленного раствора серной кислоты. Измерение объема выполняйте мерным цилиндром. Добавьте в каждую колбу капель раствора фенолфталеина.
3. Бюретку заполните 0,1 Н раствором NaOH немного выше верхней (нулевой) отметки. Нажимая на стеклянный шарик в резиновой трубочке бюретки, установите мениск раствора на нулевой отметке.
4. Титрование выполняйте следующим образом: к 20 мл раствора H2SO4 приливайте 0,1Н раствор NaOH, нажимая на стеклянный шарик в резиновом наконечнике бюретки. Добавляемую в кислоту щелочь непрерывно размешивайте круговыми движениями конической колбы. После появления первой окраски (исчезающей при перемешивании), раствор NaOH добавляйте по каплям.
Как только окраска раствора стала бледно-розовой, титрование прекратите. Возьмите отсчет по шкале бюретки объема раствора NaOH, израсходованного на титрование. Запишите результат первого титрования Vщ1 = … мл.
Долейте раствор NaOH до нулевой отметки бюретки и оттитруйте раствор H2SO4 во второй колбе. Запишите результат второго титрования Vщ2 = … мл.
Найдите среднее арифметическое значение результатов двух титрований Vщ (ср). Это объем NaOH, необходимый для титрования 20 мл приготовленного раствора кислоты.
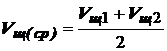
5. Рассчитайте по данным титрования значение нормальной концентрации приготовленного раствора кислоты. Расчет выполняйте по закону эквивалентов:
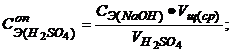
6. Рассчитайте погрешность опыта:
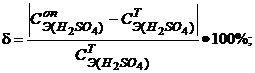
7. Вычислите титр приготовленного раствора.
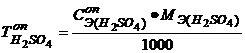
8. Все результаты сведите в таблицу. Сформулируйте вывод по результатам работы.
Содержание отчёта
Отчет должен содержать:
1. Все необходимые расчеты;
2. Таблицу приведенной ниже формы;
3. Вывод.
Таблица исходных данных и полученных результатов
| V12% H2SO4, мл |
| Объём раствора NaOH (щелочи), израсходованного на титрование |
| δ, % |
г/мл | ||
|
|
| ||||||
20 |
Лабораторная работа № 2
Зависимость скорости реакции от концентрации раствора и температуры
Опыт 1.
Цель опыта: установить зависимость скорости химической реакции от концентрации
реагирующих веществ.
Химические реактивы: сульфит натрия Na2SO3, подкисленный H2SO4; крахмал (внесен в раствор Na2SO3); иодат калия KIO3; дистиллированная вода.
Химическая посуда и оборудование: секундомер, мерительные цилиндры, химические стаканы.
Ход работы:
Скорость реакции в зависимости от концентрации исследуется на примере:
2KIO3 + 5Nа2SO3 + H2SO4 = K2SO4 + 5Na2SO4 + I2 + H2O
Приготовьте растворы иодата калия трех различных концентраций. Для этого отмерьте цилиндром 30 мл KIO3 и перелейте в стакан № 1. Затем отмерьте 20 мл KIO3, перелейте в стакан № 2 и добавьте туда же 10 мл Н2О. В третий стакан отмерьте 10 мл KIO3 и добавьте туда 20 мл Н2О. Воду отмерять тем же цилиндром, что и раствор KIO3 . Затем другим цилиндром отмерьте 30 мл Na2SO3.
Раствор Na2SO3 быстро прилейте в стакан № 1, одновременно с приливанием включите секундомер. В момент окончания реакции ( резкое изменение цвета раствора ) – выключите секундомер. Запишите в таблицу время, прошедшее с момента сливания растворов до появления синего окрашивания. Аналогично измерьте время реакции для стаканов № 2 и № 3, также быстро прилив туда по 30 мл сульфита натрия.
Заполните таблицу:
Опыт | Раствор / объем, мл | Относительная концентрация | Время реакции, с | Относительная скорость | ||
Na2SO3 | KIO3 | H2O | ||||
1 | 30 | 30 | 0 | 1,00 | ||
2 | 30 | 20 | 10 | 0,67 | ||
3 | 30 | 10 | 20 | 0,33 |
Относительную скорость (V) рассчитайте как Сотн. / t (относительная концентрация ко времени реакции).
Постройте график, откладывая по горизонтальной оси концентрации, а по вертикальной оси - относительную скорость реакции.
Сделайте вывод, основываясь на законе действия масс. Соответствует ли ваш график этому закону?
Опыт 2.
Цель опыта: установить зависимость скорости химической реакции от температуры.
Химические реактивы: тиосульфат натрия Na2S2O3, серная кислота H2SO4.
Химическая посуда и оборудование: секундомер, мерительные цилиндры, химические стаканы, пробирки, термометр.
Ход работы:
Скорость реакции в зависимости от температуры исследуется на примере:
Nа2S2O3 + H2SO4 = Na2SO4 + H2SO3 + S
Отмерьте мерительной пробиркой 3 раза по 3 мл H2SO4 и перелейте в три химические пробирки. Другой мерительной пробиркой также 3 раза по 3 мл отмерьте раствор Na2S2O3 и перелейте в 3 другие химические пробирки. Сгруппируйте пробирки в три пары (кислота – тиосульфат натрия).
Измерение 1. Возьмите первую пару пробирок и слейте оба раствора вместе. В момент сливания включите секундомер. При появлении слабой опалесценции выключите секундомер. Запишите в таблицу время реакции (“t, c”). Температура растворов равна комнатной, поэтому в графу “t0 c” запишите эту температуру по вашему термометру.
Измерение 2. Вторую пару пробирок поместите в стакан с теплой водой, предварительно опустив в одну из пробирок термометр. Как только температура одного из растворов станет на 10 0С выше температуры первого опыта, уберите термометр и быстро слейте содержимое пробирок. Время реакции запишите в таблицу.
Измерение 3. Проводится аналогично, но температуру третьей пары пробирок нужно установить на 10 0С выше температуры второго опыта.
Измере- ние | t,0C | Время, c | Относительная скорость | Температурный коэффициент |
1 | ||||
2 | ||||
3 |
Относительную скорость рассчитайте по формуле: 1/t. Определите температурный коэффициент ( ![]() ).
).
Сделайте вывод о влиянии температуры на скорость изученной реакции.
Лабораторная работа № 3
Гидролиз солей и рН-метрия растворов
Цель работы: ознакомиться с гидролизом трех типов солей;
научиться составлять уравнения гидролиза;
познакомиться с методами определения водородного показателя (рН) водных растворов разной природы.
Опыт1. Окраска индикаторов в различных средах.
Возьмите 9 пробирок. Налейте в 3 пробирки по 1 мл. дистиллированной воды. В следующие 3 пробирки по 1 мл. 0,1 Н раствора NaOH, еще в 3 пробирки по 1 мл. 0,1 Н раствора HCl. В одну пробирку с водой, в одну с раствором щелочи и в одну с раствором кислоты добавьте по 1 – 2 капли раствора метилоранжа. Аналогично в три другие пробирки добавьте по 1 - 2 капли раствора фенолфталеина. И в оставшиеся 3 пробирки добавьте по 1 – 2 капли раствора лакмуса. Составьте таблицу окраски индикаторов в различных средах.
Опыт 2. Количественное определение рН раствора.
В пять пробирок налейте по 1 мл.: в одну 0,1 Н раствора соляной кислоты, в другую 0,1 Н раствора уксусной кислоты, в третью 0,1 Н раствора аммиака, в четвертую 0,1 Н раствора гидроксида натрия и в пятую – дистиллированной воды.
В каждую пробирку опустите ½ полоски индикаторной бумаги. Окраску индикаторной бумаги сравните с эталонной шкалой. Результаты определения рН запишите в таблицу.
Опыт 3. Гидролиз солей.
В четыре пробирки налейте по 1 мл.: в одну дистиллированной воды, в другую раствор Na2CO3, в третью – ZnCl2, в четвертую – KCl. В каждую из пробирок прилейте по 1 – 2 капли фиолетового раствора лакмуса и сравните окраску лакмуса в воде и в растворах солей.
Какие из испытуемых солей подверглись гидролизу? Составьте уравнение гидролиза.
Опыт 4. Гидролиз соли слабого основания и слабой кислоты.
К 1 мл. раствора сульфата алюминия прилейте 1 мл. раствора Na2CO3. Напишите молекулярное и ионное уравнения взаимодействия солей.
Какая из образовавшихся солей не подвергается гидролизу, а какая подвергается полному необратимому гидролизу? Составьте молекулярное уравнение полного необратимого гидролиза этой соли.
Опыт 5. Растворение металла в продукте гидролиза его соли.
Опустите кусочек цинка в пробирку с раствором хлорида цинка и нагрейте пробирку в горячей воде. Чем объяснить выделение водорода? Ответ подтвердите уравнениями реакций.
Лабораторная работа № 4
Окислительно-восстановительные реакции (ОВР)
Цель работы: приобретение навыков уравнивания окислительно - восстановительных реакций методом электронно-ионного баланса.
Ход работы: провести следующие три опыта, отметить цвет всех растворов до реакции и после. Определить коэффициенты в уравнениях ОВР методом электронно-ионного баланса.
Опыт 1.
В пробирку налить 1 мл 0,005 М раствора перманганата калия КМnO4. Затем прилиить1 мл 20 % раствора серной кислоты H2SO4 и 2 мл 0,5 Н раствора нитрита натрия NaNO2 или нитрита калия КNO2. Отметить изменения, происшедшие в результате реакции. Уравнять ОВР:
КМnO4 + H2SO4 + NaNO2 ® NaNO3 + MnSO4 + K2SO4 + Н2О
Опыт 2.
В пробирку налить 1 мл 0,005 M раствора перманганата калия KMnO4. Затем прилить 1 мл 2 H раствора соляной кислоты HCl и 2 мл 3 % раствора пероксида водорода H2O2. Отметить изменения, происшедшие в ходе реакции. Уравнять ОВР:
KMnO4 + HCl + H2O2 ® KCl + MnCl2 + H2O + O2
Опыт 3.
В большую пробирку поместить несколько кристалликов сульфата железа (II) FeSO4. Вместо сульфата железа можно использовать соль Мора. Затем прилить 2 мл 20 % раствора серной кислоты H2SO4. После полного растворения соли добавить 1 мл 0,005 М раствора перманганата калия KMnO4. Отметить изменения, происшедшие в результате реакций. Уравнять ОВР:
FeSO4 + H2SO4 + KMnO4 ® MnSO4 + Fe2(SO4)3 + K2SO4 + Н2О
Лабораторная работа № 5
ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ И ЭЛЕКТРОЛИЗ
Цель работы: Ознакомление с устройством гальванических элементов и электролизом растворов электролитов.
Опыт 1. Работа гальванического элемента Якоби-Даниэля.
В один химический стакан налить не менее ½ объема 1 М раствор сульфата меди, в другой не менее ½ объема 1 М раствор сульфата цинка. Собрать гальванический элемент и измерить его ЭДС вольтметром. Сделать рисунок гальванического элемента, написать его электрохимическую схему и реакции, протекающие на электродах (в ионном виде). Рассчитать ЭДС данного гальванического элемента.
Опыт 2. Концентрационный гальванический элемент.
Записать электрохимическую схему концентрационного гальванического элемента на основе двух металлических электродов (электроды определяет преподаватель). Составить уравнения реакций, протекающих на электродах (в ионном виде). Рассчитать теоретическое значение ЭДС данного гальванического элемента.
Опыт 3. Электролиз раствора хлорида меди (II).
Налейте в U-образную трубку 0,5 М раствор хлорида меди (II) примерно до половины обьема. Вставьте в оба колена трубки графитовые электроды. Присоедините электроды к источнику постоянного тока и пропускайте ток около 5 минут. Выключите ток и рассмотрите катод, убедитесь в том, что на нем выделилась медь. Составьте схему электролиза и уравнения реакций, протекающих на электродах.
Опыт 4. Электролиз раствора сульфата натрия.
Налейте в U-образную трубку 0,5 М раствор сульфата натрия. Измерьте с помощью универсальной индикаторной бумаги реакцию раствора (если цвет бумаги не меняется, раствор имеет нейтральную реакцию, рН = 7). Погрузите в трубки графитовые электроды. Включите ток и пропускайте его около 5 минут. Наблюдайте выделение пузырьков газа на электродах. Выньте один электрод из трубки и прикоснитесь к нижнему концу электрода полоской индикаторной бумаги. Если она окрашивается в красноватый цвет – реакция раствора кислая (рН<7), если в зеленоватый – щелочная (рН>7). Отметьте реакцию раствора у анода и катода. Составьте схему электролиза и уравнения реакций, протекающих на электродах.
Опыт 5. Электролиз раствора серной кислоты с медным анодом.
Налейте в U-образную трубку 1 М раствор серной кислоты. Вставьте в оба колена трубки электроды, один графитовый, другой медный. Графитовый электрод соедините с катодом, а медный – с анодом источника тока. Включите ток. Во время электролиза наблюдайте за процессом, протекающим на катоде. Обратите внимание на то, что в начале опыта на катоде выделяются пузырьки газа, затем по мере окрашивания раствора в голубой цвет скорость выделения газа уменьшается и одновременно катод начинает покрываться слоем меди. Дайте объяснение этим явлениям и составьте уравнения реакций, протекающих на аноде и катоде.
СБОРНИК КОНТРОЛЬНЫХ ЗАДАНИЙ
. Контрольная работа 1. Способы выражения концентрации растворов. Расчёты концентраций растворов.
Вариант 1
1. К 1000 г 80%-ной уксусной кислоты прибавлено 3л воды. Найти процентную концентрацию раствора.
2. Сколько граммов нитрата алюминия содержится в 3 л 2 Н раствора этой соли?
3. Рассчитать нормальность раствора 20%-ной серной кислоты плотностью 1,14 г/мл.
4. Сколько граммов фосфорной кислоты надо взять для приготовления 500 мл 0,02 Н раствора?
5. На реакцию с хлоридом калия, содержащимся в 10 мл раствора, израсходовано 45 мл 0,02 Н раствора нитрата серебра. Сколько хлорида калия содержится в 1 литре раствора?
Вариант 2
1. Определить процентную концентрацию 6 Н раствора серной кислоты, если плотность раствора равна 1,18 г/мл?
2. Сколько мл 70%-го раствора нитрата калия плотностью 1,6 г/мл нужно взять, чтобы приготовить 0,5 л 0,2 Н раствора?
3. Определить титр раствора гидроксида натрия, если на титрование 20 мл его потребовалось 50 мл 0,3 Н раствора соляной кислоты?
4. Сколько граммов сульфата меди нужно взять для приготовления 400 мл 0,6 Н раствора?
5. Для полной нейтрализации 1 г некоторой двухосновной кислоты потребовалось 111,1 мл 0,2 Н раствора гидроксида натрия. Найти молекулярную массу кислоты.
Вариант 3
1. Сколько граммов 10-ти водного сульфата натрия нужно растворить в 250 г воды для получения 5%-го раствора безводной соли?
2. Определить молярность раствора фосфорной кислоты, если 6 г её содержится в 150 мл раствора.
3. Рассчитать молярность раствора азотной кислоты, концентрацией 23,3% и плотностью 1,14 г/мл.
4. Сколько мл 70%-го раствора нитрата калия, плотность которого 1,6 г/мл, нужно взять для приготовления 0,5 л 0,2 Н раствора?
5. Сколько мл воды приходится на 28 г КОН в его 1 моляльном растворе?
Вариант 4
1. Вычислить нормальность 50%-го раствора гидроксида натрия плотностью 1,54 г/мл.
2. Сколько мл 20%-го раствора азотной кислоты плотностью 1,115 г/мл, потребуется для нейтрализации раствора, содержащего 16 г гидроксида натрия?
3. Вычислить молярность 10%-го раствора азотной кислоты плотностью 1,056 г/мл.
4. Сколько мл 0,12 Н раствора соляной кислоты потребовалось для полной нейтрализации 15 мл 0,1 Н раствора гидроксида натрия?
5. Определить титр 10% раствора КОН, плотность которого 1,09 г/мл.
Вариант 5
1. В 100 г воды содержится 114,1 г хлорида кадмия. Вычислить процентную и моляльную концентрацию раствора.
2. Вычислить нормальную концентрацию раствора иодида калия, 1 мл которого содержит 0,0017 г иодида калия.
3. Рассчитайте моляльность 40%-го раствора хлорида магния.
4. Сколько граммов серной кислоты содержится в 1 мл 0,1 Н раствора?
5. Сколько граммов хлорида натрия нужно растворить в 500 г воды, чтобы получить 0,5 моляльный раствор?
Контрольная работа 2. Термодинамический расчет химической реакции.
вариант 1
Вычислите при какой температуре начнется диссоциация пентахлорида фосфора, протекающая по уравнению:
PCl5(г) = PCl3(г) + Cl2(г)
вариант 2
Вычислите изменение энергии Гиббса реакции, протекающей по уравнению:
СО(Г) + 3Н2(Г) = СН4(Г) + Н2О(Г). Возможна ли эта реакция при температуре минус 70 0С?
вариант 3
Определить ![]() G0298 реакции, протекающей по уравнению:
G0298 реакции, протекающей по уравнению:
4NH3(г) + 502(г) = 4NO(г) + 6H2O(г) .Вычисления сделать на основании ![]() Н0 и S0 соответствующих веществ. Возможна ли эта реакция при стандартных условиях?
Н0 и S0 соответствующих веществ. Возможна ли эта реакция при стандартных условиях?
вариант 4
Рассчитайте тепловой эффект (кДж) реакции взаимодействия 3 литров водорода с кислородом.
вариант 5
Рассчитайте тепловой эффект (кДж) реакции взаимодействия 10 м3 водорода с кислородом.
Контрольная работа 3. Кинетический расчет химической реакции.
ВАРИАНТ 1
1. Константа скорости реакции 2A(ж) + B(ж) <==> C(ж) равна 0,8. Начальные концентрации веществ А и В равны соответственно 2,5 и 1,5 моль/л. В результате реакции концентрация вещества В составила 0,5 моль/л. Какой стала концентрация вещества А и чему стала равна скорость данной реакции?
2. Перечислить все факторы, которыми можно увеличить выход SO3 по реакции:
2SO2(г) + O2(г) <==> 2SO3(г) + 192 кДж.
3. Скорость реакции при tо = 20 оС равна 1. Чему равна скорость этой реакции при tо = 50 C, если ![]() = 3,5 ?
= 3,5 ?
ВАРИАНТ 2
1. Равновесная концентрация вещества В составляет 5 моль/л. Какое количество вещества А вступает в реакцию, если начальная концентрация вещества В равна 8 моль/л. А + 2В <==> С.
После окончания реакции концентрация вещества А равна 2 моль/л.
2. Напишите закон действия масс для реакции: CO(г) + Cl2(г) --> COCl2(г). Как изменится скорость реакции, если объем системы уменьшить вдвое.
3. При температуре 60оС скорость реакции составляет 0,64 моль/л. с. Какова скорость реакции при 10оС, если температурный коэффициент скорости реакции равен 2 ?
ВАРИАНТ 3
1. В реакции CO(г) + H2О(г) <==> CO2(г) + H2(г) равновесие установилось при концентрациях [CO] = 0,04 моль/л, [H2О] = 0,16 м/л, [H2] = 0,08 моль/л, [CO2] = 0,08 моль/л. Вычислить Кр и исходные концентрации [CO] и [H2О].
2. Как повлияет на равновесие реакции 2H2(г)+ O2(г) <==>2H2О(г) + 483,6 кДж
а) увеличение температуры, б) повышение давления?
3. Две реакции протекают при 25оС с одинаковой скоростью. Температурный коэффициент скорости первой реакции равен 2,0 ; а второй 2,5. Найти отношение скоростей этих реакций при 95оС.
ВАРИАНТ 4
1. При состоянии равновесия системы N2 + 3H2 <==> 2NH3 концентрации участвующих в реакции веществ равны [N2] = 3 моль/л, [H2] = 9 моль/л, [NH3] = 4 моль/л. Каковы были исходные концентрации азота и водорода?
2. Как сместить равновесие в реакции N2 (г) + 3H2 (г) <==> 2NH3 (г) + 92,4 кДж в прямом направлении.
3. Скорость реакции при 0оС равна 1. Чему равна скорость этой реакции при 200°С, если ![]() = 2 ?
= 2 ?
ВАРИАНТ 5
1. Через некоторое время после начала реакции: 3 А + В <==> 2 C концентрации веществ составляли [А] = 3 моль/л, [В] = 1 моль/л,[С] = 0,8 моль/л. Каковы исходные концентрации веществ А и В?
2. Газовая смесь состоит из водорода и хлора. Реакция идет по уравнению H2 + Cl2 --> 2HCl. Как изменится скорость реакции, если увеличить давление в три раза?
3. Вычислить ![]() реакции, если константа скорости её при 1200С составляет 5,88.10-4 , а при 1700С равна 6,7.10-2.
реакции, если константа скорости её при 1200С составляет 5,88.10-4 , а при 1700С равна 6,7.10-2.
Контрольная работа 4. Расчет водородного показателя водного раствора кислоты, основания или соли.
Вариант 1
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) нитрата цинка.
2. Найти молярную концентрацию раствора гидроксида бария, если рН равен 9.
Вариант 2
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) хлорида магния.
2. Чему равен рН в 0,025 Н растворе серной кислоты.
Вариант 3
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) карбоната лития.
2. Вычислить рН раствора азотной кислоты, в 500 мл которого содержится 3,15 г азотной кислоты.
Вариант 4
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) нитрата свинца (II).
2. рН раствора гидроксида кальция равен 12. Найти концентрацию этого раствора в г/л.
Вариант 5
1. Напишите уравнение гидролиза (в молекулярной и ионной форме) роданида натрия.
2. рН раствора гидроксида калия равен 11. Найти нормальность этого раствора.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |



