Уравнивая число электронов в полуреакциях, находим дополнительный множитель ко второй полуреакции (3). После умножения получим:
ClO3– + 3Н2О + 6![]() → Cl– + 6ОН–
→ Cl– + 6ОН–
3H2O2 - 6![]() → 3O2 + 6Н+
→ 3O2 + 6Н+
![]()
СдЩ3– + 3Н2О + 6![]() + 3Р2Щ2 - 6
+ 3Р2Щ2 - 6![]() → Сд– + 6ОН - + 3Щ2 + 6Н+
→ Сд– + 6ОН - + 3Щ2 + 6Н+
Уничтожаем электроны и из 6Н+ и 6ОН– образуется 6Н2О
ClO3– + 3Н2О + 3H2O2 → Cl– + 3O2 + 6Н2О
ClO3– + 3H2O2 → Cl– + 3O2 + 3Н2О
Переносим коэффициенты в исходное уравнение и получаем:
KClO3 + 3H2O2 = KCl + 3O2 + 3H2O
4.2. Гальванические элементы и электрохимические процессы
4.2.1. Понятие электрода
Электрохимия изучает процессы, связанные с взаимным превращением химической и электрической энергии.
Преобразование энергии реакции в энергию электрическую осуществляется в устройствах, называемых химическими источниками тока или гальваническими элементами. Химические же превращения за счёт внешней электрической энергии происходят в процессах электролиза. В устройствах обоих типов протекают окислительно-восстановительные реакции (называемые электрохимическими), особенностью которых является не хаотичность, а пространственная локализация приёма-отдачи электронов. Она достигается исключением прямого контакта между окислителем и восстановителем.
Электрохимические процессы происходят на устройствах, называемых электродами. Электрод, на котором происходит процесс окисления, называется анодом. Соответственно электрод, на котором происходит процесс восстановления, называется катодом.
По природе участвующих в проводимости частиц электроды делятся на:
Ø электроды первого рода (проводниками электричества являются электроны). Это металлы, графит, уголь.
Ø электроды второго рода (в электропроводимости участвуют ионы). Это металлические или газовые электроды, в схеме которых присутствует раствор электролита.
4.2.2. Типы электродов. Электродный потенциал
Ионно-металлический электрод второго рода – это металл (Ме), погруженный в раствор, содержащий катионы этого металла.
Запись его схемы: Ме0 | Меz+, C(Mez+) или Ме0 | МеХ, С(МеХ),
где Ме0 – металл (твёрдая фаза);
Меz+, МеХ – раствор электролита (жидкая фаза);
C(Mez+), С(МеХ) – молярная концентрация соответственно катионов или соли данного металла в растворе, моль/дм3.
Вертикальная черта обозначает поверхность раздела фаз металл – раствор.
Например: Fe0 | Fe2+, C(Fe2+) или Fe0 | FеSO4, С(FеSO4)
На границе раздела металл-раствор происходит взаимодействие, характер которого обусловлен природой металла. На активных металлах, обладающих, в основном, восстановительными свойствами, металл окисляется, и его катионы переходят в раствор:
Ме0 – ze → Меz+ (окисление металла).
Электроны, заряд которых не скомпенсирован, остаются в металле. Металл при этом заряжается отрицательно, а раствор – положительно благодаря адсорбции катионов к границе раздела.
На неактивных металлах, обладающих преимущественно окислительными свойствами, происходит восстановление катионов металла из раствора:
Меz++ ze → Ме0 (восстановление)
Это приводит к уменьшению количества свободных электронов в металле, и поверхность металла на границе раздела заряжается положительно, а из раствора адсорбируются отрицательно заряженные ионы.
Таким образом, на границе раздела фаз металл–раствор как в случае активного, так и пассивного металлов образуется двойной электрический слой. Возникающую при этом разность потенциалов между металлом и электролитом называют равновесным электродным потенциалом. Потенциалу присваивается тот знак, который возникает на поверхности металла в двойном электрическом слое, величина потенциала соответствует состоянию динамического равновесия: Меz++ ze ![]() Ме. Обозначение потенциала –
Ме. Обозначение потенциала – ![]() . Например,
. Например, ![]() .
.
Величина равновесного потенциала ионно-металлического электрода ЕР(Меz+/Ме) рассчитывается по уравнению, которое при Т = 298 К имеет вид:
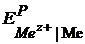 =
= 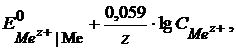
где z – число электронов, принимающих участие в динамическом равновесии, определяемое зарядом катиона;
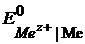 - стандартное значение потенциала, равное потенциалу электрода в растворе с
- стандартное значение потенциала, равное потенциалу электрода в растворе с 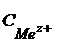 = 1 моль/дм3, Т = 298 К (значения приводятся в приложении 6).
= 1 моль/дм3, Т = 298 К (значения приводятся в приложении 6).
Значения стандартных электродных потенциалов составляют ряд напряжений и характеризуют окислительно-восстановительные свойства металлов. Чем меньше алгебраическая величина 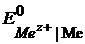 , тем более химически активен металл, он легче окисляется (отдаёт электроны) и труднее восстанавливается (принимает электроны) и наоборот:
, тем более химически активен металл, он легче окисляется (отдаёт электроны) и труднее восстанавливается (принимает электроны) и наоборот:
Е1(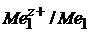 ) < Е1(
) < Е1(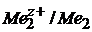 ) < … Еn(
) < … Еn(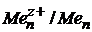 ).
).
← усиление восстановительных свойств
усиление окислительных свойств →
Каждый предыдущий в ряду напряжений металл вытесняет последующий из раствора его соли.
Газовые электроды состоят из инертного электрода (благородный металл (платина, родий и т. п.), графит, уголь), помещённого в раствор электролита, через который на поверхность электрода подаётся газ (O2, H2, Cl2 и т. п.). Инертный электрод сорбирует молекулы газа и служит проводником электронов от молекул газа к ионам в растворе и наоборот.
Ниже приведены схемы процессов, происходящих на водородном и кислородном электродах в растворах разной природы.
Таблица 4.3. Водородный и кислородный газовые электроды
Природа среды | Обозначение | Электродная реакция | Стандартный потенциал, В |
ВОДОРОДНЫЙ ЭЛЕКТРОД | |||
Кислая рН < 7 | Pt, H2|H+ | 2Н++ 2e | 0 |
Нейтральная, щелочная рН ≥ 7 | Pt, H2|H2O | 2Н2О+ 2e | (-0,059 pH) |
КИСЛОРОДНЫЙ ЭЛЕКТРОД | |||
Кислая рН < 7 | Pt, О2|H+ | О2 + 4Н++ 4e | (1,213 – 0,059 pH) |
Нейтральная, щелочная рН ≥ 7 | Pt, О2|H2O | О2 + 2Н2О+ 4e |
4.2.3. Гальванические элементы
Гальванические элементы (ГЭ) – химические источники электричества. При работе ГЭ в нём самопроизвольно идёт реакция окисления-восстановления. Химическая энергия этой реакции переходит в электрическую. Процессы окисления и восстановления в ГЭ пространственно разделены: окисление происходит на аноде, восстановление – на катоде. Потенциал анода всегда меньше потенциала катода. ГЭ получают, объединяя в одну систему два электрода с разными значениями равновесного электродного потенциала.
Схема ГЭ, собранного из двух металлических электродов, показана ниже:
(–А) Ме1 | ![]() (С1) ||
(С1) || ![]() (С2) | Ме2 (+К),
(С2) | Ме2 (+К),
где две вертикальные черты означают границу раздела между электродами. В схеме ГЭ анод принято записывать слева, катод – справа. Процессы, протекающие в ГЭ:
На аноде (А): Ме1 – ze → (окисление Ме1).
На катоде (К): ![]() + ze → Ме2 (восстановление ).
+ ze → Ме2 (восстановление ).
Токообразующая реакция: Ме1 + ![]() →
→ ![]() + Ме2.
+ Ме2.
Электродвижущая сила (ЭДС) ГЭ равна разности равновесных потенциалов катода и анода:
ЭДС = ![]() –
– ![]() .
.
Если металлы анода и катода по своей природе одинаковы, то такой элемент называется концентрационным ГЭ. В этом случае ЭДС возникает только за счёт разных концентраций растворов соли металлов. Схема концентрационного ГЭ:
Ме | Меz+ (С1) || Меz+ (С2) | Ме.
Если С1(Меz+) < С2 (Меz+), то левый электрод на схеме будет анодом, а правый электрод – катодом. Электродные процессы:
(А): Ме – ze → Меz+.
(К): Меz+ + ze → Ме.
Электродвижущая сила концентрационного ГЭ при Т = 298 К:
ЭДС = ![]() –
– ![]() =
= 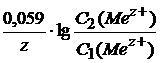 .
.
4.2.4. Электролиз расплавов и водных растворов электролитов
Электролизом называются окислительно-восстановительные процессы, протекающие на электродах под действием электрического тока, подаваемого от внешнего источника.
При электролизе – катод («-» источника) – восстановитель, т. к. он отдаёт электроны катионам, а анод («+» источника) – окислитель, т. к. он принимает электроны у атомов. Катоды, используемые в электролизе, всегда инертные, а аноды могут быть как инертными, так и растворимыми (из любого металла, стоящего в ряду напряжений после алюминия: Cu, Sn, …).
Под действием электрического поля начинается направленное движение ионов к электродам и на них протекают соответствующие реакции.
Электродные реакции окисления и восстановления, происходящие в двойном электрическом слое, называются первичными. Вторичные реакции обусловлены взаимодействием продуктов первичных реакций друг с другом, с материалом электродов и со средой.
Природа и течение электродных процессов определяются составом электролита, растворителем, материалом электродов и режимом электролиза (напряжение, плотность тока, температура). Необходимо различать электролиз растворов и электролиз расплавов электролитов.
Электролиз водных растворов
При электролизе водных растворов на электродах кроме ионов электролита могут окисляться и восстанавливаться и молекулы Н2О. Восстановление на катоде происходит в соответствии со следующим правилом: чем меньше алгебраическая величина стандартного электродного потенциала, тем характернее для частицы ионное состояние и тем труднее восстановить его ионы на катоде. По способу восстанавливаться на катоде из водного раствора электролита все катионы металлов можно разделить на три группы в зависимости от положения в ряду напряжений металлов:
1. Катионы металлов сильных восстановителей (от Li+ до Al3+ включительно, Е0(Меz+/Ме) ≤ –1,66В) на катоде не восстанавливаются, на нем выделяется водород по одной из реакций:
а) рН < 7 К: 2Н+ + 2е → Н2;
б) рН ≥ 7 К: 2Н2О + 2е → Н2 + 2ОН─.
При этом раствор у катода подщелачивается, т. е. рН увеличивается по сравнению с исходным значением.
2. Катионы металлов, стандартный электродный потенциал которых меньше стандартного потенциала водородного электрода и больше потенциала алюминия (Е0(Al) < Е0(Me) < Е0(H2)), восстанавливаются на катоде одновременно с молекулами Н2О или ионами Н+:
а) рН < 7 К: Меz+ + ze → Me0,
2Н+ + 2е → Н2;
б) рН ≥ 7 К: Меz+ + ze → Me0,
2Н2О + 2е → Н2 + 2ОН─.
3. Катионы металлов, стандартный электродный потенциал которых больше потенциала стандартного водородного электрода (от Cu2+ до Au3+), при электролизе практически полностью восстанавливаются на Катоде.
К: Меz+ + ze → Me.
Характер реакций, протекающих на аноде, зависит от присутствия молекул H2O, так и от вещества анода и определяется следующим правилом: на аноде легче окисляются электрохимически активные частицы с алгебраическим значением стандартного электродного потенциала.
![]() В случае инертного анода материал анода не окисляется, а является лишь приемником электронов от молекул или анионов. При этом анодный процесс зависит лишь от природы электролита:
В случае инертного анода материал анода не окисляется, а является лишь приемником электронов от молекул или анионов. При этом анодный процесс зависит лишь от природы электролита:
а) при электролизе растворов, содержащих бескислородные анионы (Cl─, Br─, I─, CN─, кроме F─), на аноде легко окисляются эти анионы в порядке уменьшения значения электродного потенциала:
А: 2Br─ – 2e → ![]() ;
;
б) при электролизе растворов с кислородсодержащими анионами (![]() и т. д.) на аноде в зависимости от рН раствора окисляется вода или анионы ОН─:
и т. д.) на аноде в зависимости от рН раствора окисляется вода или анионы ОН─:
Анодный процесс:
а) рН ≤ 7 А(С): Н2О – 4е → О2 + 4Н+;
б) рН > 7 А(С): 4ОН─ – 4е → О2 + 2Н2О.
При этом раствор у анода подкисляется, т. е. рН уменьшается.
![]() В случае растворимого анода независисмо от вида электролита (раствор и расплав), или от природы аниона окисляется материал анода:
В случае растворимого анода независисмо от вида электролита (раствор и расплав), или от природы аниона окисляется материал анода:
А (Ме): Ме ─ ze → Mez+
Электролиз расплавов электролитов
При электролизе расплавов
![]() на катоде восстанавливаются катионы электролита в порядке увеличения стандартного электродного потенциала;
на катоде восстанавливаются катионы электролита в порядке увеличения стандартного электродного потенциала;
![]() на инертном аноде окисляются анионы электролита в порядке уменьшения стандартного электродного потенциала. На растворимом аноде окисляется материал анода.
на инертном аноде окисляются анионы электролита в порядке уменьшения стандартного электродного потенциала. На растворимом аноде окисляется материал анода.
4.2.5. Законы Фарадея
Процессы превращения веществ на электродах описываются законами Фарадея:
1. Массы или объемы веществ, испытавшие электрохимические превращения на электродах, прямо пропорциональны количеству прошедшего электричества:
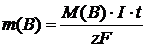 .
.
Для газообразных веществ:
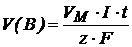 ,
,
где m(B) – масса вещества, претерпевшего электрохимическое превращение на электроде, г;
V(B) – объем газообразного вещества при н. у., претерпевшего электрохимическое превращение на электроде, дм3;
M(B) – молярная масса вещества, г/моль;
![]() – молярный объем газообразного вещества при н. у., равный 22,4 дм3/моль;
– молярный объем газообразного вещества при н. у., равный 22,4 дм3/моль;
z – число электронов в электродном процессе, определяемое соответствующим электродным процессам;
I ∙ t =Q – количество электричества, пропущенное через электролизер, А∙с;
I – сила тока, А;
t – продолжительность электролиза, с.
2. Массы или объемы прореагировавших на электродах веществ при постоянном количестве электричества относятся между собой, как молярные массы эквивалентов или молярные объемы эквивалентов этих веществ.
Учитывая, что М(В)/ z(В) = 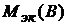 ,
, ![]() / z(В) = , получаем при Q = const
/ z(В) = , получаем при Q = const
.
4.2.6. Примеры решения задач
Задача № 1
ГЭ состоит из серебряного электрода, погружённого в раствор AgNO3, в 100 см3 которого содержится 0,17 г соли, и водородного электрода в растворе HCl с рН = 4. Составьте схему ГЭ, напишите электродные реакции и рассчитайте ЭДС.
Решение:
Определим молярную концентрацию AgNO3 в растворе:
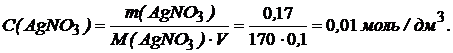
AgNO3 – сильный электролит со степенью диссоциации α(AgNO3) = 1, поэтому концентрация ионов Ag+ определяется как
С(Ag+) = С(AgNO3) ∙ α(AgNO3) = 0,01 ∙ 1 = 0,01 моль/дм3.
Тогда потенциал серебряного электрода
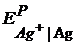 =
= 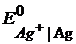 + 0,0591 lg C(Ag+) = 0,799 + 0,0591 lg 0,01 = 0,681 B.
+ 0,0591 lg C(Ag+) = 0,799 + 0,0591 lg 0,01 = 0,681 B.
Рассчитаем потенциал водородного электрода
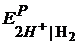 = –0,059рН = –0,059 ∙4 = –0,236 В.
= –0,059рН = –0,059 ∙4 = –0,236 В.
Сравнение электродных потенциалов показывает, что анодом будет водородный электрод. Схема ГЭ:
Pt, H2 | HCl || AgNO3 | Ag.
(А): Н2 – 2e → 2Н+
(К): Ag+ + e → Ag
Токообразующая реакция: Н2 + 2Ag+ = 2Ag + 2Н+.
ЭДС = ![]() –
– ![]() = 0,681 – (–0,236) = 0,971 В.
= 0,681 – (–0,236) = 0,971 В.
Ответ: Электродвижущая сила ГЭ составляет 0,971 В.
Задача № 2
Напишите уравнения электродных процессов при электролизе водного раствора NiSO4 с графитовым анодом.
Решение:
Графитовый анод (С) – нерастворимый.
Диссоциация в растворе NiSO4 ![]() , так как -1,66 В < Е0(Ni2+/ Ni) < 0 В, следовательно, на катоде протекают процессы восстановления Ni2+ и водорода. Учитывая гидролиз NiSO4 соли сильной кислоты и слабого основания будут следующими:
, так как -1,66 В < Е0(Ni2+/ Ni) < 0 В, следовательно, на катоде протекают процессы восстановления Ni2+ и водорода. Учитывая гидролиз NiSO4 соли сильной кислоты и слабого основания будут следующими:
Ni2+ + H2O → NiOH+ + H+, pH < 7,
Электродные процессы
K (–):
2H+ + 2e → H2↑
A (+): H2O – 4e → O2↑ + 4H+
Задача № 3
Напишите электродные процессы при электролизе расплава
MgCl2 ∙ 6CaCl.
Решение:
В расплаве происходит диссоциация:
MgCl2 ∙ 6CaCl Mg2+ + 6Ca2+ + 8Cl─
Е0(Меz+/Ме): –2,363B > –2,925B
Так как Е0(Мg) > Е0(Ca), то на катоде восстанавливается катион Mg2+, а потом ─ Ca2+.
Катодный процесс: Mg2+ + 2е → Mg
Ca2+ + 2e → Ca.
На аноде окисляются анионы Cl─.
Анодный процесс: 2Cl─ ─ 2e → Cl2.
Задача № 4
При электролизе раствора CuSO4 на графитовых электродах масса катода увеличилась на 10,58 г. Определите объем газа, выделившегося на аноде (н. у).
Решение:
Чтобы определить, какие вещества выделились на электродах, напишем уравнение диссоциации CuSO4 и электродные процессы:
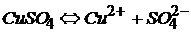 , рН < 7 из-за гидролиза
, рН < 7 из-за гидролиза
К (–): Cu2+ + 2е → Cu z(Cu) = 2
А (+): 2Н2О – 4е → О2 + 4Н+ z(О2) = 4
Следовательно, на катоде выделяется медь, на аноде – газ кислород. = 63,5/2 = 31,75 г/моль·экв.
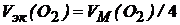 = 22,4/4 = 5,6 дм3/моль.
= 22,4/4 = 5,6 дм3/моль.
Поскольку при электролизе через катод и анод проходит одно и то же количество электричества: Q = Qа = Qк, то
.
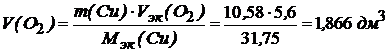 .
.
Ответ: объём образовавшегося на аноде кислорода составляет 1,866.
Приложение 1. Названия некоторых кислот и соответствующих им солей
Формула | Название кислоты (сильная –1, слабая –0) | Пример средней соли | Название солей |
HF | Фтороводородная –0 (плавиковая) | NH4F | Фториды |
HCl | Хлороводородная –1 (соляная) | NaCl | Хлориды |
HClO | Хлорноватистая –0 | NaClO | Гипохлориты |
HClO2 | Хлористая–0 | LiClO2 | Хлориты |
HClO3 | Хлорноватая –1 | KClO3 | Хлораты |
HClO4 | Хлорная –1 | NaClO4 | Перхлораты |
HBr | Бромоводородная –1 | KBr | Бромиды |
HI | Иодоводородная –1 | MgI2 | Иодиды |
HIO3 | Иодноватая –1 | KIO3 | Иодаты |
H2S | Сероводородная –0 | (NH4)2S | Сульфиды |
H2SO3 | Сернистая-0 | Na2SO3 | Сульфиты |
H2SO4 | Серная-1 | Na2SO4 | Сульфаты |
H2S2O3 | Тиосерная-0 | Na2S2O3 | Тиосульфаты |
HNO3 | Азотная-1 | KNO3 | Нитраты |
HNO2 | Азотистая-0 | NH4NO2 | Нитриты |
H3PO4 | Фосфорная-0 | Ag3PO4 | Фосфаты |
H3AsO4 | Мышьяковая-0 | Na3AsO4 | Арсенаты |
H3AsO3 | Мышьяковистая-0 | Na3AsO3 | Арсениты |
H2CrO4 | Хромовая-1 | K2CrO4 | Хроматы |
H2Cr2O7 | Двухромовая-1 | K2Cr2O7 | Дихроматы |
HMnO4 | Марганцовая-1 | KMnO4 | Перманганаты |
H2SiO3 | Кремниевая-0 | Na2SiO3 | Силикаты |
H2CO3 | Угольная-0 | CaCO3 | Карбонаты |
HCN | Циановодородная-0 (синильная) | KCN | Цианиды |
HSCN | Тиоциановая-0 (родановая) | NH4SCN | Тиоцианаты (роданиды) |
CH3COOH | Уксусная-0 | NaCH3COO | Ацетаты |
H3BO3 | Борная-0 | K3BO3 | Бораты |
H2B4O7 | Четырехборная-1 | Na2B4O7 | Тетрабораты |
HВrO3 | Бромноватая-1 | LiBrO3 | Броматы |
HCOOH | Муравьиная-0 | NaHCOO | Формиаты |
H2C2O4 | Щавелевая-0 | CaC2O4 | Оксалаты |
HCrO2 | Хромистая-0 | KСrO2 | Хромиты |
H5IO6 | Ортоиодная-0 | (NH4)5IO6 | Ортопериодаты |
HIO4 | Метаиодная-1 | NaIO4 | Метапериодаты |
H2MnO4 | Марганцовистая-1 | Na2MnO4 | Манганаты |
HOCN | Циановая-0 | Mg(OCN)2 | Цианаты |
HPO3 | Метафосфорная-1 | Ca(PO3)2 | Метафосфаты |
H4P2O7 | Двуфосфорная-1 | Na4P2O7 | Дифосфаты |
H3PO3 | Фосфористая-0 | AlPO3 | Фосфиты |
H3PO2 | Фосфорноватистая-0 | Na3PO2 | Гипофосфиты |
H2S2O8 | Пероксодвусерная-1 | BaS2O8 | Пероксодисульфаты |
H2S2O7 | Двусерная-1 | K2S2O7 | Дисульфаты (пиросульфаты) |
H2S2O5 | Двусернистая-1 | CaS2O5 | Дисульфиты |
H2S2O2 | Тиосернистая-0 | Na2S2O2 | Тиосульфиты |
H2S2O6 | Дитионовая-1 | K2S2O6 | Дитионаты |
H6TeO6 | Теллуровая-0 | Na6TeO6 | Теллураты |
HVO3 | Ванадиевая-1 | LiVO3 | Ванадаты |
H2WO4 | Вольфрамовая-1 | CaWO4 | Вольфраматы |
Приложение 2. Термодинамические характеристики некоторых веществ

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |



