На правах рукописи
АВГУСТИНОВИЧ
АЛЕКСАНДРА ВЛАДИМИРОВНА
ОСОБЕННОСТИ ЛИМФОГЕННОГО МЕТАСТАЗИРОВАНИЯ И ВЫБОР ОПТИМАЛЬНОГО ОБЪЕМА ЛИМФОДИССЕКЦИИ ПРИ РАКЕ ЖЕЛУДКА
14.00.14 – онкология,
14.00.19 – лучевая диагностика, лучевая терапия
А В Т О Р Е Ф Е Р А Т
диссертации на соискание ученой степени
кандидата медицинских наук
Томск – 2009
Работа выполнена в Научно-исследовательском институте онкологии Сибирского отделения Российской академии медицинских наук, г. Томск.
 Научные руководители:
Научные руководители:
доктор медицинских наук
доктор медицинских наук,
профессор
Официальные оппоненты:
доктор медицинских наук,
профессор
доктор медицинских наук,
профессор
Ведущая организация – Медицинский радиологический научный центр РАМН, г. Обнинск
Защита состоится “____” ____________________ 2009 г. в ____ часов на заседании диссертационного совета Д 001.032.01 при Научно-исследовательском институте онкологии СО РАМН ( г. Томск, пер. Кооперативный, 5).
С диссертацией можно ознакомиться в библиотеке НИИ онкологии ТНЦ СО РАМН.
Автореферат разослан “____” _____________________ 2009 г.
Ученый секретарь диссертационного совета,
доктор медицинских наук, профессор
Общая характеристика диссертации
Актуальность проблемы:
Рак желудка в настоящее время занимает 2-ое место в структуре общей онкологической заболеваемости. с соавт., 2001; с соавт., 2002; , 2004; , , 2004; Muller M. K., 2000; Kim G. P., Takimoto C. H., 2001; Karpen M. S. et al., 2002). Ежегодно в мире регистрируется 755 тыс. новых случаев и 628 тыс. смертей от этого заболевания. В структуре онкологической заболеваемости данная патология составляет 12,3%.
К числу стран с особенно высокой заболеваемостью злокачественными новообразованиями верхних отделов пищеварительного тракта – так называемому «поясу рака пищевода и желудка», относятся государства Юго-Восточной Азии, в первую очередь, Япония, Китай, особенно его северные районы, Российская Федерация и большинство других республик бывшего Советского Союза.
В настоящее время ранняя диагностика рака желудка является глобальной проблемой. Во всем мире, кроме Японии, не существует реально работающих программ скрининга по раку желудка (, 2003; Maruyama M. et al., 2006; Moreto M., 2001). В нашей стране до 80% больных обращаются за медицинской помощью при III-IV стадии опухолевого процесса, что, естественно, не может положительно сказаться на эффективности лечения. Основным фактором, определяющим прогноз при раке желудка, является лимфогенное распространение опухолевого процесса.
Несмотря на очевидные достижения современной клинической онкологии в ряде областей, состояние раздела «Рак желудка, отдаленные результаты лечения» нельзя признать удовлетворительным ( с соавт., 2007; с соавт., 2003; с соавт., 2008; Sano T., Sasako M., 2006).
Стойкое излечение возможно только на начальных стадиях процесса, когда практически отсутствуют клинические проявления заболевания, а инструментальная диагностика крайне затруднена. При раннем раке желудка в практику начинают внедряться малоинвазивные эндоскопические операции, но до сих пор они доступны небольшому кругу высокоспециализированных лечебных учреждений, показания к ним уточняются ( с соавт., 2003; с соавт., 2004; Miyata M. et al., 2000; Rembacken D. J. et al., 2001).
По-прежнему, ключевым методом лечения рака желудка, остается хирургическое вмешательство. Основные принципы радикальных операций по поводу РЖ были разработаны одними из первых в практической онкологии и в настоящее время не подлежат сомнению. Предпринимаются попытки решить проблему улучшения результатов лечения местнораспространенного рака желудка за счет расширения объема хирургического вмешательства путем перигастральной лимфодиссекции в объеме D2 и более. (, 2004; Maruyama K et al, 1999; Ogata Y. et al., 2000). Однако, на сегодняшнем этапе, в мировой литературе имеются диаметрально противоположные мнения об отдаленной эффективности расширенных и комбинированных операций. В ряде рандомизированных исследований, проведенных в основном западноевропейскими хирургами (Robertson C. S. et al., 1994; Bobenkamp J. J. et al., 1993; van de Velde C. J.H. et al., 1999), не подтверждаются преимущества радикальных операций с широкой лимфодиссекцией перед стандартными вмешательствами, на чем настаивают японские и российские авторы ( с соавт., 2003, 2004; с соавт., 2004; Sawai K. et al., 1994; Inada T. et al., 1999; Natsugoe S. et al., 1999). Применительно ко многим злокачественным новообразованиям внутренних локализаций, и для рака желудка, в частности, стратификация по стадиям на этапе предоперационной диагностики не является окончательной. Единственным надежным методом, определяющим состояние регионарных лимфатических узлов, и соответственно стадирование опухолевого процесса, является морфологическое исследование удаленного препарата. В последние годы широко обсуждается концепция «выбора объёма хирургического лечения в зависимости от стадии». Исследование так называемых «сторожевых» лимфатических узлов, по мнению ряда авторов, может сократить объём вмешательства и минимизировать тем самым его травматичность и риск у 1/3 больных, у которых по статистике отсутствуют лимфогенные метастазы. До недавнего времени концепция «сторожевых» лимфатических узлов при раке желудка подвергалась серьезной критике, что связано со сложностью путей лимфоттока от этого органа и наличием большого количество лимфатических коллатералей. Однако сейчас негативная точка зрения пересматривается, но остается достаточно большое количество нерешенных вопросов.
Таким образом, на современном этапе назрела объективная необходимость определить показания для выбора оптимального объёма лимфодиссекции. Настоящая работа посвящена решению этой проблемы.
Цель исследования:
Разработка методического подхода в определении объема лимфодиссекции у больных раком желудка.
Задачи исследования:
1. Изучить влияние объема перигастральной лимфодиссекции на показатели отдаленной выживаемости и риска развития локорегионарных рецидивов у больных раком желудка.
2. Исследовать закономерности и основные факторы риска, а также частоту лимфогенного метастазирования рака желудка.
3. Разработать методику радионуклидного выявления «сторожевых» лимфатических узлов у больных раком желудка и оценить её диагностическую эффективность.
4. Определить оптимальный объём лимфодиссекции у больных раком желудка на основании закономерностей лимфогенного метастазирования и радионуклидной визуализации «сторожевых» лимфатических узлов.
Научная новизна:
Впервые разработана и внедрена в клиническую практику интраоперационная радионуклидная методика определения «сторожевых» лимфатических узлов при раке желудка, а также изучена её диагностическая эффективность в зависимости от способа введения лимфотропного радиофармпрепарата (патент на изобретение № 000).
Уточнены и систематизированы особенности лимфогенного метастазирования рака желудка при различных клинико-морфологических характеристиках опухолей.
На основании анализа закономерностей лимфогенного метастазирования рака желудка предложена математическая модель для индивидуального прогнозирования риска возникновения метастазов в лимфатические узлы
Практическая значимость
Определены значимые факторы риска лимфогенного метастазирования, на основании которых разработан алгоритм для выбора объёма лимфодиссекции у больных раком желудка.
Разработан и внедрён в клиническую практику метод интраоперационной визуализации «сторожевых» лимфатических узлов
Положения, выносимые на защиту
Выполнение лимфодиссекции в объеме D2 при наличии факторов риска лимфогенного метастазирования позволяет улучшить отдаленные результаты лечения.
Методика определения «сторожевых» лимфатических узлов при интраоперационном введении РФП является высокоэффективным диагностическим тестом.
Результаты исследования «сторожевых» лимфатических узлов позволяют выбрать оптимальный объём лимфодиссекции при «малом» раке желудка.
Внедрение
Результаты исследования внедрены и успешно применяются в практической деятельности торако-абдоминального отделения и лаборатории радионуклидных методов исследования НИИ онкологии Сибирского отделения РАМН.
Апробация работы
Основные положения диссертации докладывались и обсуждались на заседаниях Координационной комиссии и Ученого совета НИИ онкологии СО РАМН (2008 г. г.), Томского областного общества онкологов, рентгенологов (2007-08 г. г.), на Региональной конференции молодых ученых им. академика РАМН «Актуальные вопросы экспериментальной и клинической онкологии» (Томск, 2007-09 г. г.), на V съезде онкологов и радиологов СНГ (г. Ташкент, Узбекистан, май 2008 г.), на The Sixth International Congress of the Choatian Society of Nuclear Medicine (Opatija, Хорватия, май, 2008 г.), на I Международной конференции по торако-абдоминальной хирургии, «К 100-летию со дня рождения академика » (г. Москва, июнь 2008 г.), на межрегиональной научно-практической конференции «Актуальные вопросы онкогастроэнтерологии» (г. Барнаул, июнь 2008 г.), на Xth World Congress on Gastrointestinal Cancer, www. postersessiononline. eu (г. Барселона, Испания, июнь 2008 г.), на Российской научно-практической конференции с международным участием «Проблемы современной онкологии» (г. Барнаул, июнь 2009 г.).
Структура и объем работы:
Диссертация состоит из введения, 3 глав, заключения, выводов, практических рекомендаций, указателя литературы. Текст изложен на 134 странице, иллюстрирован 23 таблицами и 28 рисунками. Библиография включает 218 источников, из них 105 отечественных и 113 иностранных.
Публикации
По теме диссертации опубликовано 22 печатных работ, отражающих основные положения диссертации, в том числе статей в рецензируемых изданиях, рекомендованных списком ВАК – 1. Получен патент РФ за № 000 на изобретение «Способ диагностики «сторожевых» лимфатических узлов при раке желудка».
Содержание работы
Материалы и методы: Работа основана на проспективном анализе историй болезни 138 больных, оперированных по поводу рака желудка в НИИ онкологии СО РАМН, в период с 2006 по 2008 гг. Все пациенты находились на стационарном лечении в отделении торакоабдоминальной онкологии. В исследование включались больные с морфологически подтвержденным диагнозом рак желудка, ранее не подвергавшиеся какому-либо лечению.
Основную группу составили 72 пациента, получившие оперативное вмешательство с перигастральной лимфодиссекцией D2. Из них 46 больным проведено исследование «сторожевых» лимфатических узлов. В группу контроля вошли 66 пациентов, которым было выполнено радикальное оперативное вмешательство с лимфодиссекцией D1.
По основным прогностическим критериям сравниваемые группы были однородны. Среди 138 больных было%) мужчин и,7%) женщины в возрасте от 30 до 75 лет. Средний возраст пациентов составил 53,4 ± 11,3 лет.
Наиболее часто опухолью поражался пилороантральный отдел 63 пациента (43,5%), поражение тела желудка выявлено у,6%) пациентов, рак проксимального отдела желудка диагностирован у,8%) больных, у 7 (10,1%) пациентов опухоль тотально поражала желудок.
Морфологическая характеристика опухоли включала следующие параметры: глубина инвазии, размер, степень дифференцировки, тип роста по Borrmann. Практически у всех больных диагностирована аденокарцинома различной степени дифференцировки – ,1%) случаев.
У большинства пациентов размер опухоли превышал 5 см в диаметре –,6%) наблюдений. По глубине инвазии у,6 %) пациентов опухоль прорастала серозную оболочку, выходила за пределы желудочной стенки у,5%) больных, у,4%) – была ограничена слизистой оболочкой желудка и у,3%) – прорастала мышечный слой.
Наиболее часто в исследовании встретились II и III тип опухолевого роста по Borrmann –,6%) и%) случаев соответственно.
В сравниваемых группах больным проведено радикальное хирургическое лечение. Субтотальная дистальная резекция желудка выполнена 72 пациентам (52,2%), гастрэктомия –,7%), комбинированная гастрэктомия,6%), операция Гэрлока – 3 (2,2%), операция Льюиса – 4 (2,8%), субтотальная проксимальная резекция – 2 (1,4%).
Исследование «сторожевых» лимфатических узлов выполнено 46 больным раком желудка (63,9%) основной группы, находившимся на стационарном лечении в клиниках института с 2007 года. В связи с задачами исследования по способу введения радиофармпрепарата (РФП) пациенты были разделены на две группы:,8%) больных РФП вводился за сутки до операции, путем 4-х эндоскопических субмукозных инъекций по периметру опухоли,,2%) пациентам РФП был введён во время операции, субсерозно паратуморально.
Статистическая обработка данных произведена с использованием разработанной базы данных в программе Microsoft Access 2000 и программы Statistica 6. Достоверность различий определялась по критерию χ², точному критерию Фишера и t-критерию Стьюдента. Критерий «выживаемость» оценивался по методу моментов Kaplan-Meier.
Результаты исследования и их обсуждение
Непосредственные результаты перигастральной лимфодиссекции у больных раком желудка.
Сравнительный анализ течения послеоперационного периода показал, что при радикальной операции с лимфодиссекцией D2 послеоперационные осложнения возникли у 8 пациентов, что составило 10,5 ± 3,1%. При оперативном лечении с лимфодиссекцией D1 – у 14 больных (21,2 ± 3,2%). Различия статистически не значимы (p>0,05).
При изучении структуры и характера осложнений отмечено, что статистически значимых различий между группами также нет, несмотря на то, что в I (основной) группе отмечено некоторое увеличение частоты острых послеоперационных панкреатитов, по сравнению с группой контроля – 6 (8,3%) и 3 (4,5%) случаев соответственно. Возможно, это связано с большим числом расширенно-комбинированных операций, проведённых в основной группе. Благодаря отработке методики выполнения расширенно-комбинированных операций и адекватного ведения периоперационного периода в последние годы, нам удалось улучшить непосредственные результаты хирургического лечения. Тем не менее, частота этого осложнения в обеих группах не превышает среднестатистический уровень, который по данным литературы может составлять до 7-24% ( и др., 2004; и др., 2006; и др., 2006).
Общая послеоперационная летальность составила 8,6 ± 4,1%, умерло 12 больных, из них – 4 (6,9 ± 1,7%) больных в основной группе и 6 (9,1 ± 1,7%) в контрольной группе соответственно. Различия между группами статистически недостоверны (p>0,05).
Оценка отдаленных результатов хирургического лечения рака желудка с расширенной перигастральной лимфодиссекцией D2 наглядно продемонстрировали её преимущества. Отмечено статистически значимое уменьшение количества местных рецидивов и отдаленных метастазов, что улучшило показатели отдаленной выживаемости. Соответственно, скорректированная пятилетняя выживаемость больных, получивших оперативное лечение с лимфодиссекцией D2, составила 65,1 ± 5,4% , что достоверно выше, чем при хирургическом лечении c лимфодиссекцией D1 – 21,7 ± 4,8% (p<0,05).
Особенности лимфогенного метастазирования рака желудка
В основной группе были изучены частота и закономерность лимфогенного метастазирования в зависимости от основных характеристик опухолевого роста: глубины инвазии, локализации и размеров опухоли, макроскопических типов по Borrmann, гистологического варианта злокачественных новообразований и степени их дифференцировки.
После морфологического анализа установлено, что в,4%) случаях не было выявлено метастатического поражения лимфатических узлов, до 6 поражённых метастазами лимфоузлов (N1) обнаружено – в,2%), от 6 до 15 (N2) лимфоузлов – у 5 пациентов (6,9%). В,5%) наблюдениях имелось обширное метастатическое поражение лимфатического аппарата – свыше 15 (N3) лимфоузлов. Общая частота лимфогенного метастазирования составила 55,6% (40 из 72 пациентов).
В зависимости от глубины инвазии опухоли стенки желудка были выявлены следующие особенности: при опухолевой инвазии стенки желудка в пределах слизистого и подслизистого слоёв (рТ1-2) лимфогенные метастазы отсутствовали в 23 наблюдениях (31,9%). При увеличении глубины проникновения опухоли в стенку органа отмечается нарастание частоты поражение лимфатических коллекторов, в т. ч. и отдаленных. Так при опухоли соответствующей Т3-Т4 статистически значимо возрастает частота поражения забрюшинных лимфоузлов, что наблюдалось в 7 (9,7 ± 4,4%) случаях, при N3 во всех случаях опухоль прорастала соседние органы (Т4). При оценке отдалённых результатов лечения установлено, что пятилетняя выживаемость у больных распространенностью опухолевого процесса – Т1, Т2, Т3 и Т4 соответственно составила 90 ± 4,3%; 61 ± 4,8%, 35 ± 3,2%; 21 ± 4,1%. Таким образом, показатель глубины опухолевой инвазии является крайне значимым фактором, определяющим прогноз течения и исход заболевания.
Нами не было выявлено чёткой зависимости частоты лимфогенного метастазирования от макроскопического типа роста опухоли. Возможно, это связано с тем, что наиболее часто в исследовании встретились II и III тип опухолевого роста по Borrmann и практически не встречались I и IV макроскопические варианты. При II типе общая частота лимфогенного метастазирования составила 53,6 ± 4,9% (22 из 41 пациентов), при III – 57,1 ± 4,9% (16 из 28).
При анализе частоты лимфогенного метастазирования в зависимость от локализации опухоли в желудке установлено, что при злокачественном поражении тела желудка регионарные лимфогенные метастазы наблюдались в 35,7 ± 4,7% случаев (10 из 28), при раке нижней трети желудка этот показатель равнялся 60,0 ± 4,8% (15 из 25), при опухолях верхней трети – 75 ± 4,3% (9 из 12), при тотальном поражении органа – 85,7 ± 3,3% (6 из 7) (p>0,05). Метастазирование в лимфоузлы уровня N2, N3 наблюдалось при раке верхней трети желудка и его тотальном поражении. Причем проксимальная локализация оказалась в числе факторов риска (p<0,05) экстраперигастрального метастазирования. По результатам проведённого исследования одним из неблагоприятных фактором прогноза явился переход опухоли на пищевод. При наличии опухоли в проксимальном отделе желудка без распространения на пищевод частота лимфогенного метастазирования составила 41,4 ± 4,9%, тогда как при поражении розетки кардии этот показатель возрастает до 56,7 ± 4,9%, а при переходе опухолевой инфильтрации на пищевод лимфогенные метастазы наблюдались в 68,0 ± 4,6% случаев.
Число больных с выявленными лимфогенными метастазами находится в прямой пропорциональной зависимости от размеров опухоли. Показано, что размеры опухоли в 3 см можно считать критическим в плане потенциального риска злокачественного поражения регионарных лимфатических коллекторов. Действительно, при линейных размерах опухоли, не превышающих 3,0 см, наблюдался только один случай метастазирования в перигастральные лимфоузлы (N1), что составило 6,3%. Тогда как, при опухолях превышающих этот размер, статистически значимо возрастает риск лимфогенного метастазирования, что отмечено в 62,1% случаев. Кроме того, поражение лимфоузлов уровня N2 наблюдалось при опухолях размером, как минимум равных 5 см и более.
При сравнительном анализе степени дифференцировки и частоты лимфогенного метастазирования отмечено, что нарастания уровня злокачественности опухоли является неблагоприятным фактором прогноза. Так, при высокодифференцированной аденокарциноме случаев поражения регионарного лимфатического аппарата не наблюдалось, тогда, как частота метастатического поражения лимфоузлов при раке умеренной степени дифференцировки составила 20,0% (8 из 19), при низкой степени дифференцировки – 67,5% (27 из 40). Достоверные различия в частоте лимфогенного метастазирования отмечены только между подгруппами пациентов с опухолями высокой и низкой степени дифференцировки (p<0,01).
Анализ влияния на отдаленные результаты лечения степени дифференцировки опухоли, макроскопических типов, размера опухоли не выявил статистических различий, что не позволяет рассматривать эти факторы как значимые при раке желудка. Наиболее весомое влияние оказала лимфогенная распространенность процесса. На основании классификации МПС (2002) были рассчитаны показатели пятилетней выживаемости по подгруппам. При отсутствии лимфогенных метастазов 5-летняя выживаемость составляет 75 ± 4,4%. При pN1 показатели 5-летней выживаемости статистически значимо хуже – 37,9 ± 4,2%. При pN2 показатель 5-летней выживаемости статистически значимо хуже – 11,6 ± 4,9%. При поражении более 15 узлов (pN3) никто из пациентов не пережил 24 месяца наблюдения (рис. 1).
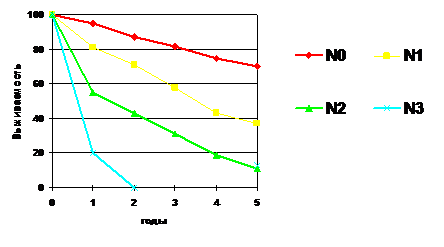
Рис. 1 Общая выживаемость больных в зависимости от лимфогенной распространённости процесса.
На основании вышеуказанной классификации были проанализированы результаты выживаемости в зависимости от стадии опухолевого процесса.
После проведённого планового гистологического исследования больные по стадиям распределились следующим образом: I стадия -,9%), II стадия-8 (11,2%), IIIА стадия,4%), IIIВ стадия,1%), IV стадия заболевания,4%).
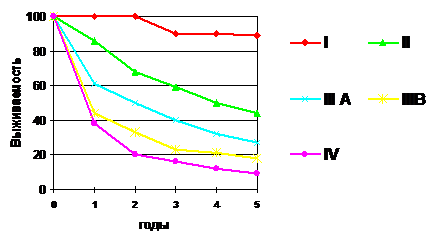 |
Рис. 2. Общая выживаемость больных в зависимости от стадии опухолевого процесса
Таким образом, по результатам проведённого нами исследования, наиболее статистически значимыми параметрами в отношении риска развития регионарных лимфогенных метастазов оказались следующие параметры опухолевого процесса: глубина инвазии опухоли в стенку желудка, размер новообразования, степень дифференцировки, распространение опухолевой инфильтрации на пищевод.
В соответствии с этим нами была разработана математическая модель, которая позволяет отнести пациента в группу с отсутствием (N-) или наличием (N+) метастазирования в регионарные лимфоузлы:
![]()
![]()
где, G1 – глубина инвазии опухоли, G2 – размер опухоли, G3 – переход опухоли на пищевод, G4 – степень дифференцировки опухоли.
Диагностическая точность при определении распространённости процесса по регионарным лимфатическим узлам составила 93% .
По предложенной нами математической модели наиболее высокий риск лимфогенного метастазирования отмечен при следующих характеристиках злокачественного процесса: инвазии опухоли в серозный слой и выход опухоли за пределы желудочной стенке, размере опухоли более 3,0 см, локализации в кардиоэзофагеальном переходе и субтотальное или тотальное поражение органа, низкой степени дифференцировки.
Риск лимфогенного метастазирования оказался минимальным при размерах первичной опухоли менее 3,0 см – 6,3%, а также при высокодифференцированном внутрислизистом раке – 0%. У пациентов с низким риском лимфогенного метастазирования возможно сокращение объёма лимфодиссекции. Однако, современные методы исследования (эхография, компьютерная и магниторезонансная томография, радионуклидная диагностика и др.) не могут дать точного ответа о наличии или отсутствии метастазов в лимфатических узлах на этапе предоперационного обследования. Поэтому больным, имеющим низкий риск лимфогенного метастазирования, для оптимизации объема перигастральной лимфодиссекции необходима разработка надежных методов интраоперационной оценки состояния регионарного лимфатического аппарата, одним из которых является исследование «сторожевых» лимфатических узлов.
Исследование «сторожевых» лимфатических узлов
В соответствии с вышеизложенным, следующим этапом исследования была оценка эффективности радионуклидной детекции «сторожевых» лимфатических узлов у больных раком желудка и на основании этого определение показания для оптимального объёма перигастральной лимфодиссекции. Концепция СЛУ была предложена R. M. Cabanas в 1977 году. Она основана на предположении, согласно которому метастазы в регионарных лимфатических узлах возникают в определенном порядке, обусловленном анатомическими особенностями лимфооттока от того или иного отдела желудка. При этом, как правило, один или несколько регионарных лимфатических узлов, называемых «сторожевыми», первыми стоят на пути оттока лимфы и, следовательно, первыми поражаются мигрирующими с током лимфы опухолевыми клетками.
В данный раздел исследования было включено 46 пациентов основной группы, которым выполнялась радикальная операция с перигастральной лимфодиссекцией D2. Всем пациентам был введён радиоактивный лимфотропный коллоид (99mTc-«Nanocis») в дозе 80 MBq. Инъекции РФП выполнялись по периметру опухоли в 4-х точках (в дозе 20 MBq в каждой инъекции). Детекция СЛУ в операционной осуществлялся при помощи гамма-зонда НТЦ и гамма-детектора Gamma Finder®II. Исследуемый лимфатический узел рассматривался как сторожевой, если его радиоактивность как минимум втрое превышала радиоактивность окружающих тканей. Нами был разработан и внедрён в клиническую практику новый способ визуализиции СЛУ, который заключался в следующем: лимфотропный РФП, меченный 99mТс (например, Nanocis) вводился в дозе 10 МБк по периметру опухоли в четырёх точках (соответственно четырём бассейнам метастазирования рака желудка) паратуморально непосредственно во время операции (до выполнения лимфодиссекции), далее осуществляют поиск СЛУ с помощью цифрового гамма-зонда.
Предложенный нами способ визуализации СЛУ при раке желудка, позволил не только обнаружить СЛУ, но и также во время операции контролировать так называемые «skip» метастазы.
В итоге СЛУ удалось идентифицировать у 43 пациентов (93,5%). У трёх пациентов (6,5%) СЛУ не были выявлены. Всего определен 91 СЛУ. Количество выявленных на одного пациента СЛУ составило от 1 до 4 (среднее количество выявленных СЛУ – 2,0). Детекция СЛУ в каждом бассейне и последующее плановое гистологическое исследование проводилось раздельно. Наиболее часто нами были выявлены СЛУ во втором – 45 СЛУ (49,4%) и третьем бассейнах регионарного метастазирования по – 21 СЛУ (23,1%).
При исследовании удалённых лимфоузлов у 22 пациентов (47,8%), выявлено наличие метастатического поражения сторожевых лимфоузлов, при этом во всех случаях были обнаружены метастазы, как минимум, в одном последующем лимфатическом узле соответствующего коллектора. У 24 больных (52,2%) отсутствовало метастатическое поражение СЛУ и дистальные лимфоузлы были интактны. Таким образом, в нашем исследовании мы не наблюдали феномена «прыгающих» метастазов. Напротив, наблюдалась чёткая последовательность лимфогенного метастазирования рака желудка соответственно бассейнам регионарного лимфооттока по .
При сравнительной оценке диагностической эффективности методики определения СЛУ в зависимости от способа введения РФП, установлено, что при эндоскопических субмукозных инъекциях препарата 99mTc-«Nanocis», что чувствительность, специфичность и точность составили 75%, 100%, 87%, при интраоперационном субсерозном введении РФП эти показатели равнялись – 93%, 100% и 96% соответственно. Таким образом, методика определения СЛУ с интароперационным введением РФП является более эффективной и может быть рекомендована к практическому применению в условиях специализированного лечебного учреждения.
Учитывая закономерности лимфогенного метастазирования рака желудка, а также исследование «сторожевых» лимфатических узлов нами предложен следующий алгоритм хирургического лечения рака желудка (рис. 3): на основании проведённого комплексного обследования пациенту устанавливается диагноз операбельный рак желудка. Далее определяется степень риска лимфогенного метастазирования (основные морфологические характеристики опухоли + математическая модель). В том случае, если у пациента имеется высокий риск лимфогенного метастазирования, ему показана радикальная операция с перигастральной лимфодиссекцией в объёме D2. В том случае, что прогнозируется низкий риск метастатического поражения лимфатического аппарата, необходимо исследование «сторожевых» лимфатических узлов. При наличии в СЛУ, как минимум одного метастатического очага показано оперативное вмешательство с перигастральной лимфодиссекцией D2, в случае отсутствия метастазов в СЛУ возможно уменьшение стандартного объёма лимфодиссекции.
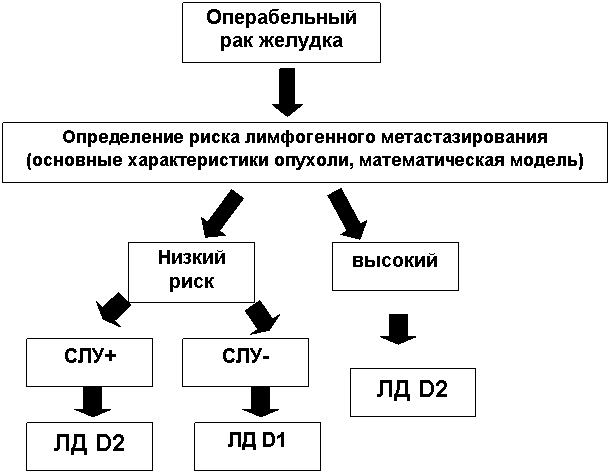

Рис. 2. Алгоритм хирургического лечения больных операбельным раком желудка.
Выводы
1. Лимфодиссекция D2 позволяет улучшить общую 5-летняя выживаемость больных раком желудка по сравнению с лимфодиссекцией D1 – 66,1 ± 2,1 % и 21,6 ± 3,4%, при недостоверных различиях в частоте послеоперационных осложнений – 10,5 ± 3,1% и 21,2 ± 3,2% и летальности – 8,3 ± 1,7% и 9,1 ± 1,7% соответственно.
2. Основным фактором, определяющим отдаленные результаты хирургического лечения рака желудка, является лимфогенная распространенность опухолевого процесса. При N0 общая пятилетняя выживаемость составила 75 ± 4,4%, при N1 – 37,9 ± 4,2%, при N2 – 11,6 ± 4,9%, при N3 – 0%.
3. Разработана математическая модель, позволяющая с точностью 93% определить риск лимфогенного метастазирования рака желудка. Основными прогностическими критериями модели являются степень инвазии опухолевого процесса, размер, локализация и степень дифференцировки опухоли.
4. Интраоперационная радиометрическая индикация после субмукозного введения радиоактивного коллоида во время хирургического вмешательства позволяет с чувствительностью 96,7 %, точностью 97,4% и специфичностью 100% определять «сторожевой» лимфатический узел. Независимо от стадии опухолевого процесса частота выявления «skip» метастазов составила 0%.
5. Исследование «сторожевых» лимфатических узлов показано пациентам с высокодифференцированным раком тела и антрального отдела желудка, распространенностью Т1, размером менее 3 см. При метастатическом поражении СЛУ показано выполнение радикальной операции с лимфодиссекцией D2, при интактных СЛУ у больных с вышеперечисленными характеристиками опухоли операцией выбора является перигастральная лимфодиссекция меньшего объёма.
Практические рекомендации:
1. Для определения сторожевых лимфатических узлов при раке желудка более предпочтительной является методика интраоперационного субсерозного введения РФП.
2. Наличие позитивных «сторожевых» лимфатических узлов у пациентов с поражением тела или антрального отдела желудка, с инвазией в пределах подслизистого слоя, аденокарциноме высокой степени дифференцировки является показанием для радикальной операции с перигастральной лимфодиссекцией D2. При негативных «сторожевых» лимфатических узлах с аналогичными клинико-морфологическими характеристиками возможно сокращение объёма лимфодиссекции.
Список опубликованных работ по теме диссертации:
Августинович подходы к комбинированному лечению рака желудка [текст] / , , // Сборник статей областной клинической больницы: Материалы научно-практической конференции. – Томск, 2002. – С 51-52. Августинович расширенной лимфодиссекции в комбинированном лечении рака желудка [текст] / // Материалы Всероссийской студенческой научной конференции им . – Томск, 2004. – С. 143-144. Августинович методы выявления «сторожевых» лимфатических узлов у онкологических больных [текст] / , , // Медицинские и экологические эффекты ионизирующего облучения (MEEIR-IV): Материалы IV международной научно-практической конференции, посвящённой 50-летию образования филиала № 2 Государственного научного центра института биофизики. – Томск, 2007. – С. 228-229. Августинович методы исследования в выявлении «сторожевых» лимфатических узлов [текст] / , , // Сибирский онкологический журнал. – 2008. – № 4 (28). – С. 5-10. «Сторожевые» лимфатические узлы: их поиск и значение при раке желудка [текст] / , // II международный конкурс молодых учёных-медиков. – Курск, 2008. – С. 67-68. Августинович расширенно-комбинированных операций при местно-распространённом раке желудка [текст] / , // Лечение рака в XXI веке: Материалы III научно-практической конференции молодых специалистов-онкологов. – Челябинск, 2008. – С 3-5. Августинович -комбинированные операции при раке желудка [текст] / , , // I Международная конференция по торако-абдоминальной хирургии (К 100-летию со дня рождения академика ): Сборник тезисов. – М., 2008. – С. 198. Августинович опыт определения «сторожевых» лимфатических узлов у больных раком желудка [текст] / , , // Совершенствование онкологической помощи в современных условиях: Материалы Российской научно-практической конференции с международным участием. – Барнаул, 2008. – С. 72-73. Августинович результаты комбинированного лечения рака желудка с применением интраоперационного облучения [текст] / , , // Совершенствование онкологической помощи в современных условиях: Мат. Российской научно-практической конференции с международным участием. – Барнаул, 2008. – С. 173-174. Августинович расширенно-комбинированных операций в лечении местнораспространенного рака желудка [текст] / , , // Совершенствование онкологической помощи в современных условиях: Материалы Российской научно-практической конференции с международным участием. – Барнаул, 2008. – С. 174-175. Августинович доступа при оперативном лечении кардиоэзофагеального рака [текст] / , , // Диагностика и лечение опухолей грудной полости: Материалы Всероссийской научно-практической конференции. – СПб., 2008. – С. 94-95. Августинович «сторожевых» лимфатических узлов при раке желудка [текст] / , , // Достижения современной лучевой диагностике в клинической практике: Материалы конференции, посвященной 120-летию лечебного факультета Сибирского государственного медицинского университета. – Томск, 2008. – С. 239-240. Августинович определение «сторожевых» лимфатических узлов при раке желудка – способ выбора оптимальной тактики хирургического лечения и прогноза [текст] / , , // Достижения современной лучевой диагностике в клинической практике: Материалы конференции, посвященной 120-летию лечебного факультета Сибирского государственного медицинского университета. – Томск, 2008. – С. 246-248. Августинович определения «сторожевых» лимфатических узлов у больных местно-распространённым раком желудка [текст] / , // Актуальные вопросы экспериментальной и клинической онкологии: Материалы III региональной конференции молодых учёных им. академика . – Томск, 2008. – Сибирский онкологический журнал. – 2008. – Прил. №1. – С. 7-8. Avgustinovich A. V. Detection of sentinel lymph nodes in patients with gastric cancer [текст] / S. G. Afanasyev, A. V. Avgustinovich, V. I. Chernov, I. G. Sinilkin, M. Y. Volkov // Annals of Oncology. – 2008. – Vol. 19, Suppl. 6. – P. 024 Августинович «сторожевых» лимфатических узлов у больных раком желудка [текст] / , , // Материалы V съезда онкологов и радиологов СНГ. – Ташкент, 2008. – С. 272. Avgustinovich A. V. Detection of sentinel lymph nodes in gastric adenocarcinoma [текст] / I. G. Sinilkin, V. I. Chernov, A. V. Avgustinovich, S. G. Afanasyev, A. A. Titskaya, M. B Karakeshisheva // In Abs. book: The Sixth International Congress of the Choatian Society of Nuclear Medicine. – Choatia, Opatija, 2008. – P. 42. – O-23. Avgustinovich A. V. Detection of Sentinel Lymph nodes in Gastric Cancer [текст] / V. I. Chernov, I. G. Sinilkin, A. V. Avgustinovich, S. G. Afonasyev, A. A. Titskaya // Annual Congress of the EANM. – Munich, Germany, 2008. – P. 232. Августинович оптимизации объема лимфодиссекции у больных операбельным раком желудка [текст] / , , // Реформа онкологической службы УФО и идеология развития позитронной эмиссионной томографии в регионах: Материалы Российиской научно-практической конференции. – Челябинск, 2009. – С. 23-24. Августинович «сторожевых» лимфатических узлов у больных раком желудка [текст] / , , // Материалы III Евразийского радиологического форума. – Астана, 2009. – С. 89. Августинович оптимизации объёма лимфодиссекции у больных операбельным раком желудка и кардиоэзофагеальным раком [текст] / , , // Актуальные вопросы экспериментальной и клинической онкологии: Материалы IV региональной конференции молодых учёных им. ак. . – Томск, 2009. – Сибирский онкологический журнал. 2009. – Прил. № 1. – С. 10-11. Августинович лимфогенного метастазирования рака желудка [текст] / , , // Пути повышения эффективности онкологической службы Российской Федерации: Материалы Всероссийской научно-практической конференции с международным участием. – Казань, 2009. – С. 28-30.
Патент:
1. Способ диагностики «сторожевых» лимфатических при раке желудка. , , Синилкин на изобретение № 000 от 10.05.09. Бюллетень № 13 от 10.05.09 (по заявке /14 от 18.10.07).
Список использованных сокращений:
СЛУ – «сторожевой» лимфатический узел
РЖ – рак желудка
ЛД – лимфодиссекция
РФП – радиофармпрепарат
РЛУ – регионарный лимфатический узел


