В настоящее время у нас налажено производство деионизированного желатиноля — модежел, представляющего значительно большую ценность для перфузии. В европейских странах, как мы упомянули выше, также производят препараты желатины. Для примера назовем Haemacel и Gelifiindol (ФРГ) и Gelplex (Италия). В отличие от желатиноля эти, как и другие препараты желатина западного производства, имеют стабильный ионный состав.
Прегюраты гндроксиэтилкрахмта Эта группа коллоидов получена из амилопектина, являющегося сырьем для гидроксиэтилового крахмала. Выпускают б и 10% раствор гидроксиэтилового крахмала на изотоническом растворе натрия хлорида. К препаратам относятся волекам (Россия), оксиамал (Беларусь), 6-HES (ФРГ, Япония). Молекулярная масса препара*-тов около 200 тыс. дальтонов.
Принято считать, что к достоинствам этих растворов относятся относительно длительное пребывание в сосудистом русле, дешевизна и минимальные аллергические реакции. Вместе с тем и фирма Fresenius (ФРГ) указывает, что её препарат HAES-Steril 6% может вызывать анафилактоидные реакции, которые могут колебаться от слабых субъективных жалоб до остановки дыхания и сердца.
Наш незначительный опыт работы с волека-мом свидетельствует о нецелесообразности применения во время одной перфузии более одного флакона препарата (400 мл). У больных, у которых использовали большее количество волекама, чаще производили рестернотомии по поводу кровотечения. Малое число наших наблюдений такого рода позволяет лишь предположительно высказаться на этот счет.
Заканчивая краткое описание растворов для гемодилюции, применяемых для проведения искусственного кровообращения, считаем необходимым высказать следующее соображение. В зарубежных странах (в частности США) получила широкое распространение практика заправки аппарата искусственного кровообращения одними кристаллоидиыми растворами, не применяя коллоидов. Это относится к операциям только у взрослых больных. Ввиду того, что у абсолютного большинства наших больных в различной степени выражены дис - и гипопротеинемии (вследствие характера: их питания, патологического процесса и т. д.), мы считаем абсолютно неприемлемым заправлять аппарат искусственного кровообращения без того или иного коллоидного раствора. Это положение тем более относится к больным детям. Кратковременная попытка отойти от этого протокола пфя влиянием зарубежного опыта была очень быстро прекращена ввиду заметного увеличения числа послеоперационных больных с нарушением оксигенирующей функции легких и сердечной недостаточностью.
5.ТЕМПЕРАТУРНЫЙ РЕЖИМ ПЕРФУЗИИ
Исторически начало операций с искусственным кровообращением совпало по времени с применением в кардиохирургии метода наружной гипотермии Это обстоятельство, а также малая мощность первых оксигенаторов, способствовали тому, что ги-потермическая перфузия заняла доминирующее положение в перфузиологии, что имеет место и сегодня. Принято считать, что гипотермическая перфузия способствует сохранности внутренних органов ( в первую очередь мозга и миокарда), а также уменьшает травму крови в результате более низкой объемной скорости перфузии.
В рамках настоящей работы мы не будем обсуждать плюсы и минусы (а их более, чем достаточно) гипотермического искусственного кровообращения. Ограничимся лишь констатацией обшей ситуации с температурным режимом перфузии на сегодняшний день.
Существует ряд классификаций характера перфузии в зависимости от температуры тела больного. В настоящее время, как нам кажется, наиболее реальной представляется выделение нормотермического искусственного кровообращения (температура тела 34—37° С); перфузии с умеренной гипотермией при температуре 26-30° С; и искусственного кровообращения с глубокой гипотермией (20-22° С и ниже), сопровождающейся обычно временным прекращением перфузии (циркулярный аррест). Это разделение, имеющее, как и всякая классификация, схематичный характер, важно чисто в рабочее плане.
В целом ситуацию в современной перфузиологии в плане выбора оптимального режима искусственного кровообращения можно характеризовать как "смещение" в сторону более высокой минимальной температуры перфузии, чем это наблюдалось в прежние годы.
Сказанное выше, понятно, не относится к перфузиям с глубокой гипотермией и остановкой кровообращения, проводимым при некоторых операциях по поводу аневризмы аорты и сложных врожденных пороков сердца.
В настоящее время абсолютное большинство перфузии при операциях реваскуляризации миокарда или при пороках сердца, осуществляют в режиме минимальной гипотермии или нормотермии. Число нормотермических перфузии сегодня составляет около 20% от общего количества перфузии.
Общеизвестно, что при охлаждении и согревании крови больного наблюдается выраженный градиент температур между различными сосудистыми областями. Разумеется, возможно многоканальное мо-ниторирование температуры в различных "точках интереса". Практически, однако, обычно ограничиваются постановкой одного термодатчика в носо - или ротоглотку, пищевод, прямую кишку или в область наружного слухового прохода.
Температуру в артериальной и венозной магистрали аппарата искусственного кровообращения определяют не во всех клиниках.
Мы считаем целесообразным измерять температуру в магистралях экстракорпоральной системы. Практически все современные оксигенаторы имеют гнезда для установки и артериального и венозного термодатчиков
В настоящее время получает распространение пассивное охлаждение больного, когда искусственное кровообращение проводят, сначала не подавая в теплообменник оксигенатора воды. При этом температура тела больного уменьшается до 33—35° С. После завершения основного этапа операции в теплообменник начинают подавать теплую воду, согревая больного до нормальной температуры. Такую термотактику используют, например, при операциях открытой митральной комиссуротомии, некоторых видах коронарного шунтирования, несложных септальных дефектах.
Особо отметим, что необходимым показанием к проведению гипотермической перфузии является гипоксический удар, перенесенный больным до начала или во время искусственного кровообращения, будь то остановка сердца до перфузии или та или иная аварийная ситуация во время нее. В этих ситуациях гипотермическое искусственное кровообраще-. ние наряду с медикаментозными средствами является помимо прочего и методом профилактики или лечения отека мозга.
Коль скоро у конкретного больного решено проводить гипотермическую перфузию, перфузиолог должен грамотно поддерживать температурный режим больного. Градиент между температурой хладоа-гента (подаваемой в теплообменник оксигенатора воды) не должен более, чем на 10° С, отличаться от температуры крови (перфузата). Об этом сказано во всех инструкциях к оксигенаторам. Если есть необходимость в снижении объемной скорости перфузии, то к этому можно прибегать лишь после практической ликвидации температурного градиента между различными органами и тканями.
В нашей повседневной практике, проводя искусственное кровообращение в режиме умеренной гипотермии, мы не снижаем объемной скорости по сравнению с расчетным перфузионным индексом (2,5 л/ мин м2. у взрослых и 3,0 л/ мин м2. у детей) Хотя с точки зрения кислородного баланса снижение объемной скорости при температуре тела 26—30° С и возможно, но мы предпочитаем не делать этого для профилактики возникновения кислородной задолженности на этапе согревания. Более подробно этот вопрос освещается в монографии В П Осипова (1976).
Сниженную объемную скорость перфузии вплоть до циркуляторного арреста мы осуществляем лишь по хирургическим показаниям или, как было сказано выше, в случае внезапной гипоксии.
Поддержание кислотно-щелочного состояния при проведении гипотермической перфузии мы осуществляем в режиме альфа-стат, о чем детально говорится в соответствующей главе данной работы. Методика искусственного кровообращения с глубокой гипотермией описывается в главе об искусственном кровообращении при операциях на аорте.
6.УЛЬТРАФИЛЬТРАЦИЯ КРОВИ ПРИ ОПЕРАЦИЯХ С ИСКУССТВЕННЫМ КРОВООБРАЩЕНИЕМ
Ультрафильтрация (гемофильтрация, ультрафильтрационная гемоконцентрация - УФГ) — это метод удаления из крови воды, электролитов и других соединений с относительно малой молекулярной массой путем их конвективного транспорта через полупроницаемую мембрану за счет градиента гидростатического давления по обе стороны мембраны.
Все соединения, молекулярная масса которых позволяет проникнуть через поры мембраны ультрафильтра, удаляются с ультрафильтратом. Метод позволяет уменьшить объем плазмы и внеклеточной жидкости. Перемещение интерстициальной жидкости в сосудистое русло происходит вследствие увеличения коллоидноонкотического давления плазмы за счет повышения в ней концентрации белков, не фильтрующихся через мембрану ультрафильтра. Таким образом, ультрафильтрация представляет возможность удаления избытка электролитов плазмы, а также токсических низко - (или) среднемолекулярных соединений независимо от их происхождения (эндо: генная интоксикация, передозировка препаратов и т. д.).
При операциях с искусственным кровообращением ультрафильтрацию используют с 1976 г. В настоящее время этот метод является общепризнанным и широко применяемым при операциях на открытом сердце. Он улучшает реологические свойства крови больного, снижает ее травму, а также расход донорской крови и уменьшает или исключает синдром гомологической крови.
Широкое применение в кардиохирургической практике бескровной заправки аппарата искусственного кровообращения и метода криcталлоидной кардиоплегии может приводить к такому разведению крови больного, когда гемодилюция перестает быть управляемой. Чрезмерная гемодилюция приводит к уменьшению кислородной емкости крови, нарушению ее свертывающей системы, осмотического и коллоидного гомеостаза, увеличению объема внеклеточной жидкости, повышению интерстициального давления. Все это может приводить к развитию в ближайшем постперфузионном периоде острой сердечной или (и) легочной недостаточности ( так называемое "отравление водой").
Применяющаяся для профилактики таких осложнений методика эвакуации из операционного поля "отработанного" кардиоплегического раствора обычным "грязным" отсосом неизбежно сопровождается непреднамеренной кровопотерей и в итоге увеличивает количество переливаемой донорской крови. Из существующих способов реверсии гемодиллюции, к которым относится медикаментозная стимуляция диуреза, применение устройств "cell saver" и ультрафильтрация, наиболее эффективным во время искусственного кровообращения является именно ультрафильтрация.
Для УФГ применяют одноразовые диализаторы аппарата "искусственная почка" или специальные гемоконцентраторы. В зависимости от формы мембраны существуют два типа устройств для ультрафильтрации* пластинчатые (устаревшие в настоящее время) и половолоконные или капиллярные. Пластины помещены в жесткий корпус, между листами мембраны помещают изолирующие прокладки (устройство типа "сэндвича"). Толщина мембраны составляет 20—30 мкм. С одной стороны мембраны находится полость, по которой протекает кровь (внутрення полость ультрафильтра), с другой стороны — полость, к которой присоединяют источник вакуума1 (внешняя полость ультрафильтра).
 1 Ряд современных ультрафильтров может работать без вакуума
1 Ряд современных ультрафильтров может работать без вакуума
В половолоконных устройствах кровь проходит внутри капилляров, образованных из синтетических мембран. Капилляры располагаются в жестком цилиндрическом корпусе. Внутренний диаметр капилляра равен 200—300 мкм. Число капилляров колеблется в зависимости от поверхности фильтрующей мембраны и составляет величину порядка 5—10 тыс. и более. При этом поверхность мембраны варьирует от 0,5 до 2—-2,5 кв. м. В эксплуатации половолоконные устройства удобнее, чем пластинчатые. Они компактнее и имеют меньший заправочный объем. Кроме того капилляры обеспечивают более стабильный кровоток, что уменьшает концентрационную поляризацию, выражающуюся в оседании белков на поверхности мембраны и образовании пленки, ухудшающей работу ультрафильтра.
Мембраны, изготовляемые специально для ультрафильтрации крови, как правило, относятся к асимметричным. Они представляют тонкий полимерный слой толщиной 0,1—1 мкм, уложенный на пористую основу толщиной 100—200 мкм. Тонкий слой является собственной мембраной, а пористая основа необходима для придания всей структуре прочности. Такие мембраны действуют как поверхностный фильтр. Вещества, которые он не пропускает, не оседают внутри фильтра, а остаются на его поверхности, откуда они смываются потоком крови.
В процессе ультрафильтрации кровь движется вдоль мембраны. При этом вода плазмы, электролиты и мелкие молекулы фильтруются через мембрану и удаляются из крови. Движущей силой процесса является трансмембранное давление, представляющее алгебраическую сумму давления во внутренней полости микрофильтра (между мембраной и корпусом) и давления на входе и выходе устройства. Последнее зависит от сопротивления ультрафильтрата току крови. Для его увеличения можно создать ограничение на выходе из ультрафильтра, например, частично пережав трубку, по которой отводится кровь. Однако считается, что такая манипуляция нежелательна, так как может приводить к травме форменных элементов крови. Для увеличения трансмембранного давления можно создавать отрицательное давление во внешней полости ультрафильтра, присоединяя её к источнику вакуума (см. выше).
Максимальное трансмембранное давление не должно превышать 700—800 мм рт. ст. Более высокое давление не повышает производительности ультрафильтра, но может вызывать гемолиз и приводить к разрыву мембраны.
В результате ультрафильтрации пропорционально количеству удаленной жидкости увеличивается концентрация форменных элементов крови. Гепавин частично выводится с ультрафильтратом, и его уровень в плазме несколько снижается, поскольку при ультрафильтрации кровь проходит через дополнительный экстракорпоральный контур, теоретически имеется опасность возникновения гемолиза. Однако экспериментальные и клинические исследования показали, что гемолиз не возрастает.
При проведении ультрафильтрации рекомендуется постоянно следить за уровнем калия сыворотки, так как удаление большого количества ультрафильтрата (свыше 5 л у взрослого) может вызвать гипокалиемию. Предполагается, что выход калия из клетки может происходить в результате обезвоживания межклеточного пространства.
Ультрафильтрат по своему составу соответствует первичной моче, образующейся в почках в результате клубочковой фильтрации. Осмолярность крови и ультрафильтрата, полученного во время искусственного кровообращения, практически не отличается. Онкотическое давление в ультрафильтрате из-за отсутствия в нем белка не определяется. Концентрация электролитов, глюкозы и креатинина ультрафильтрата и крови совпадают. В ультрафильтрате были обнаружены токсины с малой и средней молекулярной массой (так называемые "средние молекулы"), о чем мы упоминали выше. -
При операциях с искусственным кровообращением к ультрафильтрации крови существуют пред-и (по преимуществу) интраоперационные показания. К предоперационным показаниям, которые имеют относительный характер, относятся заведомо длительное искусственное кровообращение (свыше 1,5—-2-х часов); наличие у больного отеков любой этиологии; выраженная недостаточность выделительной функции почек, особенно при наличии олиго-анурии; выраженная анемия; септическое состояние:
 Однако чаще всего показания к ультрафильтрации возникают по ходу операции и искусственного кровообращения или после окончания последнего. К таким показаниям относится избыточная гемодилю-ция, не купируемая медикаментозно, со снижением гематокрита менее 20% (или) уменьшением коллоидно-осмотического давления крови ниже 18 мм рт. ст. на фоне увеличенного объема циркулирующей крови (высокий уровень крови в оксигенаторе).
Однако чаще всего показания к ультрафильтрации возникают по ходу операции и искусственного кровообращения или после окончания последнего. К таким показаниям относится избыточная гемодилю-ция, не купируемая медикаментозно, со снижением гематокрита менее 20% (или) уменьшением коллоидно-осмотического давления крови ниже 18 мм рт. ст. на фоне увеличенного объема циркулирующей крови (высокий уровень крови в оксигенаторе).
 Перед началом работы ультрафильтр необходимо отмыть стерильным физиологическим раствором. Невыполнение этого требования может вызвать гемолиз и привести к нарушению функции почек вследствие попадания в кровь больного глицерина, которым при изготовлении заполняют капилляры или покрывают плоскую мембрану ультрафильтра. Методика отмывки ультрафильтра изложена в инструкции, прилагаемой к диализатору или гемоконцентратору.
Перед началом работы ультрафильтр необходимо отмыть стерильным физиологическим раствором. Невыполнение этого требования может вызвать гемолиз и привести к нарушению функции почек вследствие попадания в кровь больного глицерина, которым при изготовлении заполняют капилляры или покрывают плоскую мембрану ультрафильтра. Методика отмывки ультрафильтра изложена в инструкции, прилагаемой к диализатору или гемоконцентратору.
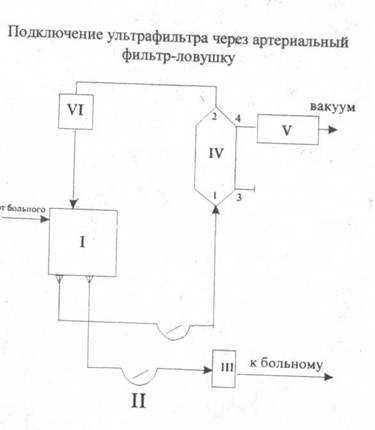
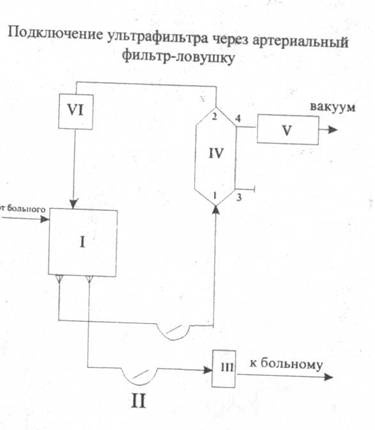
К аппарату искусственного кровообращения ультрафильтр можно подключить с помощью отдельного роликового насоса, без использования насоса (через артериальный фильтр-ловушку) и селективно (для ультрафильтрации только содержимого кардио-томического резервуара). Эти три варианта подключения представлены на рисунках.
Подключение ультрафильтра для селективной УФГ
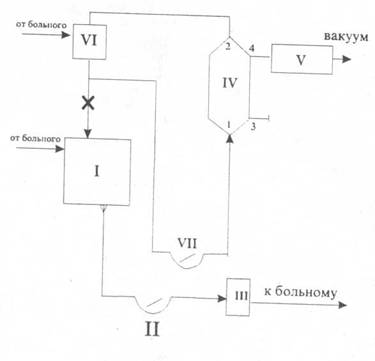
I - оксигенатор; II - артериальный роликовый насос; III - артериальный фильтр-ловушка: IV - ультрафильтр; V - резервуар для сбора ультрафильтрата; VI - кардиотомный сосуд; VII - дополнительный роликовый насос;
1, 2 - входной и выходной штуцеры ультрафильтра для крови; 3, 4 - штуцеры диализатора для днализного раствора;
Ультрафильтрацию всегда следует начинать с включения насоса или доступа крови в ультрафильтр из артериального фильтра-ловушки. Только после этого может быть подан вакуум к наружной стороне мембраны.
Кровь должна проходить через ультрафильтр со скоростью 100—300 мл/мин. При подключении ультрафильтра к артериальному фильтру-ловушке через ультрафильтр протекает примерно 10% производительности артериального насоса, которые сбрасываются обратно в оксигенатор. Для компенсации этого сброса производительность артериального насоса необходимо увеличить в таких же пределах
Ультрафильтрацию проводят до тех пор, пока не будет достигнут желаемый результат — уровня гематокрита 22—25%. Заканчивают ультрафильтрацию прекращением подачи вакуума лишь затем прекращают подачу крови в ультрафильтр. Если вновь возникает необходимость, — ультрафильтрацию продолжают.
Описанный процесс можно проводить и после окончания искусственного кровообращения, если в оксигенаторе осталось достаточное количество крови с низким гематокритом. Отконцентрированную при этом кровь переливают больному.
Ультрафильтрация не удаляет из крови белки плазмы и не изменяет концентрации в плазме веществ, уходящих с ультрафильтратом. Однако абсолютное их количество в организме больного, естественно, уменьшается. Это требует некоторого увеличения добавляемы по ходу искусственного кровообращения коррегирующих препаратов (натрия бикарбонат, калия хлорид, гепарин).
Скорость удаления ультрафильтрата из крови зависит преимущественно от величины поверхности ультрафильтра и типа применяемой мембраны. Современные ультрафильтры способны за час работы удалять из крови до 6 л жидкости. Появление в ультрафильтрате примеси крови свидетельствует о нарушении целости мембраны ультрафильтра. В этой ситуации следует заменить ультрафильтр на новый, предварительно отмыв его.
Каких-либо специфических осложнений, характерных именно для ультрафильтрации, проводимой при операциях с искусственным кровообращением — в литературе не описано. Однако, недостаточно квалифицированное применение ультрафильтрации может вызвать сгущение крови и (или) привести к гиповолемии>
Абсолютных противопоказаний к ультрафильтрации во время искусственного кровообращения нет. Она не показана при высоком (выше 25%) содержании гематокрита. При низком уровне крови в оксигенаторе, сочетающимся с низким гематокритом, ультрафильтрацию можно проводить, предварительно добавив в оксигенатор необходимое количество эритроцитарной массы.
Для выбора правильной тактики управления гемодилюцией во время искусственного кровообращения можно руководствоваться приведенной ниже схемой.
СХЕМА УПРАВЛЕНИЯ ГЕМОДИЛЮЦИЕЙ ВО
ВРЕМЯ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ
Гематокрит в % | Уровень крови в оксигенаторе | Рекомендации |
Ниже 20 | Низкий Оптимальный Высокий | Добавить эритромассу То же плюс ультрафильтра ция Ультрафильтрация |
20-25 | Низкий Оптимальный Высокий | Добавить эритромассл Не делать ничего Возможна ультрафильтрация |
Выше 25 | Низкий Оптимальный Высокий | Добавить плашозамени-тель Не дезать ничего Не делать ничего |
7. ЗАЩИТА МИОКАРДА ПРИ ОПЕРАЦИЯХ НА ОТКРЫТОМ СЕРДЦЕ
Проблема защиты миокарда при операциях с искусственным кровообращением находится на стыке кардиохирургии, кардиоанестезиологии и перфузио-логии. Ни в одном разделе оперативной кардиологии, наверно, нет такого полиморфизма в подходах и оценках, как в проблеме защиты миокарда. Практически в каждом крупном кардиохирургическом центре наблюдается "свой" подход к этой проблеме, не исключающий, впрочем, общих концепций.
Защита миокарда является существенным условием успеха операций на открытом сердце с искусственным кровообращением. С середины 50-х годов, когда кардиохирургия начала свое триумфальное шествие, стали очевидны преимущества работы на остановленном и ишемизированном сердце. Тогда же начались исследования по разработке способов и методов так называемой кардиоплегии.
Общий термин "кардиоплегия" объединяет два понятия: обездвиживание сердца во время хирургиче* ского вмешательства, т. е. собственно кардиоплегию, и консервацию сердца, т. е. сохранение его жизнеспособности на период времени, необходимый для выполнения хирургического вмешательства. Современная кардиоплегия смыкается с проблемой консервации сердца для его трансплантации.
Целью настоящего очерка является ознакомление читателя в самой общей форме с основными современными аспектами практической кардиоплегии (КП). При этом мы сознательно оставляем в стороне такие фундаментальные проблемы, как патофизиология ишемии миокарда и механизмы его репер-фузионного повреждения.
Классификация методов защиты миокарда
Знакомство с состоянием проблемы защиты миокарда во время его вынужденной ишемии при операциях на открытом сердце убеждает, что вопрос этот еще далек от окончательного решения. Предложенные к настоящему времени разные способы КП очень отличаются друг от друга, что обусловливает отсутствие их общепринятой^ классификации. Нам представляется целесообразной следующая систематизация методов КП, наиболее полно учитывающая их патофизиологические и методические особенности.
По механизму воздействия на миокард:
— ишемическая;
— электрическая (искусственная фибрилляция);
— холодовая;
— фармакологическая.
По способу применения раствора для КП:
— наружная;
— перфузионная.
По основному составу раствора для КП:
— бескровная (кристаллоидная);
— кровяная.
По месту нагнетения кардиологического раствора:
— ортоградная;
— ретроградная;
— сочетанная
Но содержанию О2 в кардиоплегическом растворе:
— с оксигенацией;
— без оксигенации.
По температурному режиму:
— холодовая (гипотермическая);
— нормотермическая.
По содержанию биологически активных веществ (БАВ):
— с использованием БАВ;
— без использования БАВ.
По времени проведения:
— непрерывная;
— периодическая.
Ишемическая КП в чистом виде по понятным причинам не нашла сколько-нибудь широкого распространения. Отдельные виртуозы-кардиохирурги иногда пережимают аорту при нормальной температуре на очень короткое время.
Искусственная фибрилляция сердца применяется в клинике с 1970 года. Электрическая фибрилляция при нормотермии уменьшает кровоток миокарда по сравнению со спонтанной фибрилляцией. При использовании этого метода рекомендуют дренировать левый желудочек через правую легочную вену, так-как растяжение фибриллирующего сердца нежелательно. Системное АД необходимо поддерживать на уровне 80—100 мм рт. ст., так как при этом ишемиче-ские изменения миокарда и уровень лактата минимальны. Сочетание искусственной фибрилляции с охлаждением крови до 20—28° С снижает потребность миокарда в кислороде, уменьшает напряжение фибриллирующего сердца и пролонгирует фибрилляцию. При искусственной фибрилляции целесообразно проводить и охлаждение эпикарда с помощью холодного раствора Рингера. Большинство современных кардиохирургов не применяет искусственной фибрилляции, так как при использовании этого метода происходит большой расход энергии миокардом и возникают нарушения его сократительной функции в послеоперационном периоде.
До недавнего времени наиболее распространенным видом защиты миокарда была перфузионная кардиоплегия кристаллоидами. Применяемые для этого растворы подразделяются в зависимости от состава на растворы с вне - и внутриклеточной активностью. К первой группе относятся растворы, близкие по концентрации основных ингредиентов к внеклеточной жидкости. Наиболее "прославленными" из них является раствор госпиталя Св. Томаса, применяемый в клинике с 1976 г. В состав этого раствора входят (в ммоль/л): калий — 16, магний — 16, кальций — 1,2, натрий — ПО. рН раствора 7,8; осмоляль-ность — 324 моем/кг. Моментальная остановка сердца достигается за счет высокого содержания калия и магния в сочетании с низкой температурой раствора.
Так называемые внутриклеточные растворы содержат минимальное количество натрия и кальция или совсем их не содержат. Так, в раствор Bretschneider входит (в ммоль/л): калий — 9, магний — 4, натрий — 15. рН раствора 7,1. Уменьшенное количество натрия позволило заполнить осмоляль-ный объем маннитолом (30 ммоль/кг) и гистидином (180ммоль/кг).
Дискуссия о преимуществах и недостатках вне - и внутриклеточных растворов выходит за рамки наших задач.
Ряд фармацевтических фирм выпускает офи-цинальные растворы для кардиоплегии Назовем некоторые из них. Фирма Abbot (США) под названием Plegisol производит раствор госпиталя Св. Томаса. Раствор Бретшнайдера под названием Kastodiol выпускается в Германии (фирма Frants Kechler Chemie). Там же фирма Fresenius производит коронарный пер-фузат Эппендорфа на основе гидроксиэтилкрахмала. Совсем недавно НПП "Биофарм" (Москва) начало серийное производство раствора для кардиоплегии и консервации донорского сердца — Консол. Раствор, изготовляемый на основе 6% полиглюкина, содержит (в ммоль/л): натрия — 110; калия — 16; кальция — 1.2; магния— 16. Кроме электролитов в состав Кон-сола входят натрия гидрокарбонат, лидокаина гидрохлорид и рибоксин. Первые клинические испытания Консола показали его высокую эффективность.
Несмотря на наличие официнальных растворов для кардиоплегии абсолютное большинство кар-диохирургических центров (как на западе, так и в России) изготавливает соответствующие растворы в своих аптеках.
Как мы отметили выше, кристаллеидная кар-диоплегия еще совсем недавно была методом выбора защиты миокарда при операциях на открытом сердце. Однако за последние годы этот вид кардиоплегии все больше уступает место перфузионной кардиоплегии с использованием аутокрови больного. Большая кислородная и буферная емкость, а также наличие колло-идно-онкотического давления делают кровяную кардиоплегию более предпочтительной, чем чистую кри-сталлоидную. Несмотря на возражения противников этого метода, указывающих на недостатки холодовой кардиоплегии (при низкой температуре сильно охлажденная кровь плохо отдает кислород вследствие смещения влево кривой диссоциации оксигемогло-бина; гипотермия вызывает агрегацию эритроцитов и повышает вязкость крови, что нарушает микроциркуляцию в миокарде), — различные варианты кровяной кардиоплегии, по-видимому, уже обошли по частоте использования "чистую" кардиоплегию кристаллоидами.
Кристаллоидные растворы для кардиоплегии перед подачей в коронарное русло охлаждают до 3— 4° С, о чем мы скажем ниже. Общепринятой практикой кардиоплегии кристаллоидами или кровяными растворами является сочетанное использование холодовой перфузионной кардиоплегии и наружного охлаждения сердца. Локальную гипотермию миокарда (topical cooling) осуществляют путем введения в полость перикарда холодного (2 — 4° С) физиологического раствора или обкладывания сердца снегом из этого раствора. Ввиду быстрого согревания холодного раствора возникает необходимость его постоянной замены. Существует методика непрерывной циркуляции холодного солевого раствора в полости перикарда ( при этом возможна его подача и в полости сердца, если оно вскрыто).
Ортоградную подачу охлажденного кардиоп-легического раствора осуществляют либо путем пункции восходящего отдела аорты проксимальнее положенного на аорту зажима, либо непосредственно в устья коронарных артерий (при операциях на аортальком клапане). Для проведения современной кар-диоплегии используют одноразовые системы, производимые рядом зарубежных фирм (Dideco /Италия/); Baxter, Bently, Shiley /США/ и др ). В состав системы входит шунт для рециркуляции раствора, гнездо для термодатчика, микрофильтр-ловушка и трубка, присоединяемая к манометру для контроля давления подачи кардиоплегического раствора. Системы для кровяной кардиоплегии рассчитаны на соотношение крови больного (артериального перфузата) и кардиоплегического раствора 1:1, 1:2 или 1:4. Это достигается использованием трубок соответствующего диаметра, располагаемых в одном роликовом насосе.
При подаче кардиоплегического раствора необходим контроль за давлением в системе. Давление более 100 мм рт. ст. может вызвать отек миокарда и (или) травму эндотелия коронарных артерий, а давление менее 80 мм рт. ст. не обеспечивает адекватной доставки кардиоплегического раствора. Объемная скорость подачи кардиоплегического раствора колеблется в широких пределах, составляя у взрослого больного от 100 до 250 (при гипертрофированном миокарде) мл/мин.
Для подачи кардиоплегического раствора (смеси) чаше всего используют роликовый насос. При более примитивных вариантах проведения кар-диоплегии раствор поступает в коронарное русло пол действием силы тяжести, вытесняется из пластикового мешка путем его сдавливания манжеткой или нагнетается из сосуда.
Дополнительной методикой ортоградной кардиоплегии является введение холодного раствора в коронарный шунт после наложения дистального анастомоза при операциях аорто-коронарного шунтирования.
Продолжительность подачи кардиоплегического раствора колеблется весьма широко, начиная от дробной подачи различной продолжительности с различными интервалами до постоянной (непрерывной) кардиоплегии на протяжении всего периода пережатия аорты.
У больных ишемической болезнью сердца вследствие субтотальных или полных стенозов коронарных артерий ортоградная кардиоплегия может быть неэффективной из-за неравномерного распределения кардиоплегического раствора между различными участками миокарда. Более оправданной при такой ситуации является ретроградная кардиоплегия, при которой кардиоплегический раствор вводят в коронарный синус или в правое предсердие (при затянутых турникетах на полых венах и пережатой легочной артерии).
Для осуществления ретроградной кардиоплегии предложены и имеются в продаже специальные катетеры с обтурирующей надувной манжетой, препятствующей вытеканию наружу вводимого раствора. Микроманометр катетер на кончике катетера для коронарного синуса позволяет определить давление в синусе, которое не должно превышать 40—50 мм рт. ст.
К преимуществам ретроградной кардиоплегии относят более адекватную защиту миокарда у больных ИБС и аортальными пороками при отсутствии риска повреждения коронарных артерий. Недостатками метода являются более медленное, чем при ор-тоградном методе, прекращение механической и электрической активности сердца (в особенности, если кардиоплегию начинают с ретроградной подачи раствора), возможность травмы коронарного синуса и коронарных вен, а также недостаточное снабжение кардиоплегическим раствором зоны правого желудочка (последний недостаток в значительной степени нивелируется при полноценном наружном охлаждении сердца).
В настоящее время наиболее широко применяют сочетание орто - и ретроградного метода карди-оплегии, при котором остановку сердца производят при ортоградной подаче раствора, переходя затем на его ретроградную подачу.
Перед подачей в коронарное русло кристалло-идных кардиоплегических растворов возможна их предварительная оксигенация. Концепция о целесообразности оксигенации кристаллоидных растворов разделяется не всеми. Так или иначе, но оксигениро-ванные кристаллоидные растворы нашли применение при операциях на открытом сердце.
Что касается применения биологически активных веществ, то с целью уменьшения проницаемости клеточных мембран миокарда и понижения содержания клеточного кальция в кардиоплегических растворах нашли применение блокаторы кальциевых каналов (верапамил, дилтиазем, нифедипин). Содержание этих препаратов составляет соответственно 0,5; 0,21: и 0,002 ммоль/л. Однако использование вышеназванных соединений одобряется не всеми, так как антагонисты кальция оказывают отрицательное хроно - и инотропное действие на миокард, замедляя проводимость в атрио-вентрикулярном узле и способствуя продолжительной остановке сердца. Эти препараты не рекомендуют применять у больных с исходно сниженными резервами миокарда.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



