При операциях на дуге аорты используют также срединную стернотомию. Для артериальной канюли обнажают общую бедренную артерию. Если поражение захватывает проксимальную половину или более нисходящего отдела грудной аорты, производят левостороннюю боковую торакотомию или дополнительным резервом через четвертое межреберье слева превращают срединный доступ в Т-образный. После введения гепарина канюлируют бедренную артерию и устанавливают двухступенчатый катетер в правое предсердие и нижнюю полую веру. Перфузию начинают с перфузионным индексом 2,2—2,4 л/мин м. Левый желудочек дренируют через правую верхнюю легочную вену. Гематокрит рекомендуют снижать до 20% и ниже. При большом (свыше 6 л) объеме циркулирующей крови больного широко практикуют забор аутокрови.
В последнее время в американских центрах, где оперируют на аорте, получила распространение методика принудительной аспирации венозной крови из правого предсердия с помощью длинного тонкостенного катетера, вводимого через бедренную вену. Аспирацию осуществляют с помощью центрифужного насоса в специальный резервуар. Используя второй центрифужный насос, венозную кровь из этого резервуара прокачивают через мембранный оксигенатор и вводят в бедренную артерию.
После того, как температура в носоглотке достигает 12—15° С, а в прямой кишке она становится 15—18° С, начинают проведение циркуляторного арреста (т. е. временного прекращения экстракорпорального кровообращения). Больного переводят в положение Тренделенбурга, а 20—25% от объема циркулирующей крови больного дренируют в оксигенатор, после чего пережимают венозную магистраль. Некоторые авторы рекомендуют дренировать около половины крови и даже весь объем. Однако при этом возрастает опасность аспирации воздуха в артерии мозга. Защита миокарда при этих вмешательствах в принципе аналогична таковой при операциях на всходящей аорте.
Принято считать, что безопасной в плане отсутствия поражений центральной нервной системы при температуре 15—18° С является продолжительность циркуляторного арреста, не превышающая 45— 60 мин. Во время арреста рекомендуют продолжать минимальную (200—400 мл/мин) циркуляцию по шунтовой линии оксигенатора.
Согревание проводят с тем же градиентом (порядка 12° С между температурой воды и крови), что и охлаждение. При согревании перфузионный индекс составляет 2,4—2,6 л/мин м2 Обращают особое внимание на коррекцию метаболического ацидоза. Согревание считают завершенным при температуре в носоглотке 37° С и в прямой кишке 34° С. Тром-бомассу, свежезамороженную плазму и другие средства усиления свертывания крови вводят не всегда. Это же относится к введению эпсилон-аминокапроновой кислоты и апротинина. Оптимальным гематокритом в конце операции считают не более 27%.
За последние годы для повышения безопасности циркуляторного арреста на его фоне начали проводить анте - или ретроградную перфузию мозга. Ан-теградную перфузию осуществляют через безымянную и левую общую сонную артерию. Некоторые авторы предваряют антеградноД перфузии мозга "промывание мозгов" охлажденным кристаллоидным или кровяным раствором (цереброплегия по аналогии с кардиоплегией). Собственно антеградную перфузию мозга проводят в режиме умеренной гипотермии (26—28° С).
Ретроградная перфузия мозга в настоящее время, кажется, более распространена, чем антеград-ная. Ее проводят в постоянном или перемежающемся режиме через катетер в верхней полой вене при раздельной катетеризации полых вен Строго говоря, это выглядит как ретроградная перфузия головы, а не изолированного мозга. Объемная скорость ретроградной перфузии мозга не превышает 400 мл/м'ин. Достоинством этой методики является практически отсутствие вероятности воздушной эмболии мозга, так как его артерии заполнены жидкостью.
Перфузия мозга при циркуляторном аресте оправдана еще и потому, что даже во время глубокой гипотермии метаболизм головного мозга полностью не прекращается.
При операциях на нисходящей грудной и то-ракоабдоминальной аорте в зависимости от локализации поражения и "настроя" оперирующей бригады возможны следующие варианты: простое пережатие аорты без какой бы то ни было перфузии (используется крайне редко); наложение временного пассивного шунта из проксимального отдела аорты в дисталь-ный (применяется также редко); обход из левых отделов сердца (обычно из предсердия) в бедренную артерию (для этой цели сейчас используют центрифужный насос); искусственное кровообращение с перфузией через тройник на артериальной магистрали восходящей аорты и бедренной артерии.
Производительность обхода зависит от величины кровоснабжаемой при обходе зоны. Обход проводят под контролем давления в левом предсердии и электроэнцефалограммы.
Применяют также методику обхода из бедренной вены в бедренную артерию с оксигенацией с производительностью ( ПИ до 1,5 л/мин м2). Иногда операции на рассматриваемом отделе аорты проводят в условиях циркуляторного арреста и глубокой гипотермии.
Говоря о перфузионном пособии при операциях на ннсх(н)ящеи грудной и торакоа&кпшншъиои аорте, следует особо отметить, что при этой локализации аневризмы аорты обычно используют левый торакоабдоминальный доступ с резекцией пятого и шестого ребер и радиальным разрезом диафрагмы. Для проведения полноценного искусственного кровообращения через бедренную артерию при этом доступе в качестве венозного дренажа используют длинный тонкостенный катетер, который вводят через бедренную вену в правое предсердие. Часто, однако, при таком венозном дренаже приток оказывается недостаточным. В такой ситуации (иногда заранее, до начала искусственного кровообращения) через вторую бедренную вену вводят еще один, более короткий катетер, который располагают в илеофемораль-ной зоне. Еще один вариант дополнительного венозного дренажа состоит во введении длинного прямоугольного катетера в легочную артерию Предсерд-ный и легочный катетеры соединяются тройником с венозной магистралью.
Отметим, что при проведении обхода из левого предсердия в бедренную артерию тотальная гепаринизация не нужна. Время активированного свертывания при производительности до 2,0—2,4 л/мин м2 поддерживают на уровне 150—200 сек.
Заканчивая краткую характеристику перфузи-онных методов, применяемых при операциях на аорте, укажем, что эти операции сопровождаются наибольшей кровопотерей, наблюдаемой в сердечнососудистой хирургии. Это обстоятельство предопределило широкое применение селл-сейверов в хирургии аорты.
14.ВСПОМОГАТЕЛЬНОЕ КРОВООБРАЩЕНИЕ
История перфузионных методов вспомогательного кровообращения (ВК) тесно связана с развитием искусственного кровообращения, которое на сегодняшний день можно интерпретировать как механическое пособие, временно заменяющее функцию сердца и легких при выполнении кардиохирургического вмешательства в условиях «открытого» сердца. Если искусственное кровообращение условно можно отнести к методам анестезиологического плана (таким, как наркоз или релаксация, позволяющие хирургу выполнить операцию), то вспомогательное кровообращение вообще, - а в частности его перфузионные методы, - является реаниматологическим пособием, обеспечивающим совместно с сердцем минутный объем кровообращения, достаточный для питания тканей в условиях сердечной недостаточности (ОСН).
В зависимости от способа разгрузки сердца все виды ВК делятся на три группы:
- методы, основанные на снижении противодавления сердечному выбросу (методы контрапульсации);
- методы, основанные на уменьшении перекачиваемого сердцем объема крови (методы шунтирования);
- методы прямой помощи желудочкам (массаж сердца).
Помимо уменьшения потребности миокарда в кислороде, почти все они одновременно увеличивают его доставку в результате увеличения коронарного кровотока.
Методы шунтирования обладают большими возможностями разгрузки сердца, вплоть до полной замены функции одного или двух желудочков. Все они относятся к перфузионным методам и поэтому доступны учреждениям, использующим метод общего искусственного кровообращения.
Главной отличительной чертой методов шунтирования является возможность поддержки адекватного, необходимого по величине, минутного объема кровообращения (МОК) Все, что не в состоянии обеспечить ослабленное сердце, берет на себя аппарат вспомогательного кровообращения. Критериями эффективности шунтирующих методов ВК могут служить показатели общей гемодинамики и газообмена (суммарный МОК, системное артериальное давление, центральное венозное давление, напряжение кислорода в венозной крови, общее потребление кислорода, диурез и др.).
Подключение аппарата вспомогательного кровообращения (АВК) производят как к периферическим, так и к центральным сосудам (при вскрытии грудной клетки). А зависит это от конкретно сложившейся ситуации при возникновении ОСН. Ниже даны схемы подключения исполнительного устройства к пациенту, нуждающемуся в перфузионных методах ВК.
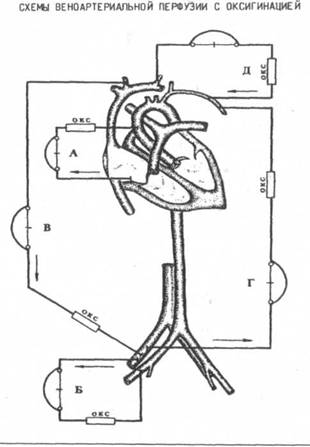
1. Веноартериальная перфузия с оксигенацией
а) правое предсердие - аорта,
б) бедренная вена - бедренная артерия,
в) яремная вена - бедренная артерия,
г) бедренная вена - подмышечная артерия,
д) яремная вена - подмышечная артерия.
2. Веноартериальная перфузия без оксигенации
а) бедренная вена - бедренная артерия,
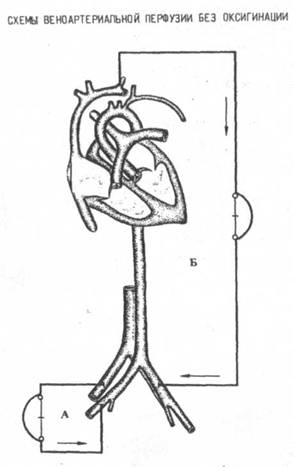 б) яремная вена - бедренная артерия.
б) яремная вена - бедренная артерия.
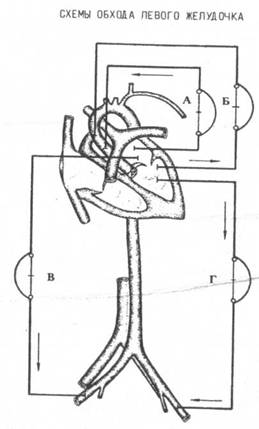
3. Обход левого желудочка
а) левое предсердие - аорта,
б) левый желудочек - аорта,
в) левое предсердие - бедренная артерия,
г) левый желудочек - бедренная артерия.
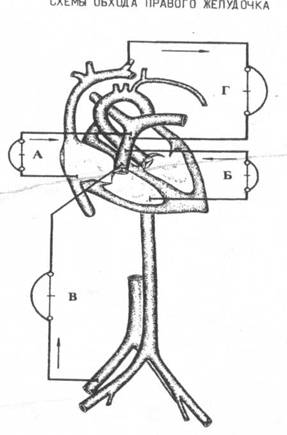
4. Обход правого желудочка
а) правое предсердие - легочная артерия,
б) правый желудочек - легочная артерия,
в) бедренная вена - легочная артерия,
г) яремная вена - легочная артерия.
|
5.Обход обоих желудочков
а) правое предсердие - легочная артерия, левое
предсердие - аорта,
б) правое предсердие - легочная артерия, левый
желудочек - аорта.
СХЕМЫ ОБХОДА ОБОИХ ЖЈЛУ1ОЧКОВ
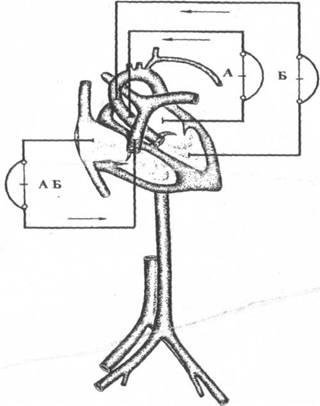
При присоединении к периферическим сосудам обычно канюлируют дистальный и проксимальный концы вены и артерии - с целью полного дренажа и кровообеспечения конечности.
В качестве исполнительных устройств могут быть использованы. 1. роликовый насос как наиболее доступный в кардиохирургических клиниках, 2. центрифужный насос, 3. различные модификации искусственных желудочков. Последние могут располагаться экстра - и интракорпорально (в. грудной или брюшной полости).
Главной особенностью роликовых и центробежных насосов является отсутствие пульсации кровотока, которую обеспечивают различные модификации искусственных желудочков. Справедливорти ради необходимо заметить, что современные роликовые насосы могут работать в пульсирующем режиме, о преимуществах и недостатках которого ведутся дискуссии и по сей день.
Вспомогательное кровообращение может вестись в синхронном и асинхронном с работой сердца пациента режимах. Предпочтительно синхронизировать работу пульсирующего исшэлйи?№чопэ устройства, эффективнее помогая ослабленному сердцу. Но, к сожалению, чаще не удается это сделать из-за развивающихся у пациентов с ОСН тахикардией или аритмией. Правда, когда речь идет о ситуации, при которой шунтируется весь или почти весь МОК, синхронизированная поддержка теряет свой смысл.
Основная задача-минимум перфузионных методов ВК - обеспечить суммарный с сердцем перфузионцый индекс для адекватного метаболизма в организме пациента.
Основная задача-максимум перфузионных методов ВК - способствовать восстановлению утраченной функции жизненно важных органов (сердца, легких, мозга, почек, печени и т. д.), т. е. выздоровлению пациентов, перенесших тяжелую ОСН, рефрактерную к медикаментозной терапии.
Опыт показывает, что выздоровление происходит в тех случаях, когда к моменту начала ВК еще не наступили необратимые изменения в жизненно важных органах человека.
Таким образом, особо важное значение приобретает правильный подход к показаниям для тех или иных видов ВК.
Специалист, имеющий в своем арсенале все вышеперечисленные перфузионные методы ВК и вспомогательного дыхания (ВД), должен правильно ориентироваться в возникшей ситуации, а после оперативной коррекции того или иного порока ввести соответствующую поправку и предложить данному больному оптимальную методику. Надо сказать, что иногда трудно принять верное решение даже при учете отработанных показаний вследствие изменений, привнесенных коррекцией порока. Чаще всего это бывает при врожденных пороках сердца, когда сердечно-сосудистая система адаптировалась к порочному кровообращению, а после радикальной коррекции порока норма приводит к фатальному исходу. Это касается, прежде всего, таких пороков, как тетрада или триада Фалло, когда малый круг недогружен кровотоком, а после коррекции через него должно проходить столько же крови, как и через большой.
Тут действует так называемый второй барьер, когда кровь устремляется по шунтам, не омывая альвеолы и не рксигенируясь. При этом растет общее легочное сопротивление, а правый желудочек испытывает большую постнагрузку, чем до коррекции. В связи с тем, что кровь в левые отделы сердца по коронарным артериям идет недооксигенированной, желудочки работают на «голодном пайке». Результат - относительная правожелудочковая недостаточность, которую, прежде всего, регистрируют в операционной - по сниженному артериальному и повышенному венозному давлению. Легочная й левожелудочковая недостаточность проходит «вторым планом» и часто не диагностируется.
Специалист, занимающийся вспомогательным кровообращением и дыханием, знает, что если имеется изолированная слабость левого желудочка, - показан обход левого желудочка, если имеется изолированная слабость правого желудочка, что встречается значительно реже, нужен обход правого желудочка, если возникает тотальная слабость сердца - необходим обход обоих желудочков (бивентрикулярный обход).
В ситуациях, когда помимо ОСН имеются явления острой дыхательной недостаточности (ОДН) или, как говорят, легочной недостаточности, необходим один из вариантов веноартериальной перфузии с оксигена-цией.
На сегодняшний день в большинстве учреждений вопрос о применении перфузионных методов ВК ставится только тогда, когда использованы все средства медикаментозной терапии, искусственной вентиляции легких и интрааортальная контрапульсация. При этом упущено время и не получен положительный эффект. Правомочность такой установки сомнительна, в связи со скромностью получаемых результатов.
Первопричиной такой ситуации называют позднее начало ВК по поддержанию адекватного МОК уже после наступления необратимых изменений органов и
тканей.
Веноартериальная перфузия с оксигенацией
Веноартериальная перфузия с оксигенацией - это процедура, сущность которой заключается в частичной замене функции сердца и легких. Когда же речь идет о замене функции сердца и легких в связи с их недостаточностью, то данный метод выступает в новой роли вспомогательного кровообращения и дыхания.
Логика веноартериальной перфузии с оксигенацией (ВАПО) при острой сердечной недостаточности, особенно при кардиогенном шоке, заключается в механической возможности удвоить или учетверить доставку оксигенированной крови к тканям и к органам, и разгрузить ослабленное сердце. Уменьшая объем каждой камеры сердца, ВАПО предотвращает чрезмерное напряжение стенки сердца (закон Лапласа), а, следовательно, уменьшает потребление кислорода миокардом.
Вторым положительным фактором ВАПО является возможность уменьшить (а в некоторых случаях и прекратить) введение катехоламинов, а, следовательно, снизить вероятность развития метаболических некрозов в миокарде и снизить летальность от ОСН в ближайшем постперфузионном периоде.
Общим показанием к осуществлению ВАПО является ОСН, не позволяющая прекратить искусственное кровообращение после коррекции порока, согревания больного и обычной медикаментозной терапии с применением небольших доз катехоламинов (допа-мин до 4 мкг/кг мин). Если пользоваться ординарными критериями гемодинамики, то ВАПО следует считать показанной, когда при венозном давлении 10-14 мм рт. ст. среднее артериальное давление не поднимается выше 60 мм рт. ст., а на ЭКГ наблюдаются признаки ишемии миокарда.
При измерении сердечного выброса и давления в левом предсердии крайними проявлениями острой левожелудочковой недостаточности являются: сердечный индекс (СИ) менее 2 л/мин м2 и среднее давление в левом предсердии выше 25 мм рт. ст
При правожелудочковой недостаточности: СИ < 2 л/мин м2, ЦВД выше 15 мм рт. ст.
После установления факта острой сердечной недостаточности не следует использовать весь арсенал медикаментов с целью увеличить инотропизм миокарда, а продолжать искусственное кровообращение во вспомогательном режиме. То есть с помощью аппарата искусственного кровообращения осуществлять разгрузку сердца настолько, чтобы не перегружать его объемом перекачиваемой крови.
Мы исходим из концепции, что сердце должно осуществлять работу в пределах своих возможностей, которые мы определяем по косвенным признакам: отсутствию ишемии миокарда на ЭКГ, среднему артериальному давлению выше 60 мм рт. ст., давлению в левом предсердии ниже 15 мм рт. ст., суммарному перфузионному индексу выше 2 л/мин м2 при гема-токрите около 30%. Так как последний при управляемой гемодиллюции к моменту окончания перфузии редко достигает 30%, то необходимо внести поправку в объемную скорость, получив анализ содержания кислорода в венозной крови. Напряжение кислорода в венозной смешанной крови при нормотермии не должно быть ниже 36 мм рт. ст.
Когда будут достигнуты нормальных показателей перечисленные критерии, станет ясно, сколько крови может перекачивать сердце больного без применения инотропных средств, то есть без стимуляции а - и р-рецепторов. Это позволит оценить возможность сердца выполнять работу самостоятельно. Как правило, на выяснение причин и степени острой сердечной недостаточности уходит до 20-30 минут. За это время, если коррекция порока адекватна, и не нарушены проводящие пути сердца, если не наступили необратимые изменения в миокарде и не развился инфаркт миокарда вследствие неадекватной кардиоплегии или травмы коронарных артерий, если не произошло тромбоэмболии' в сосудистое русло сердца, если ликвидирована гиповолемия, то, как правило, удается справиться с острой сердечной недостаточностью и прекратить вспомогательное кровообращение. В таких случаях за эти 20-30 минут удается «отмыл»» сердце от кардиоплегического раствора и метаболитов или «прогнать» воздух из коронарных сосудов, устранить мозаичность в кровоснабжении всех слоев, миокарда, то есть подготовить сердце к нормальным нагрузкам. Наш опыт показал, что чаще всего этим больным в ближайшем постперфузионном периоде не требуется введение инотропных препаратов.
Если же при попытке прекратить искусственное кровообращение острая сердечная недостаточность выражена настолько, что требуется почти полная замена сердца как насоса и объемная скорость ВК равна или почти равна объемной скорости ИК, то совершенно очевидна более серьезная причина, в которой необходимо тут же разобраться, не затушевывая картину введением больших доз катехоламинов, в частности допамина свыше 10 мкг/кг мин.
В такой ситуации появляется необходимость обсудить прогноз для жизни больного, и определить показания для применения длительных видов вспомогательного кровообращения или же в организме больного произошли необратимые изменения.
Было отмечено, что если после искусственного кровообращения концентрация лактатов превышает 6 ммоль/л, то в 90-100% случаев наступает смерть.
Обход левого желудочка.
Обход левого желудочка (ОЛЖ) - перфузионный метод вспомогательного кровообращения (ВК), заключающийся в шунтировании (перекачивании) части или всего минутного объема сердца из левого предсердия или желудочка в аорту или бедренную артерию с помощью того или иного насоса.
На сегодняшний день наиболее эффективным и чаще других используемым способом механической поддержки ослабленного левого желудочка у кардио-хирургических больных является обход, или шунтирование левого желудочка. Методы шунтирования желудочков обладают большими возможностями разгрузки сердца вплоть до полной замены одного или обоих желудочков.
Основная цель ОЛЖ - работая вместо или одновременно @ левым желудочком сердца; поддерживать в организме объемный суммарный кровоток, достаточный для нормального питания тканей. При этом на долю самого ослабленного левого желудочка должна приходится работа, которую он способен выполнять в оптимальном для данного состояния режиме (без перегрузки)
Показания к ОЛЖ. Обход левого желудочка применяют в случае изолированной его слабости. При сочетанной слабости обоих желудочков необходимо применять обход обоих желудочков.
Общим показанием для ОЛЖ, как для любого пер-фузионного метода ВК, является невозможность отключить больного от АИК во время операции на открытом сердце, т. е. перевести больного на самостоятельное кровообращение: ОЛЖ показан при невозможности уменьшить объемную скорость перфузии АИК ниже 30% от расчетной.
Критериями опасной для жизни депрессии левого желудочка при попытке отключить аппарат искусственного кровообращения являются:
- повышение среднего давления в левом предсердии выше 25 мм рт. ст.,
- сердечный индекс меньше 2 л/мин м2,
- снижение среднего артериального давления меньше 60 мм рт ст.,
- быстрое нарастание медленной активности на ЭЭГ
- появление признаков ишемии миокарда и нарушение ритма на ЭКГ,
- видная на глаз слабость сокращений левого желудочка и его перерастяжение.
- появление признаков ишемии миокарда и нарушение ритма на ЭКГ,
- видная на глаз слабость сокращений левого желудочка и его перерастяжение.
В такой ситуации необходимо тут же начинать ОЛЖ через дренаж левого желудочка, как показано на рисунке, а, следовательно, не удалять дренаж да попытки прекратить искусственное кровообращение и убедиться, что'нет острой сердечной недостаточности.
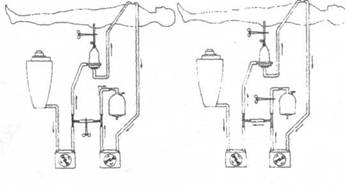
Во время обхода левого желудочка необходимо попытаться найти причину слабости левого желудочка и устранить ее. Если для этого понадобится искусст-. венное кровообращение, то начать его.
В ситуации, когда ясно, что причина сердечной слабости неустранима или не найдена, и комплексное лечение с применением медикаментозных средств (допамин до 10мкг/кг мин) не дает эффекта, надо переходить на длительный обход левого желудочка как эффективный метод частично или полностью заменить слабый левый желудочек.
Техника ОЛЖ. Подключение насоса к больному можно проводить через тройники. артериальной магистрали АИК и дренаж левого желудочка, с помощью которого осуществляется временный его обход или через специальную одноразовую систему, отдельно приготовленную для этой процедуры. В последние годы для ОЛЖ мы используем систему с центрифужным насосом, которую собирает операционная сестра из одноразовых компонентов (трубки, головка центрифужного насоса, флоу-коннектор, коннектор для измерения перфузионного давления). Затем операционная сестра отдает всю систему пер-фузиологу за исключением приводящей и отводящей петли, и начинает заполнять физиологическим раствором с гепарином (в соотношении 1000:1).
Перфузиолог устанавливает головку в центрифужный насос, накладывает зажим на отводящую магистраль системы и выставляет ноль на флоуметре. После подсоединения камеры давления к датчику давления устанавливается электрический ноль по каналу давления
После удаления пузырьков воздуха из экстракорпоральной системы для ОЛЖ включают центрифужный насос и, не снимая зажима с отводящей петли, доводят количество оборотов в минуту до в минуту и только затем снимают зажим. В это время на флоуметре появляются цифры производительности насоса. Затем перфузиолог ручкой производительности насоса выставляет, заданную скорость перфузию, равную объемной скорости аппарата для общей перфузии на этапе, предшествовавшем включению насоса. Увеличивая или уменьшая частоту вращения ротора. Одновременно с этим производительность аппарата для общей перфузии также плавно
снижают до 0; Далее производительность насоса регулируют таким образом, чтобы давление в левом предсердии было не выше 15 мм рт. ст., а среднее артериальное давление выше 60 мм рт. ст. Аппарат для общей перфузии не отключают от больного до тех пор, пока не ликвидируют гиповолемию и не произведут тщательный гемостаз
Затем предпринимают частичную нейтрализацию гепарина протаминсульфатом (примерно 1 мг/кг), снижая время активированного свертывания до 110-140 с. На этом уровне ВАС поддерживают, проверяя его каждый час и добавляя гепарин в малых дозах (3-10 ед. кг/час внутривенно). Закрывают грудную клетку так, чтобы магистрали ОЛЖ нигде не перегибались и не пережимались.
При стабильных гемодинамических показателях больного перекладывают на носилки аппарата вспомогательного кровообращения и транспортируют в специальное отделение кардиологической реанимации с непрекращающимся шунтированием крови, во избежание свертывания ее в экстракорпоральной системе.
В отделении реанимации, если это не было сделано в операционной, необходимо ввести в правые отделы сердца до бифуркации легочной артерии катетер Swan-Ganz с целью определения минутного объема кровообращения (МОК) методом термодилюции и давления в легочной артерии.
Проводить ОЛЖ следует таким образом, чтобы суммарный МОК был не менее 2,5 л мин/м2, а среднее давление в левом предсердии не превышало 15 мм рт. ст. При этом необходимо помнить, что - при функциональной полноценности правого желудочка это может быть достигнуто только при достаточном объеме циркулирующей крови в организме, критерием чего может служить ЦВД на уровне 10-12 мм рт. ст.
Поддержание оптимального объема циркулирующей крови (ОЦК) достигают внутривенным введением крови, ее компонентов (эритроциты, плазма) или плазмозамещающих жидкостей, руководствуясь данными измерения гематокрита, состава плазмы, а • также величиной диуреза.
Определение суммарного МОК дает возможность вычислить процент участия в нем левого желудочка (ЛЖ) по формуле:
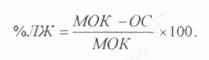
где ОС - объемная скорость насоса.
По мере увеличения % ЛЖ следует медленно уменьшать ОС до 500 мил/мин. ВАС необходимо увеличить до 200-250с. По достижении доли участия ЛЖ, равной 90% и более, при сохранении сердечного индекса на уровне не менее 2,5 л/мин м2 и при удовлетворительных цифрах давления в левом предсердии и в артерии ОЛЖ может быть прекращен.
Главными критериями адекватности ОЛЖ считаются показатели метаболизма (напряжение кислорода в венозной крови, концентрация лактата и ионов плазмы, артериовенозная разница по кислороду).
Деканюляцию левого предсердия, аорты или бедренной артерии производят хирурги оперативным путем (рестернотомия).
Наш экспериментальный и клинический опыт лечения острой сердечной недостаточности подтверждает данные литературы о гемодинамической эффективности шунтирования левого желудочка. Показатели метаболизма свидетельствуют об адекватном ответе организма пациента, находящегося на ОЛЖ. .
Экстракорпоральная мембранная оксигенация (ЭКМО)
Проблема лечения острой дыхательной недостаточности до сих пор остается одной из самых сложных, что заставляет искать новые методы борьбы с этим осложнением. До недавнего времени искусственная вентиляция легких оставалась последним достижением медицины в лечении дыхательной недостаточности, когда весь комплекс терапевтических мероприятий оказывался неэффективным.
Сегодня можно использовать новые достижения исследователей, занимающихся искусственным кровообращением и разработкой новой аппаратуры для вспомогательного кровообращения. Создание мембранного легкого позволило осуществлять газообмен в течение нескольких дней и даже недель, т. е. появилась возможность помочь больным, которым грозит Смерть от острой дыхательной недостаточности. Каждый метод лечения имеет пределы своего воздействия, и судить о его эффективности можно только по приобретении достаточного опыта его применения.
Впервые метод экстракорпоральной мембранной оксигенации был применен у больного с дыхательной недостаточностью J. A. Helmsworth в 1952 году. Однако до создания современных мембранных оксигенаторов он не мог получить широкого распространения. Так же, как и новые методы вспомогательного кровообращения, мембранную оксигенацию применяли у умирающих больных, поэтому успех терапии был незначительным.
Непрерывное совершенствование оксигенаторов заставляет по-новому оценить роль ЭКМО в лечении больных с острой дыхательной недостаточностью. Накапливающийся опыт убеждает в необходимости начинать ЭКМО до развития необратимых процессов в органах и тканях, обязательно учитывая при этом степень эффективности обычных терапевтических мероприятий.
Так как с помощью искусственной вентиляции легких обычно удается корригировать дыхательный ацидоз, применение экстракорпоральной мембранной оксигенации показано, главным образом, при резко выраженной гипоксемии.
Больным с такими видами острой дыхательной недостаточности показана ЭКМО, когда, несмотря на вдыхание смеси, содержащей более 50% кислорода, напряжение кислорода в артериальной крови не поднимается выше 50 мм рт. ст. При гипоксемии такой степени (в условиях нормальной работы сердца) ве-ноартериальное шунтирование составляет более 2 /3 общего объема легочного кровотока. Дальнейшее повышение инспираторной фракции кислорода существенно не влияет на величину напряжения кислорода в артериальной крови, но возрастает риск токсического действия кислорода и дальнейшего поражения легких.
Одним из действенных способов снизить внут-рилегочное шунтирование является применение постоянной искусственной вентиляции легких с положительным давлением в конце выдоха, которая позволяет повысить напряжение кислорода в артериальной крови. В тех случаях, когда, несмотря на большую концентрацию кислорода в дыхательной смеси, гипоксемия сохраняется, нужно, прежде всего, применить положительное давление в конце выдоха. До тех пор, пока напряжение кислорода в артериальной крови (РаОг) не превышает 50 мм рт. ст., величину положительного давления в конце выдоха (ПДКВ) можно поддерживать в пределах 5-20 см вод. ст.
Нарастание гипоксемии, несмотря на применение ИВЛ с ПДКВ 100% кислородом в течение длительного времени, а также клинические признаки ухудшения состояния больного, служат показаниями для экстракорпоральной мембранной оксигенации.
Показания к применению ЭКМО разработали W. M. Zapol и соавторы, которые считают, что если у больного определена прогрессирующая гипоксемия (РаО2 ниже 50 мм рт. ст. при 100% вдыхании кислорода и ПДКВ - 10 см вод. ст.) в течение 6-12 часов, а также уменьшена растяжимость легких до значений менее 15 мл/см вод. ст, увеличена доза кардиотони-ческих препаратов, необходимых для поддержания адекватного сердечного выброса, появились опасные для жизни нарушения ритма сердца и отсутствуют противопоказания к ЭКМО, необходимо осуществлять экстракорпоральный газообмен с применением мембранного оксигенатора.
К противопоказаниям ЭКМО авторы относят: 1) геморрагию, 2) распространенный опухолевый про
цесс, 3) пожилой возраст больного, 4) хроническую или заведомо необратимую легочную недостаточность, 5) резкие неврологические нарушения, б) сепсис, 7) ожоги более 50% поверхности тела. Почечная недостаточность, по их мнению, не является противопоказанием к экстракорпоральной мембранной ок-сигенации.
После массивных травм ЭКМО может быть применена, если прошло 12-24 часа с момента прекращения кровотечения. Увеличенное сопротивление легочных сосудов свидетельствует об интенсивной их облитерации и служит плохим прогностическим признаком
Экстракорпоральная мембранная оксигенация, однако, не является лечением самого патологического процесса, приведшего к острой дыхательной недостаточности. Это лишь симптоматическая терапия, дающая возможность выиграть время, в течение которого газообменная функция легких может быть восстановлена, Главным условием успеха данного лечения является обратимость патологических процессов в легких. К сожалению, мы еще не знаем, какие из них обратимы. Несомненно, однако, что уменьшение действия таких повреждающих факторов, как высокая концентрация кислорода и повышенное давление в дыхательных путях, при экстракорпоральной мембранной оксигенации должно способствовать обратному развитию патологических процессов.
Перфузионные схемы Э)КМО На сегодняшний день существует много схем подключения экстракорпорального контура к периферическим сосудам пациента для лечения острой
дыхательной недостаточности. Мы будем говорить о наиболее употребляемых, а, следовательно о наиболее эффективных схемах экстракорпоральной мембранной оксигенации.
Артериовенозная (АВ) схема, при которой кровь продвигается по экстракорпоральной и венозной системе за счет сердечных сокращений (варианты Б, В) Недостатки ее те же, что и при любом артерио-венозном шунте: снижение периферического кровообращения и перегрузка левого сердца. Дяя компенсации этих нарушений необходима повышенная работа сердца, которую не всегда переносят больные, особенно находящиеся в тяжелом состоянии.
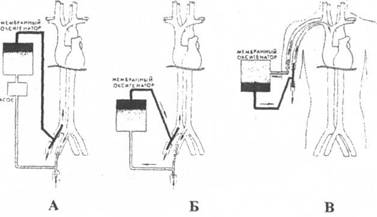
Варианты подключения ЭКМО по артериовенозной схеме
А - артериовенозная схема с насосом (бедренная артерия-бедренная вена)
Б - артериовенозная схема без насоса
(бедренная артерия-бедренная вена)
В - артериовенозная схема без насоса (лучевая артерия - лучевая вена)
У большинства современных оксигенаторов большое перфузионное сопротивление, что требует включения в контур одного или двух насосов (вариант А).
Недостатки артериовенозной схемы ЭКМО:
1) требуется увеличенный сердечный выброс,
2) чаще всего при наличии легочной гипертензии и правожелудочковой недостаточности;
3) во время байпасса в оксигенатор поступает артерилизованная кровь, что снижает его коэффициент полезного действия;
4) при увеличении сердечного выброса во время артериовенозного байпасса может снизиться коэффициент вентиляция /кровоток или увеличится сброс справа налево, что, в свою очередь, приведет к снижению насыщения кислородом артериальной крови.
Достоинства артериовенозной схемы ЭКМО:
1. простота и безопасность безнасосной перфузии; с хорошими канюлями и простой антикоагуляцией, методика может быть использована в домашних условиях при задержке элиминации углекислоты с помощью простого диализатора;
2. минимальная травма крови;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |