Метод Шелла. Метод заключается в том, что легкие фракции нефти (в основном газойль) переводят в газообразные олефины. Фракция газойля в трубчатой печи доводят до полного испарения при нагреве до 400 0С. Пары направляют в колонну, в которой конденсируется фракция, использованная в качестве топлива. Остальные фракции колонны проходят через два трубчатых нагревателя, где температуру доводят до 600-700 0С. Температурный предел устанавливают в зависимости от того какого состава олефины стремятся получить. В трубчатую печь подают перегретый водяной пар который препятствует образованию кокса и, снижая парциальное давление, препятствуют протеканию побочных реакций олефинов особенно полимеризации. Чтобы избежать дальнейших превращений и потерь олефинов, газы немедленно после выхода из печи охлаждают впрыскиванием масла.
Реакционный продукт поступает во фракционирующую колонну, в которой его разделяют на газ, дистиллят и топливное масло. Газообразную часть направляют на разделение и после переработки получают чистый этилен и остальные олефины. Преимуществом этого метода является то, что помимо получения олефинов в качестве побочного продукта и жидкой фракции получают высокооктановый бензин.
Парофазный пиролиз по Келлагу. Пиролиз проводят в присутствии перегретого водяного пара, который служит передатчиком тепла. Принцип установки для пиролиза следующий. Лигроин, бензин или газойль нагревают в трубчатых печах в присутствии водяного пара до 590-600 0С. Уже при этом происходит частичное крекирование, выходящий из печи газ смешивают с водяным паром, доведенным до 530 0С, и короткое время выдерживают в адиабатическом реакторе. Определением соотношения между количеством перегретого пара и количества углеводородных паров определяют глубину крекинга. После пиролиза газы немедленно охлаждают до 200-300 0С. При применении этого метода внутри пиролизной печи можно поддерживать высокую температуру без опасения вызвать коксообразование, а низкое парциальное давление способствует высокому содержанию олефиновых углеводородов в отдельных фракциях. Длительность пребывания газа в зоне нагрева равна одной секунде. Газы с температурой 200 0С поступают во фракционирующую башню, в которой образуется конденсат, а водяной пар, легкие углеводороды и газ отводят через верхнюю часть колоны. Газ поступает в компрессорную установку на доработку.
В результате пиролиза максимальный выход этилена из лигроина составляет 32% вес., а из газойля 26% вес. Меняя условия крекинга можно получать пропен или другие олефины. Интересно отметить, что ф. С4 содержащий лишь 5% бутана, в зависимости от условий крекирования можно получить 20-50% бутадиена.
Метод непрерывного пиролиза сырых нефтей и нефтяных остатков. Непрерывный пиролиз служит для производства олефинов, поэтому стремятся к возможно полному превращению исходного материала в газообразные продукты реакции. При этом образуется кокс, который оседает на находящихся в трубчатом нагревателе и непрерывно движущихся накаленных шариков диаметром 5-12 мм. Эти шарики поставляют нужное для эндотермического процесса тепло. Их нагревают при помощи внешнего обогрева при 650-759 0С, и опрыскивают предварительным сырьем. Горячее масло (нефть и другие) попадает в зону смешения на коксовые шарики, в результате наступившей реакции газы пиролиза выходят из печи, а кокс полностью оседает на шарики.
Газы быстро охлаждают при помощи тяжелого масла и подают на разделение во фракционирующую колонну, где они разделяются на газ, бензин, фракцию газойля и остаток который служит легким топливом. Газ отправляют на разделение. Коксовые шарики регенерируют в коксоотделителе, очищают от пыли на ситах и подают обратно в трубчатку. Трубчатка (коксонагреватель) из хромомолибденовой стали, омывается топливными газами, вследствие чего удается избегать перегрева.
Каталитическая дегидратация спиртов. Легкость дегидратации спиртов зависит от их строения. Легче всего дегидратируются третичные спирты, вторичные занимают промежуточное положение, а первичные спирты наиболее прочны. В определенных условиях дегидратацию можно проводить простым нагреванием в присутствии водоотнимающих веществ, например, конц. Н2SO4. Исключительно легко дегидратируется третичный бутанол – изобутанол, образуя очень чистый изобутелен.
При дегидратации спиртов до олефинов в производственных условиях пропускают пары спирта над дегидратирующими катализаторами. Особенно активными катализаторами является окись алюминия и кремниевая кислота, или их смеси. При Т=350-400 0С реакция обычно протекает очень гладко.
Дегидратацию спиртов можно проводить и под давлением. Этот процесс имеет то преимущество, что при этом можно простым охлаждением водой превращать выделяющийся газообразный изобутилен в жидкость.
Рассмотрим процесс получения изобутилена из соответствующего спирта. Пары изобутанола пропускают при Т=360-380 0С над активированной окисью алюминия, помещенной в трубы, обогреваемые электричеством в количестве из расчета 1-1,5 кг спирта на 1 л катализатора. Давление составляет примерно 4 атм. выходящий изобутилен охлаждают и отделяют в отстойнике от воды. Затрата катализатора на 1 кг полученного изобутилена составляет примерно 1,2 кг окиси алюминия. Его не генерируют. Полученный изобутилен достаточно чист для дальнейшей переработки. Для полимеризации изобутилена, его очищают повторно простой дистилляцией под давлением.
1.1.2. Химические свойства олефинов.
1. Гидрирование
В определенных условиях проводят термическое или фотохимическое гидрирование олефинов с хорошей скоростью по радикальному механизму. Однако такой свободно-радикальный механизм оказывается энергетически невыгодным. В то же время, олефины быстро реагируют с водородом при низких температуре и давлении в присутствии ряда металлов, таких как никель, платина и палладий. При этом достигается полное превращение. Для достижения максимума каталитического действия металл обычно приготавливают в высокодисперсном состоянии. Реакция гидрирования экзотермична.
2. Электрофильное присоединение к олефинам
2.1. Гидратация
Процесс сернокислой гидратации делится на 4 стадии:
а) абсорбция олефина серной кислотой с образованием алкилсульфата:
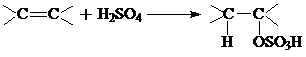
б) гидролиз алкилсульфата на спирт и серную кислоту:
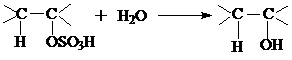
в) отделение спирта от серной кислоты и его очистка;
г) регенерация серной кислоты
На практике первую стадию проводят при Т=80 0С 97-98%-ой серной кислотой. Вторая стадия проводится под давлением не ниже 7 атм.
Другим промышленным способом гидратации является прямая реакция взаимодействия олефинов и воды в присутствии фосфорно-кислого катализатора (фосфорная кислота на диатомите):
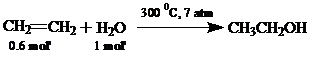
Третий способ синтеза, это получение спиртов в присутствии разбавленной серной кислоты или фосфорной кислоты в качестве катализатора:
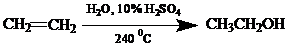
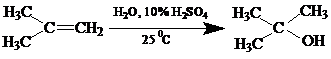
Этот метод широко используется в промышленности для получения этилового спирта и изобутилового спирта
Следует отметить, что при гидратации олефинов образуются вторичные спирты, за исключением этилена.
2.2. Присоединение галоидводородов
Легче всего присоединяется к олефинам йодистый водород; наиболее медленно реагирует НСl. О тех случаях, когда галоидводород присоединяется медленно, рекомендуется использовать в качестве катализатора ВН3. Лучше всего присоединение галоидводородов к олефинам проводить в жидкой фазе. Например, С2Н4 при 150 0С под давлением реагирует с водным раствором бромистого водорода, а в присутствии ВiBr3 реакция протекает быстро уже при 20 0С и атмосферном давлении. В качестве растворителя процесса гидрогалогенирования можно использовать ледяную уксусную кислоту, гексан и т. д., причем в различных растворителях скорость реакции не является одинаковой, поэтому для каждого случая необходим подбор подходящего растворителя.
Газообразные олефины и НСl реагируют чрезвычайно медленно, но реакция сильно ускоряется в присутствии безводного АlCl3.
Легче всего галоидводороды реагируют с третичными олефинами даже при низких температурах. Так, галогенводороды присоединяются к изобутилену в жидкой фазе при 0 0С практически мгновенно, и даже при – 78 0С скорость процесса ещё довольно велика.
Присоединение галоидводородов к несимметричным олефинам происходит обычно по правилу Марковникова; если реакция протекает по полярному механизму:
![]()
При действии света, перекисей, свободнорадикальных инициаторов на олефины в присутствии ловушек свободных радикалов осуществляется быстрая цепная реакция присоединения, протекающая против правила Марковникова:
![]()
Если такая реакция инициируется перекисями, то добавление антиокислителей (дифениламин) в реакционную смесь приводит к тому, что присоединение галогенводорода снова начинает проходить по правилу Марковникова. Аномальное присоединение по свободнорадикальному механизму наблюдается только для НСl и НВr, а присоединение НF и HI всегда проводят по правилу Марковникова.
2.3. Присоединение галогенов
Присоединение галогенов может происходить по 2-м механизмам: по молекулярному и цепному
молекулярный:
![]()
цепной:
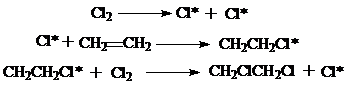
Олефины присоединят бром быстро и количественно, если, например, его раствор в ССl4 или уксусной кислоте добавлять к раствору олефина в том же растворителе. Эта реакция является качественной на олефины. Кислород воздуха не оказывает существенного влияния на присоединение галогенов к олефинам. В технике хлорирование этилена осуществляют пропусканием этилена и хлора в дихлорэтане при Т=20-25 0С с непрерывным выводом образовавшегося продукта из зоны реакции.
2.4. Получение хлоргидринов
Одновременное воздействие хлора и воды на олефины является очень важной реакцией для промышленности органического синтеза. Она приводит к получению хлорированных спиртов путем присоединения к олефину хлорноватистой кислоты, образующийся в ходе процесса из воды и хлора (реакция Кариуса):
![]() (этиленхлоргидрин)
(этиленхлоргидрин)
Хлоргидрины отличаются особой реакционноспособностью вследствие соседнего расположения хлора и гидроксильной группы. Так, например, при действии щелочи на этиленхлоргидрин
![]()
образуется циклический эфир – окись этилена, который весьма неустойчив и может легко раскрываться с присоединением разнообразных органических соединений. Такие циклические эфиры называются эпоксисоединениями. Этиленхлоргидрин также легко образуется с хорошим выходом при одновременном пропускании хлора и этилена в воду (реакция Гомберта). Выход 86-88%. Наряду с этиленхлоргидрином при этом, в результате побочной реакции хлорирования олефина, образуется 8-9% дихлорэтана. Распространение этого метода на олефины с большим чмслом атомов углерода ведет к увеличению доли побочных продуктов прямого хлорирования олефинов.
2.5. Присоединение сероводорода и меркаптанов
Сероводород и меркаптаны легко присоединяются к олефинам в присутствии перекисей, например, перекиси бензоила. При этом сероводород присоединяется по правилу Марковникова, а меркаптаны против этого правила:
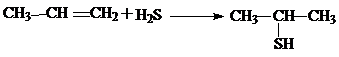
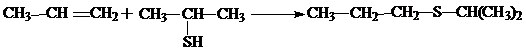
В качестве катализаторов можно использовать хлориды металлов.
Сероводород присоединяется к олефинам также под действием облучения ультрафиолетовым светом, причем газообразный Н2S при этом реагирует с олефинами очень медленно, а при проведении реакции в жидкой фазе присоединение происходит достаточно быстро.
Третичные олефины присоединяют Н2S в присутствии твердых или жидких катализаторов, например безводного НF или комплексного соединения BF3 с H3PO4.
2.6. Присоединение аммиака к олефинам
Если при 600 0С и малом времени контакта пропускать смесь аммиака и олефина над катализаторами из окиси алюминия с добавками окиси ванадия, молибдена или вольфрама, образуются нитрилы:
![]()
Однако в результате деструкции углеродного скелета для олефинов с большим количеством атомов углерода получаются низкие нитрилы и среди них преимущественно ацетонитрил. Увеличение отношения аммиака к углеводороду благоприятствует образованию ацетонитрилов и подавляет побочные реакции.
2.7. Присоединение карбоновых кислот к олефинам
Карбоновые кислоты присоединятся к олефинам с образованием соответствующих сложных эфиров:
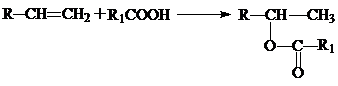
Из этилена, таким образом, получают этилацетат из пропилена и н-бутиленов – втор-пропилацетат и втор-бутилацетат. В качестве катализатора реакции наилучшие результаты получаются при использовании смеси ВH3 и HJ. Можно использовать в качестве катализатора и Н2SO4, но выходы при этом невысоки.
2.8. Присоединение спиртов
Спирты присоединяются к олефинам под действием света или в присутствии перекисей так, что в результате реакции образуются третичные спирты:
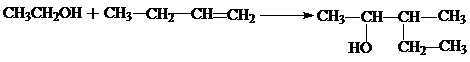
При этом водород, соединенный с атомом углерода карбонильной группы, замещается на алкильную группу.
2.9 Окисление олефинов
1. олефины при низких температурах реагируют с озоном; при этом разрывается двойная связь, и образуются циклические перекисные производные:
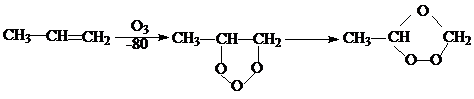
На первой стадии происходит цис-циклоприсоединение с образованием мольозонида – неустойчивого соединения, который быстро переходит в более устойчивый озонид. Озониды вследствие содержания связи (перекисной) –О-О - могут взрываться с большой силой и совершенно неожиданно.
Озониды обычно не выделяют в чистом виде, а разлагают, гидролизуя водой и восстанавливая цинком; при этом образуются карбонильные соединения, которые легко удается выделить и идентифицировать:
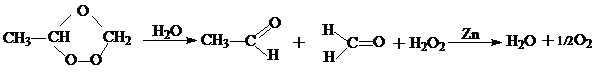
2. При окислении олефинов в мягких условиях КМnO4 или четырехокисью осмия происходит расщепление двойной связи с образованием гликолей. Оба эти вещества реагируют подобно озону по механизму циклоприсоединения:
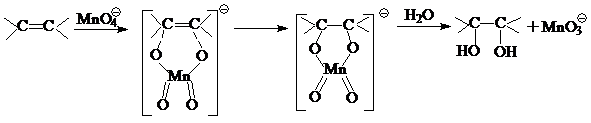
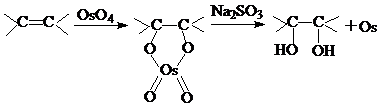
Образующиеся гликоли имеют цис-структуру.
При окислении олефинов в более жестких условиях раствором КМnO4 происходит расщепление двойной связи с образованием карбоновых кислот.
Окисление олефинов действием перекиси водорода в муравьиной кислоте приводит к образованию гликолей транс-формы:
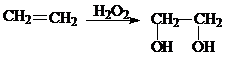
2.10 Гидроформилирование олефинов – оксосинтез (реакция Рёллена)
Совместное действие СО и Н2 на олефины в присутствии карбоната кобальта, металлического кобальта или его солей (олеаты, нафтенаты) приводит к образованию альдегидов, а в особых случаях и кетонов, т. е. соединений, содержащих оксогруппу. Реакция была открыта Отто Рёлленом в 1938г.
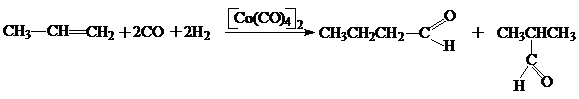
2.11 Получение карбоновых кислот по рекции Реппе
Нагревание олефинов с окисью углерода под давлением 150-200 атм до 200-300 0С в присутствии воды и карбонила никеля приводит к образованию карбоных кислот:
![]()
Если реакцию проводить в присутствии спиртов, аминов или аммиака, то образуются соответственно сложные эфиры, замещенные амиды или амиды кислот.
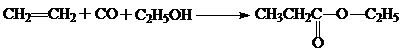
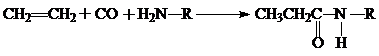
2.12 Реакции алкилирования
а) олефины вступают в реакцию с парафинами при высокой температуре (500 0С) и давлении порядка 300 атм или при комнатной температуре в присутствии катализаторов, таких как AlCl3 или HI (безводные); конц. H2SO4:
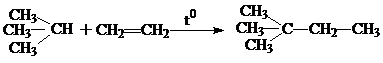 (неогексан)
(неогексан)
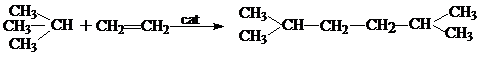
При термическом алкилировании образуются главным образом продукты, которые можно предусмотреть в соответствии с реакцией и которые соответствуют по строению исходным углеводородам.
В противоположность этому при каталитическом алкилировании парафинов получаются изомеризованные продукты.
В реакции термического алкилирования легче всего вступают этилен, а затем в порядке понижения активности пропен, н-бутен и изобутилен; при каталитическом алкилировании порядок обратный.
Как при термическом, так и каталитическом алкилировании парафинов олефинами, во избегания протекания побочных реакций полимеризации берут большой избыток первых; при этом реакции полимеризации полностью подавляются.
Алкилирование парафинов олефинами можно проводить термически в присутствии гомогенных катализаторов. При этом температуру можно снизить до 400 0С. Примечательно то, что при таком способе алкилирования продукты реакции по своему строению ничем не отличаются от тех, которые получают при обычном термическом алкилировании. В качестве катализаторов при этом пригодны главным образом органические хлорпроизводные, такие как СНСl3, трихлорпропан, дихлордифторметан (фреон-12).
б) олефины способны алкилировать также ароматические соединения в присутствии катализатора безводного AlCl3; например бензол, тиофен и т. д.:
![]()
Алкилирование бензола проводится при атмосферном давлении, без механического перемешивания. AlCl3, применяемый как катализатор должен иметь 98%-ную степень чистоты.
1.1.3. Получение сопряженных диенов
Диены-1,3 являются наиболее важными в практическом отношении мономерами и широко используются в промышленности синтетического каучука. Наиболее хорошо изучены из сопряженных диенов бутадиен-1,3, хлоропрен и 2-метил-бутадин-1,3 (изопрен), которые полимеризуются и сополимеризуются со многими другими мономерами в различных условиях, образуя ряд промышленно важных эластомеров.
Получение бутадиена-1,3
1. Метод дегидрирования бутана по Гудри
Дегидрирование бутана проводят в реакторе, облецованном керамическим материалом при давлении 0,7 атм, средней температуре процесса 553 0С при продолжительности процесса 8-10 мин. Этот метод характеризуется особым способом подвода тепла для эндотермического процесса. Это тепло выделяет сам катализатор. Поскольку теплоемкость катализатора невелика, то источником тепла служит также и материал с большим удельным весом и с большей теплоёмкостью, расположенной между шариками катализатора. Материал этот не обладает каталитическим действием; он поглощает тепло, освободившееся при регенерации катализатора, которую проводят каждые 7-15 мин. обычным, неразбавленным воздухом. В производственных условиях при регенерации катализатора освобождается обычно меньше тепла, чем это необходимо для дегидрирования. Эту небольшую разницу можно легко восполнить, повысив температуру бутана или усилив подогрев воздуха, идущего на регенерацию. За счет тепла, поглощенного во время регенерации катализатором вместе с материалом, которое регулируют так, чтобы оно соответствовало количеству тепла, необходимому для последующего дегидрирования бутана и происходит реакция.
Процесс Гудри выгодно отличается тем, что при его применении можно обходиться без трубчатых печей, в которых процесс коксования, происходящий на катализаторе и загрязняющий его, ярко выражен. В отличии от трубчатых в керамических печах коксования не происходит.
Выход бутадиена при однократном прохождении через печь в вес.% составляет 2%, н-бутенов – 32,0%, н-бутана – 52,6%, а конечный выход бутадиена при повышенной степени превращения н-бутана за один проход составляет уже 4,3%, н-бутенов – 68,2, н-бутана – 0%. Хотя выход бутадиена по этому методу невысок, он является единственным производственным методом получения его в одну стадию без стадии выделения бутена.
2. Метод дегидрирования с водяным паром Нью-Бнерси
Этот метод дегидрирования также характеризуется особым способом подвода тепла, который в этом случае осуществляют при помощи водяного пара. Применяемый для дегидрирования н-бутана в бутадиен должен быть устойчивым по отношению к водяному пару. Этим требованиям удовлетворяет катализатор N 1707 (США), имеющий состав (в %): MgO - 72.4; Fe2O3 – 18.4; CuO – 4.6; K2О – 4,6. Соотношение между бутаном и водяным паром составляет примерно 1:2. Использование водяного пара имеет много преимуществ, которые особенно отчетливо проявляются на 2-ой стадии – при дегидрировании бутана в бутадиен. Пар поставляет тепло для эндотермического процесса и снижает парциальное давление дигидрируемого углеводорода, что благоприятствует дегидрированию, который протекает с увеличением объема и является равновесным процессом. Кроме этого отпадает необходимость в подогреве углеводорода до температуры дегидрирования, т. к. можно перегреть водяной пар. Ещё одно преимущество водяного пара заключается в возможности использования его для регенерации катализатора, для чего прекращают подачу углеводорода в реактор, а водяной пар вступает во взаимодействие с углеродистыми отложениями, образуя с ними водяной газ. По окончанию регенерации в реакционную ёмкость подают н-бутан и продолжают дегидрирование.
При работе по этому методу, н-бутан, полученный из природного газа и газов переработки нефти, дегидрируют в 2 стадии до бутадиена; суммарный выход составляет примерно 65%.
В качестве катализаторов дегидрирования по этому методу используют также катализатор N 105 (Шелог Девелопментко) следующего состава: Fe2O3 – 90%, Cr2O3 – 4.0%, K2CO3 – 6.0% и катализатор N 205, который содержит больше K2CO3.
3. Парофазный крекинг низкокипящих фракций нефти
При крекинге легкокипящих фракций нефти (50-200 0С), основным продуктом реакции является этилен, пропен, бутены и бутадиен. Благодаря подбору оптимальных условий процесса парофазного крекинга удается добиться максимального выхода бутадиена, составляющего 5%.
4. Пиролиз легких фракций нефти
При пиролизе лигроинов и газойлей, производимых с целью получения этилена, неизбежно образуется фракция С4, состоящая из бутанов, бутенов и бутадиена. Бутадиен выделяют из фракции селективной адсорбцией медноаммиачными растворами или экстрактивной перегонкой в присутствии фурфурола.
5. Метод
В присутствии в качестве катализатора смеси оксидов алюминия и цинка бутадиен получают из этилового спирта. На первой стадии, в результате димеризации молекул этилового спирта образуется бутандиол-1,3, дегидрация и дегидрирование которого приводит к бутадиену:
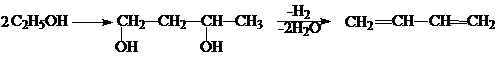
6. Частичное восстановление винилацетилена
Каталитическое гидрирование винилацетилена над катализатором Линдлара (палладий на карбонате кальция, модифицированный тетраацетатом свинца) приводит к образованию
![]()
Винилацетилен в свою очередь получают димеризацией ацетилена:
![]()
в присутствии водного раствора СuCl в аммиаке.
Получение изопрена
1. Изопрен по аналогии с бутадиеном, чаще всего получают дегидрированием ф. С5, полученной при крекинге нефти.
2. Другой способ получения изопрена заключается в каталитическом дегидрировании изопентана, который является, в свою очередь, продуктом изомеризации пентана:
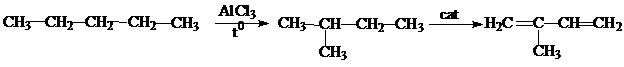 Получение хлоропрена
Получение хлоропрена
Хлоропрен получают присоединением хлористого водорода к винилацетилену. При этом присоединение идет в положении 1,4, давая аллен, который легко перегруппировывается в 2-хлорбутадиен-1,3:
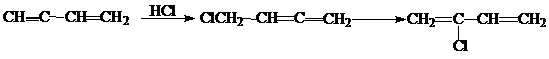
1.1.4. Химические свойства сопряженных диенов и полимеры на их основе
Сопряженные диены обнаруживают значительно более высокую реакционную способность, чем моноены и несопряженные диены. Это связано с определенной молекулярной структурой диенового звена, включающей взаимодействие 2-х двойных связей за счет перекрывания соответствующих р-орбиталей углеродов С2 и С3, в результате чего сопряженные диены ведут себя как единая система, а не как соединения с 2-мя независимыми двойными связями.
1. Гидрирование
Каталитическое гидрирование сопряженных диенов приводит обычно к образованию олефинов – продуктов 1,2 и 1,4-присоединения водорода. Кроме того, существует тенденция к дальнейшему гидрированию образующихся олефинов до соответствующих алканов.
а) восстановление диенов натрием в жидком аммиаке дает продукты 1,4-присоединения:
![]()
Аналогичное (1,4) присоединение водорода наблюдается при использовании ароматических трикарбонилхромовых комплексов.
б) селективного гидрирования сопряженных диенов в олефины путем 1,2- присоединения к наиболее замещенной двойной связи можно добиться с использованием каталитической системы: CoBr(PPh3)-BF3:
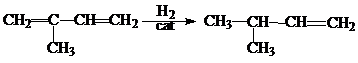
2. Реакция Дильса-Альдера
По реакции Дильса-Альдера диены-1,3 реагируют с алкенами и алкинами – с образованием шестичленных гидроароматических колец:
![]()
![]()
Реакция обратима и осуществляется обычно простым смешением компонентов при комнатной температуре или при слабом нагревании в подходящем растворителе. Присоединение происходит гораздо легче в том случае, если диенофил, содержащий отрицательные группы: карбоксильную, карбонильную, нитрильную им подобные:
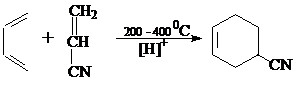
Реакция Дильса-Альдера обладает высокой стериоспецифичностью.
3. Гидрохлорирование
Продукты реакции сопряженных диенов с НСl образуется в результате конкурентного 1,2- и 1,4-присоединения.
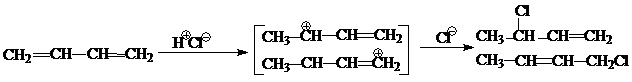
Относительные количества образующихся 1,2- и 1,4-продуктов зависят от условий реакций, т. е. от температуры, продукты растворителя и продолжительности процесса. При обычных условиях реакции, основным продуктом оказывается 1,4-соединение, проведение реакции при низких температурах приводит к 1,2-присоединению НСl.
4. Галогенирование (электрофильная реакция)
Реакции галогенирования (Cl2, Br2) протекают аналогично реакции гидрохлорирования диенов с образованием смеси продуктов 1,2- и 1,4-присоединения, соотношения количеств которых зависит от условий
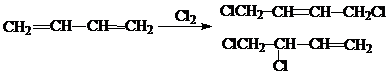
5. Присоединение хлорноватистой кислоты (электрофиль.)
Протекает аналогично НСl, Наl с образованием смеси продуктов:
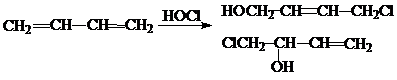
6. Реакция Лебедева
Димеризация изопрена и бутадиена приводит к образованию замещенных циклогексенов; при этом одна из 2 молекул диена выступает как диенофил.
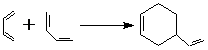
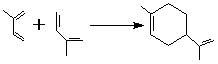
Реакция проводится в жестких условиях и дает низкий выход.
Реакции полимеризации сопряженных диенов
1. Полимер бутадиена – бутадиеновый каучук получают полимеризацией в растворе с применением комплексных металлорганических катализаторов типа Циглера-Натта или с применением литийорганического катализатора. В первом случае мономер входит в структуру макромолекулы в основном положении 1,4-цис (87-90%), остальная часть мономера – в положении 1,4-транс и в положении 1,2:
![]() ,
, ![]()
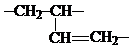
во втором случае содержание 1,4-цисструктуры снижается до 40-46% при Т=-(60-65) 0С. При обычной температуре аморфен.
2. Полимеры изопрена – изопреновые каучуки получают полимеризацией в растворе под действием тех же катализаторов, что и для бутадиенового каучука. При использовании катализаторов Циглера-Натта (СКИ-3), содержание 1,4-цис структуры изопрена достигает 98%, при использовании литийорганического катализатора (СКИЛ) содержание 1,4-цис-структуры заметно снижается. СКИ-3 содержит до 30% разветвленных макромолекул. Молекулярная масса равна тыс., способны к кристаллизации при растяжении и охлаждении. Нестоек к действию углеводородов и масел.
3. Хлоропреновый каучук получают в условиях, близких к условиям получения синтетический каучук дивиниловый (СКД) и СКИ-3. Макромолекулы полимера имеют 1,4-транс-конфигурацию. Хлоропреновый каучук отличает высокая устойчивость к агрессивным средам, прекрасная стойкость к действию масел и углеводородов.
1.2. Виниловые мономеры
1.2.1. Получение винилхлорида
Наиболее доступным из винилгалогенидов является хлористый винил, который можно получить рядом способов:

1. Самый удобный из этих способов получения винилхлорида основан на высокотемпературном хлорировании этилена:
![]()
Оксихлорирование этилена
Для получения различных хлорэтиленов, производимых в промышленных масштабах, предпочитают использовать синтезы на основе этилена. Это стало возможно в результате разработки метода оксихлорирования. В случае получения винилхлорида реакция протекает при пропускании этилена в смеси с хлором и кислородом над медным катализатором при повышенной температуре:
![]()
При этом способе хлор не теряется на образование хлористого водорода.
2. Дегидрогалогенирование дихлорэтана
Существует несколько различных способов получения винилхлорида дегидрогалогенированием дихлорэтана:
а) при пропускании паров дихлорэтана над железой или активированным углем при Т=500 0С образуется винилхлорид
![]()
б) Дегидрогалогенирование дихлорэтана осуществляют также в щелочной среде (раствор NaOH в СН3OH) при температуре 50-70 0С с 95%-ным выходом винилхлорида.
в) при термическом дегидрохлорировании при 600-650 0С в трубке с гладкими стенками можно получить винилхлорид с выходом > 99%.
г) присутствие небольших количеств свободного хлора значительно снижает температуру дегидрогалогенирования дихлорэтана. Так в присутствии 0,5% (объемов) хлора при 370 0С можно получать винилхлорид с выходом 70%. Это можно объяснить протеканием цепной реакции по следующей схеме:
![]()
![]()
![]() и т. д.
и т. д.
3. Гидрохлорирование ацетилена
Основные количества винилхлорида в технике производят присоединением хлористого водорода к ацетилену:
![]()
Физические свойства
В обычных условиях винилхлорид – газ, с характерным запахом. Ткип при атм. давлении – -13,8 0С, Тпл=-153,77 0С.
1.2.2. Химические свойства винилхлорида
1. Винилхлорид вступает в реакцию электрофильного присоединения, например, при смешении паров СН2СНСl и Сl2 на свету при Т=100-250 0С образуется 1,1,2-трихлорэтан:
![]()
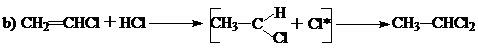
2. Считая, что соединения с атомом хлора углерод несет некоторый положительный заряд, что было доказано экспериментально реакцией бутиллития с винилхлоридом при – 100 0С:
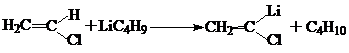
Отщепление под действием сильного основания соседнего с хлором водорода в виде протона, связывающего с бутильным остатком, ясно указывает на положительный заряд углерода, несущего хлор.
3. В обычных условиях хлор в винилхлориде не замещается на нуклеофильные частицы, что связано с алкилгалогенидами. Однако, в жестких условиях под действием сильных оснований – нуклеофилов (КОН, КОR) осуществляется нуклеофильное замещение:

4. В присутствии Н2SO4 винилхлорид взаимодействует с водой с образованием уксусной кислоты:
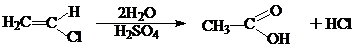
1.2.3. Галогенсодержащие полимеры
Поливинилхлорид (ПВХ) получают радикальной полимеризацией винилхлорида в присутствии пероксидных и азоинициаторов. В промышленных условиях полимеризацию осуществляют в основном в суспензии (в водной среде), а также в эмульсии и в массе. Средняя степень полимеризации ПВХ от 450 до 1750, соответственно полимер характеризуется широким ММР. ПВХ - аморфный полимер (степень кристалличности не превышает 10%) с Тст=70-80 0С. Стоек к действию агрессивных сред, масло-, бензо - и водостоек, при нагревании растворяется в хлорированных углеводородах, кетонах, циклогексане, тетрагидрофуране.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



