Конспект лекций по курсу «МОНОМЕРЫ»
для бакалавров, обучающихся по специальности
240100.62 «Химическая технология» и специалистов,
обучающихся по специальности 020201.65
«Фундаментальная и прикладная химия»
Нальчик, 2014 г.
Оглавление
Введение……………………………………………………………………....4
Глава 1. Мономеры для полимеризации…………………………………5
1. 1. Олефины …………………………………………………………………5
1.1.1. Получение олефинов…………………………………………………..5
1.1.2. Химические свойства олефинов……………………………………..15
1.1.3. Получение сопряженных диенов…………………………………….22
1.1.4. Химические свойства сопряженных диенов и полимеры
на их основе…………………………………………………………...24
1. 2. Виниловые мономеры………………………………………………….27
1.2.1. Получение винилхлорида…………………………………………….27
1.2.2. Химические свойства винилхлорида………………………………..28
1.2.3. Галогенсодержащие полимеры………………………………………29
1.3. Стирол…………………………………………………………………...29
1.3.1. Получение стирола……………………………………………………29
1.3.2. Химические свойства стирола……………………………………….30
1.3.3. Полимеризация стирола и его сополимеры…………………………31
1.4. Акрилонитрил…………………………………………………………..32
1.4.1. Получение акрилонитрила…………………………………………...32
1.4.2. Химические свойства акрилонитрила………………………………33
1.4.3. Полимеризация акрилонитрила и его сополимеры…. …………….34
Глава 2. Мономеры для поликонденсаций……………………………..35
2.1. Классификация мономеров. Сомономеры.
Гомо - и гетерополи-конденсация……………………………………36
2.2. Алифатические дикарбоновые кислоты………………………………38
2.2.1. Основные методы получения алифатических
дикарбоновых кислот………………………………………………...38
2.2.2. Химические свойства алифатических дикарбоновых кислот……...41
2.2.3. Получение непредельных одноосновных карбоновых кислот…….44
2.2.4. Физические и химические свойства непредельных
карбоновых кислот…………………………………………………...45
2.2.5. Полимеризация непредельных карбоновых кислот………………..46
2.3. Алифатические и алициклические диамины…………………………47
2.3.1. Получение алифатических диаминов……………………………….47
2.3.2. Получение алициклических диаминов……………………………...49
2.3.3. Химические свойства алифатических и алициклических диаминов……………………………………………………………………..52
2.3.4. Полимеры на основе алифатических и алициклических
диаминов………………………………………………………………53
2.4. Диолы и бисхлорформиаты…………………………………………….54
2.4.1. Получение α-диолов…………………………………………………..54
2.4.2. Получение b-диолов………………………………………….. ……...55
2.4.3. Получение g-диолов и высших гликолей……………………………57
2.4.4. Химические свойства гликолей……………………………………...58
2.4.5. Получение и свойства бисхлорформиатов….....................................59
2.4.6. Поликонденсация гликолей…………………………………………..59
2.5. Ароматические дикарбоновые кислоты……………………………….61
2.5.1. Получение ароматических дикарбоновых кислот………………….61
2.5.2. Химические свойства ароматических дикарбоновых кислот……..64
2.5.3. Получение и свойства хлорангидридов
ароматических дикарбоновых кислот….……………………………65
2.6. Ароматические диамины……………………………………………….65
2.6.1. Получение ароматических диаминов………………………………..66
2.6.2. Химические свойства ароматических диаминов……………………69
2.6.3. Полимеры на основе ароматических диаминов…………………….70
2.7. Бисфенолы………………………………………………………………72
2.7.1. Получение бисфенолов………………………………………………72
2.7.2. Химические свойства бисфенолов…………………………………..75
2.7.3. Полимеры на основе бисфенолов……………………………………75
2.8. Диангидриды тетракарбоновых кислот……………………………….77
2.8.1. Получение диангидридов тетракарбоновых кислот………………..77
2.8.2. Химические свойства диангидридов тетракарбоновых кислот……78
Литература………………..………………………………………………...80
Заключение………………………………………………………………….81
Введение
Одной из важнейших проблем полимерной химии является создание материалов с ценными физико-химическими свойствами, которые требуются для развития современной промышленности. Решение этой проблемы тесным образом связано с получением исходных реагентов (мономеров) для синтеза полимера. При этом мономерные вещества делятся на мономеры полмеризационного и поликонденсационного характера.
Данный курс ставит целью изучение основных принципов и технологических способов получения различных мономеров, из которых в дальнейшем синтезируют полимеры. При этом для получения мономеров в качестве исходного сырья широко используются природный газ, нефть, уголь. Кроме того ряд мономерных веществ получают синтетическими методами с использованием реакций органического синтеза.
Следует отметить, изучение кинетических закономерностей протекания реакций получения мономеров, особенно, полимеризационного характера, показывают о существенном влиянии различных факторов на процессы. В частности, изменение условий (температура, давление, катализатор) позволяет смещать равновесия процессов и увеличить выхода целевых продуктов. В свою очередь существующее и получаемое разнообразие мономерных веществ позволяет конструировать строение макромолекулы полимера, с целью создания материала с комплексом ценных физико-химиеских свойств.
Для успешного усвоения курса необходимо знание таких фундаментальных дисциплин, как: органическая химия и физическая химия.
Глава 1. Мономеры для полимеризации
1.1. Олефины
Обычно принято делить олефины на две группы:
а) низкомолекулярные олефины – в обычных условиях газообразные или низкокипящие вещества (начиная с этилена и кончая гексенами);
б) высокомолекулярные олефины – в обычных условиях жидкие (от гексенов и выше).
В группу моноолефинов входят этилен, пропилен, бутилен, пентены. Для современной химической промышленности эти углеводороды являются важнейшим химическим сырьем, а для полимерной химии ряд из них, например, этилен, пропилен и изобутилен – важными исходными мономерами.
1.1.1. Получение олефинов
Моноолефины могут быть получены следующими методами:
1) Выделение из смесей, образующихся в качестве неизбежных продуктов реакции и состоящих из газообразных парафинов и олефинов; такие смеси содержатся:
а) в газах переработки нефти (газах крекинга и газах образующихся при термических и каталитических процессах);
б) в газообразных продуктах синтеза Фишера-Троппа, проводимые с Со и Fe-ми катализаторами;
в) в газообразных продуктах коксования и швелевания каменного и бурого углей.
2) Непосредственным производством газообразных олефинов, которые, следовательно, являются целевыми продуктами; это:
а) дегидрирование газообразных парафиновых углеводородов (каталитическое и термическое);
б) пиролиз низко - и высокомолекулярных углеводородов:
1) газообразных углеводородов;
2) высокомолекулярных углеводородов (особенно нефтяных фракций);
в) дегидратация низкомолекулярных спиртов – этанола, пропанола, бутанолов и пентанолов.
Дегидрирование газообразных парафиновых углеводородов.
Каталитическое дегидрирование.
В случае парафиновых углеводородов (ПУВ) дегидрирование ведет к образованию олефинов с тем же числом углеродных атомов. Так, из этана образуется этилен, из пропана – пропилен и т. д. Практически дегидрирование ПУВ проводят нагреванием их в присутствии определенных катализаторов, причем большую роль играет соблюдение экспериментально установленного времени контакта углеводорода с катализатором.
Реакция дегидрирования газообразных ПУВ с открытой цепью идет со значительно большей затратой энергии, чем разрыв связи С-С. Так, например, для расщепления связи С-С в молекуле бутана необходимо затратить около 62,5 ккал/моль энергии. Для отрыва первичных атомов водорода у газообразных ПУВ необходимы 87 ккал/моль энергии; вторичных атомов водорода – 85,7 ккал/моль, а третичных – 85 ккал/моль энергии, т. е. энергия необходимая для расщепления алифатической связи С-С (крекирование) на 20 ккал/моль меньше энергии для отрыва С-Н-связи (дегидрирование).
Поэтому, удовлетворяющее техническим требованиям дегидрирование не может быть достигнуто общим лишь воздействием тепловой энергии, т. к. в этих условиях, прежде всего и в наибольшей степени будет идти крекинг, дегидрирование является лишь побочной реакцией. Поэтому различают деструктивное и недеструктивное дегидрирование. Причем, получение удовлетворяющих выходов при недеструктивном дегидрировании возможно лишь каталитическим путем.
При нагревании до высокой температуры газообразных углеводородов с числом углеродных атомов больше 2-х протекают две основные реакции:
во-первых, расщепление С-С связи с образованием низкомолекулярных олефина и парафина, по реакциям:
СН3-СН2-СН2-СН3 → СН3-СН=СН2 + СН4
СН3-СН2-СН2-СН3 → СН2=СН2 + СН3-СН3
во-вторых, дегидрирование в результате, которого отщепляется водород и образуется олефин с тем же числом углеродных атомов:
СН3-СН2-СН2-СН3 → СН3-СН2-СН=СН2 + Н2
СН3-СН2-СН2-СН3 → СН3-СН=СН-СН2 + Н2
Для алифатических УВ с увеличением числа углеродных атомов реакция крекирования проявляется все более резко. Метан по отношению к термическим воздействиям очень устойчив. Этан при нагревании даже в присутствии катализаторов подвержен только дегидрированию и превращается преимущественно в этилен и водород. В случае пропана образуется значительно больше этилена и метана, чем пропилена и водорода.
Реакцию крекинга нельзя подавить каталитическим путем. Но применением соответствующих катализаторов можно сильно ускорить реакцию дегидрирования, вследствие чего процесс отщепления водорода заканчивается в такие промежутки времени, в течение которых крекинг успевает проявиться лишь в малой степени.
В зависимости от метода дегидрирования газообразных ПУВ – термического и каталитического – образуется разные продукты переработки.
Катализаторы реакции дегидрирования. Пригодный для дегидрирования ПУВ катализатор должен удовлетворять следующим требованиям:
1) селективно отщеплять водород, не благоприятствуя крекированию;
2) легко регенерироваться после потери активности;
3) быть стойким по отношению к высокой температуре, особенно во время регенерации; критический срок службы его должен составлять сотни часов;
4) быть дешевым, приготовление его должно быть не сложным.
Этим требованиям в достаточной мере удовлетворяют катализаторы, состоящие из окиси хрома и окиси алюминия. В то время как чистая окись хрома уже при 450 0С, правда, в течение короткого времени является исключительно активной, смесь окиси хрома и окиси алюминия проявляет себя удовлетворительно лишь при 500-600 0С. Но устойчивость такого катализатора несравненно больше, и это имеет решающее значение при его использовании в технике. Исследовалось также дегидрирующее действие окиси алюминия и комбинации окиси алюминия и окиси хрома с различным содержанием хрома. Чистая окись алюминия активна лишь при высокой температуре. Дегидрирование при этом мало селективно, велика доля продуктов крекирования. При добавлении 2% окиси хрома температуру реакции можно снизить, вследствие чего крекинг несколько замедляется. Катализатор, содержащий 12-15% окиси хрома, наиболее активен.
Катализатор необходимо часто регенерировать, т. к. через короткое время он покрывается слоем кокса, снижающим его активность. Кокс выжигают при температуре большем температуры дегидрирования, поэтому к механической прочности катализатора предъявляют очень высокие требования. Кроме этого катализатор для большей эффективности должен быть однородным. Для получения этилена из этана используют каталитические методы дегидрирования.
Температура реакции дегидрирования. Т. к. реакция дегидрирования сильна эндотермична и положения равновесия зависит от температуры, при котором подводиться необходимая для реакции тепло, то с увеличением температуры увеличивается, и содержание олефинов в реакционной смеси. Чтобы получить возможно больше олефинов следует вести дегидрирование при Т = 600-700 0С. В производстве практически придерживаются интервала 500-600 0С. При низкой температуре степень превращения парафинов очень мала, и чтобы добиться удовлетворительного выхода олефинов, нужно сильно увеличить время контакта УВ с катализатором. При этом производительность установки сильно падает, кроме того, длительное пребывание в зоне катализа способствует тому, что реакция крекирования выступает на первый план. Одновременно все больше проявляется чисто термические, вторичные реакции, такие, как полимеризация и ароматизация. То же происходит в случае, если дегидрирование ведут при слишком высокой температуре. При этом вынуждают придерживаться во время реакции определенного температурного интервала, который несколько различен для разных УВ-ов.
Как правило, с повышением температуры увеличивается и степень превращения, но количество олефинов, образующихся из ПУВ с тем, же числом углеродных атом, уменьшается, иначе говоря, увеличение температуры способствует падению селективности процесса. Например, при Т = 620 0С и 26%-ой степени превращения 83% превращенного бутана переходит в бутен, т. е. селективность составляет 83%. Если температуру повысить до 680 0С, то степень превращения увеличивается до 37%, а селективность падает до 67%.
Влияние давления на дегидрирование. Как следует из уравнений реакции дегидрирования
С4Н10 ↔ С4Н8 + Н2
С3Н8 ↔ С3Н6 + Н2
процессы протекают с увеличением объема реакционной смеси, теоретически равной 100%. Поэтому уменьшение давления должно способствовать протеканию прямой реакции.
Например, степень превращения н-бутана в бутены при 527 0С и различных давлениях выглядит следующим образом:
Давление, атм | 0,01 | 0,1 | 1,0 | 10,0 | 100,0 |
Степень превращения, % | 97,0 | 80,0 | 38,5 | 13,0 | 4,0 |
При увеличении давления, вместе с уменьшением степени превращения наблюдается ухудшение селективности реакции дегидрирования. Например, если при Р=1 атм. можно в определенных условиях достигнуть 30%-го превращения и 82%-ой селективности, то при Р=3 атм. при прочих равных условиях селективность падает до 68%.
Продолжительность реакции (контакт газа с катализатором). Если очень быстро пропускать ПУВ над катализатором при возможно более высокой температуре, то реакция практически не идет. При увеличении длительности его контакта с катализатором то протекает реакция дегидрирования, причем при дальнейшем увеличении времени контакта, степень дегидрирования возрастает до максимальной. Помимо этого, и наблюдается далеко идущие побочные реакции вплоть до полного расщепления УВ-ов. Экспериментально установленный максимум выхода олефинов соответствует определенному времени контакта исходных газообразных парафинов с катализатором при определенной температуре. При времени реакции, превышающем оптимальное, выход олефинов падает, т. к. все больше проявляются побочные реакции.
Например, для пропана, как видно из табл. 1, с увеличением продолжительности реакции, степень его превращения увеличивается. Однако концентрация пропилена при этом не только не повышается, а в связи с протеканием побочных реакций, падает. При 600 0С и времени реакции 2,7 сек, каталитическое дегидрирование протекает практически без побочных реакций, водород и пропилен образуются примерно в равных количествах, эквивалентных расходу пропана.
При температуре 600 0С с использованием одного и того же катализатора, максимальное содержание бутена (30%) в отходящих печных газах, наблюдается при времени контакта н-бутана с катализатором равной 2 сек, а максимальный выход изобутилена (33%) при дегидрировании изобутана – при времени контакта 4 сек. При температуре 500 0С различия в поведении бутанов ещё отчетливее.
Таблица 1
Влияние продолжительности контакта на состав реакционных продуктов (в об. %) при каталитическом дегидрировании пропана при 600 0С
Компонент | Продолжительность контакта пропана с катализатором, сек | |||
2,7 | 8,9 | 17,5 | 36,0 | |
пропан | 59,0 | 41,0 | 32,0 | 6,0 |
пропилен | 20,0 | 21,0 | 14,0 | 9,0 |
водород | 20,5 | 24,0 | 27,5 | 29,0 |
этилен | 0,0 | 0,3 | 0,2 | 1,0 |
этан | 0,0 | 5,0 | 7,5 | 29,0 |
метан | 0,5 | 3,0 | 13,5 | 19,0 |
Для получения наибольшего количества бутена (20%) достаточно, чтобы н-бутан находился в контакте с катализатором в течении 5 сек., а для получения максимума изобутелена (19%) из изобутана – 30 сек.
Таким образом, тщательно подбирая продолжительность реакции и наиболее благоприятную для каждого катализатора рабочую температуру, можно достигнуть высоких значений выхода олефинов (высокой селективности) при незначительном протекании побочных реакций.
Термическое дегидрирование. Метод термического дегидрирования не является пригодным для всех газообразных УВ. В технике его применяют только для дегидрирования этана. При термическом дегидрировании пропана и бутанов значительное место занимают побочные реакции, ведущие к разрыву молекулы.
Дегидрирование этана в этилен достигается чисто термическим путем в отсутствии катализатора, причем крекинг его до метана и другие побочные реакции почти исключены.
Чисто термическое дегидрирование изобутана, в отличии от бутана, благодаря наличию в нем третичного водорода приводит к неплохим результатам. Так, при дегидрировании изобутана в производственных масштабах, конечный выход изобутилена при Т=650-730 0С, давлении 4,2-5,6 атм и степени превращения 20-30% составляет 50 вес. %. Наряду с изобутиленом при этом образуется 25% пропена, что вызывается реакцией крекинга, протекающей по уравнению:
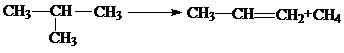
Особый интерес представляет термическое дегидрирование этана, которое может быть проведено 2-мя путями: аутотермическим и чисто термическим.
Аутотермическое дегидрирование. Этот метод дегидрирования, основан на применении кислорода и сводится к тому, что необходимое для реакции тепло, получают сжиганием в реакторе части предназначенных для дегидрирования ПУВ.
Смесь этана (около 100 объемов) и чистого кислорода (30 объемов), к которой примешан азот (3 объема), нагревают до 880 0С при давлении 350 мм рт. ст. Образующийся при этом конечный газ (газ расщепления) состоит из 170 объемных частей и содержит 30 объемных частей этилена. В газовом промывателе при атмосферном давлении, газы отмывают от органических кислот, образовавшихся в наибольшем количестве в результате окисления углеводородов и ацетилена (0,5-1%). Затем при Р=17,5 атм. газы отмывают от более тяжелых углеводородов (бензины) и угольной кислоты. После этого охлажденную до -45 0С газовую смесь перерабатывают компрессионно - конденсационным методом. При этом из 100 объемных частей газовой смеси получают 52 части остаточного газа, состоящего из водорода с небольшой примесью окиси углерода, азота и метана. Кроме того получают 18,5 частей этана 98-99%-ой чистоты, который возвращают в установку, и 30 объемных частей этилена 98-99%-ой чистоты.
Чисто термическое дегидрирование этана. Для чисто термического дегидрирования этан нагревают до 850-900 0С в трубах с наружным обогревом. В качестве материала для изготовления труб пригодна хромистая сталь, содержащая 25-30% хрома, 0,2% никеля и немного кремния. Кремний снижает степень крекирования, вследствие чего коксообразование сводится к минимуму. Газ проходит систему труб под небольшим давлением, находясь в контакте с катализатором очень короткое время; температуру газа предварительно доводят до 500 0С. В конечном газе содержится около 33 % этилена, что соответствует примерно 50 %-ному превращению этана. Газ содержит кроме этилена ещё примеси ацетилена и высокомолекулярных углеводородов. Конечный газ освобождают от ацетилена гидрированием над хромоникелевым катализатором, а затем – от высокомолекулярных углеводородов пропусканием через активированный уголь. В заключение на ректификационной колонне разделяют этан и этилен; этан возвращают в процесс. В качестве материала для труб при Т=800 0С можно использовать трубы из хромоникелевой стали 18/8, а при Т=900 0С – из хромоникелевой стали 25/20, хотя наилучшие результаты были достигнуты при использовании именно хромистой стали.
Пиролиз газообразных ПУВ (парофазный крекинг).
Общие сведения. При воздействии высокой температуры на газообразные ПУВ в первую очередь протекают реакции крекинга и получаются олефины и парафины с числом углеродных атомов, меньшим, чем в исходных углеводородах. Исключение составляют метан и этан. Этан претерпевает преимущественно дегидрирование с образованием этилена и водорода.
Олефины являются первыми продуктами пиролиза, образующимися в результате дегидрирования или крекинга. Эти первичные продукты можно быстро удалить из зоны нагрева, т. к. иначе они подвергаются дальнейшим превращениям и при длительном нагреве переходят в ароматические соединения. Поэтому соблюдение определенного времени пребывания перерабатываемых газов в пиролизных печах является важной предпосылкой образования олефинов с хорошими выходами.
Наиболее благоприятными условиями пиролиза является высокая температура и кратковременное пребывание продуктов в зоне реакции. При высокой температуре желаемые первичные реакции протекают с хорошей степенью превращения, вследствие того, что короткие сроки пребывания в зоне нагрева и большая устойчивость олефинов в этих условиях по сравнению с парафинами не благоприятствуют развитию побочных реакций.
Этан при пиролизе в основном подвергается дегидрированию. При этом наибольшее превращение его в этилен происходит при Т=834 0С и времени пребывания газа в зоне нагрева 0,8 сек.
Разрушение пропана при пиролизе происходит 2-мя путями: крекингом и дегидрированием. Крекинг не обратим, а дегидрирование является равновесной реакцией. При этом образуются следующие продукты:
СН3-СН2-СН3 → СН2=СН2 + СН4 (крекинг)
СН3-СН2-СН3 ↔ СН2-СН=СН2 + Н2 (дегидрирование)
Наибольшая степень превращения пропана (82%) наблюдается при Т=816 0С и времени пребывания пропана в зоне пиролиза 0,75 сек. Наибольшее количество олефинов содержится в выходных газах, если пиролиз проводят при Т=880 0С. При одном и том же времени реакции максимальное количество пропена образуется при Т=810 0С (дегидрирование), а максимальная концентрация этилена при Т=890 0С (пиролиз).
При пиролизе н-бутана наибольшее количество олефинов образуется при Т= 690 0С. Содержание пропена достигает максимума при 650 0С, а наибольшее количество этилена при 750 0С. Содержание н-бутена в выходящих газах не велико, что говорит о том, что дегидрирование протекает слабо. В состав первичных продуктов пиролиза входит несколько фракций: ф. С1 – метан; ф. С2 – этилен и этан; ф. С3 – пропен и пропан; и водород. Пиролиз нормального бутана является наиболее выгодным способом производства чистого пропена, так как ф. С3 практически состоит лишь из пропена, а пиролиз пропана – наиболее выгодным способом этилена, т. к. ф. С2 практически полностью составляет этилен.
При производстве олефинов крекингом газообразных углеводородов следует придерживаться, возможно, низкого давления, т. к. давление способствует их полимеризации. Попытки увеличить выходы олефинов при пиролизе увеличением длительности реакции с одновременным уменьшением температуры приводит к тому, что значительную активность начинают проявлять побочные реакции полимеризации и ароматизации образовавшихся олефинов. При пиролизе с цель получения полиолефинов рекомендуется проводить реакции в присутствии инертных разбавителей, например водяного пара.
Пиролиз газообразных парафинов. Проводят тремя способами (в технике):
1) Производства этилена крекингом пропана
Установка при этом состоит из двух частей: пиролизной, которая представляет собой в виде змеевика, нагреваемы жидким топливом и газом и установки для охлаждения и разделения выходящих газов.
Исходным сырьем для крекирования служит пропан-этановая смесь. Содержанием бутана и высокомолекулярных ПУВ не должно превышать 2%, иначе в крекируемом газе в большом количестве образуется кокс и сажа.
Температура реакции колеблется в пределах 775-780 0С. Продолжительность пребывания газа в зоне нагрева 0,1 сек. Среднее рабочее давление в системе около 3,5 атм., причем давление при выходе газа из пиролизной трубчатке примерно равно 2,4 атм. в определенных условиях можно добиться 90% степени приращении пропана при однократном прохождении25% этана и 75% пропана. Но эти условия настолько жесткие, что уже 2 недели трубы нужно очищать от образовавшегося в большом количестве кокса, вследствие чего ограничивается 85% степенью превращения пропана. Аппаратура при этом служит долгое время безотказно. Использование водяного пара добавляемого в газовую смесь способствует уменьшению коксообразования и снижению коррозии, вызываемой сернистыми соединениями которые содержатся в газах.
2) Метод Филлипса
Установка состоит из 2-х выложенных огнеупорным камнем цилиндров, смонтированных один над другим и связанным между собой трубой диаметром около 17,7 см, также выложенной огнеупорным материалом. В верхнем цилиндре, служащим камерой предварительного подогрева при помощи топочных газов нагревают каменные шарики диаметром 1см шарики одновременно с крекированным материалом поступает в нижний цилиндр – реактор, встречаясь друг с другом в противотоке, оттуда в резервуар, из которого их снова переводят в камеру предварительного нагрева током горячего воздуха. Газы, применяемые для нагрева камней, получают сжиганием природного газа под давлением 0,35 атм. в рубашке подогревателя (верхнего цилиндра). После реакции газы охлаждают до 200-300 0С и подвергают переработке.
При пиролизе методом Филлипса получаются прекрасные результаты. Например, крекирование н-бутана при первоначальной температуре камней в реакторе 9430С приводит при однократном его прохождении 91% превращению. Из 100 кг введенного в реакцию бутана получают 44,1 кг этилена и 12,5 кг пропена.
3) Термофор – пиролиз
Процесс пригоден для дегидрирования этана или пиролиза пропана.
Пиролиз осуществляют пропусканием нагретых паров углеводородов над накаленным огнеупорным материалом с использованием печей специальной конструкции, в которой максимально используется тепло. При получении олефинов регенеративным методом температура реакции выше, чем при пиролизе в трубчатом нагревателе, а длительность пребывания газов в печи выражается дробными долями секунды. При Т= 0С из пропана при 85-100% степени превращения образуется этилен с выходом 34% вес., из этана при 900-980 0С при 75-80% превращении образуется 52,5% вес. этилена, из равных объемов пропана и этана при 0С образуется этилен.
Прямое получение газообразных олефинов пиролизом нефти и ее фракций. Перерабатывать нефтяные фракции на олефины можно двумя путями. Их подвергают парофазному крекингу при 600-700 0С в присутствии большого количества водяного пара, который служит разбавителем и переносчиком тепла, а также препятствует коксованию. При крекинге образуются газообразные алифатические углеводороды, а также жидкие продукты пиролиза, содержащие до 50-70% ароматических углеводородов, выделение которых обходится дорого. Процесс пиролиза можно направлять, так что образующиеся жидкие продукты реакции на 90-95% будут состоять из ароматических углеводородов, переработка которых проста и легко выполнима.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



