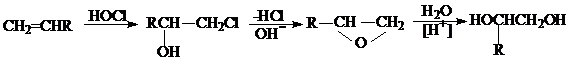
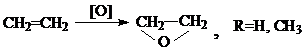
Из этиленхлоргидрина окись этилена получают обработкой щелочью. Гидролиз окиси этилена проводят при нагревании с водой при высоких Т и Р (195 0С, 15 атм.). Гидролиз ускоряется Н2SO4.
Существуют методы прямого окисления этилена до окиси этилена кислородом воздуха при высоких Т=250-290 0С и давлении Р=14 атм. в присутствии в качестве катализатора окиси серебра:
![]()
Прямое окисление окиси пропилена воздухом или кислородом не приводит сколь нибудь высоким выходам окиси пропилена, поэтому хлоргидринный путь его получения остается основным промышленным способом. Тем не менее, хорошие результаты получаются при окислении пропилена в присутствии в качестве катализатора нафтената молибдена. Гидролиз окиси пропилена происходит в сравнительно жестких условиях, а в присутствии катализатора – в более легких условиях.
2. Гидролиз других функциональных групп.
Наибольшее применение здесь находят гидролиз галогенпроизводных или хлоргидринов пропилена и этилена:
![]()
![]()
Гидролиз хлоргидринов проводят в водном растворе в присутствии дикарбоната натрия при Т=70-90 0С.
3. Гидрирование и восстановление.
α – диолы получают гидрированием или восстановлением различных соединений. Так, этиленгликоль синтезируют гидрированием гликоля сложных эфиров гликолей, глеколевой или щавелевой кислоты, например:
![]()
Полипропилен получают из эфиров молочной кислоты глицидного спирта (?) и глицерина. В небольших количествах пропиленгликоль образуется в качестве продукта гидрирования глицеридов жирных кислот.
4. Другие способы.
Из остальных способов получения α – диолов практическое применение находят реакции окисления двойной связи непосредственно до гликолей. Например, присоединение перекиси водорода к олефинам в присутствии в качестве катализатора окислов различных металлов. При окислении перекисью водорода в присутствии тетраокиси осмия образуются соответствующие диолы с хорошим выходом.
![]()
Хорошие результаты получаются также при использовании в качестве катализатора органических надкислот.
Окисление по двойным связям можно проводить также перманганатом калия, хлоратом, электролитически и т. д.
Пропиленгликоль можно получать также ферментативным гидролизом глицерина.
2.4.2. Получение β – диолов
Основными способами получения β – диолов, наиболее важными из которых является бутандиол-1,3, неопентилгликоль и 2,2,4-триметилпентадиол-1,3 являются реакции восстановления продуктов альдольной конденсации 2-х альдегидов и реакция Принса.
1. Альдольная конденсация.
Альдольная конденсация катализируется кислотами или основаниями, причем основания применяются чаще. Когда в реакции участвует 1 альдегид, её называют самоконденсацией, 2 и более различных альдегидов – смешанной конденсацией.
Бутандиол-1,3 получают из ацетальдоля (3-оксимаслянного альдегида), который в свою очередь получают самоконденсацией ацетальдегида:
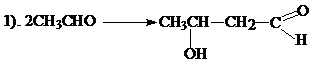
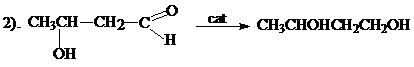
Неопентилгликоль получают альдольной конденсацией изомасляного альдегида и формальдегида с последующей перекрестной реакцией Коницаро:
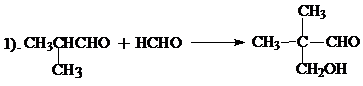
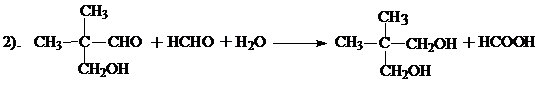
2,2,4-триметилпентандиол-1,3 получают восстановлением продукта альдольной самоконденсации изомасляного альдегида:
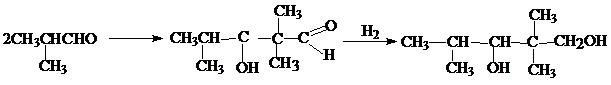
2. Реакция Принса.
Под влиянием кислых катализаторов формальдегид в водных растворах присоединяется к двойной связи в виде метиленгликоля:
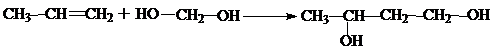
3. Гидрирование и восстановление.
Наиболее распространенным из этих методов является восстановление β-кетоспиртов в присутствии в качестве катализатора восстановителя амальгамы алюминия или гидрирование над окисью платины, активированной FeCl3 при высоких температурах:
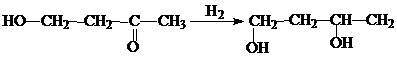
Другой наиболее применимый способ получения β-диолов – восстановление сложных эфиров над Р при высоких Т в присутствии хромита меди:
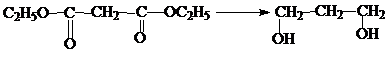
2.4.3. Получение γ – долов и высших гликолей
В γ-диолах и высших гликолях гидроксильные группы практически ведут себя независимо друг от друга. Восстановление таких функциональных групп, обычно идет гладко.
1. Все методы синтеза γ-диолов и высших гликолей, в настоящее время основаны на реакциях восстановления и каталитического гидрирования.
а) Реакция этинилирования.
Уникальные возможности для синтеза γ-диолов представляет реакция присоединения ацетилена к карбонильной двойной связи – этинилирование, с образованием ацетиленгликолей:
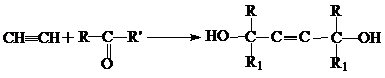
Так, в промышленную основу синтеза бутиндиола-1,4 положена именно эта реакция:
![]()
Реакцию проводят при Т=110 0С и Р=5 атм., пропуская исходные реагенты над этиленидом меди на носителе. Дальнейшее гидрирование бутиндиола в присутствии в качестве катализатора Ni (или Pt) (Т=40-60 0С, Р=210 атм.) дает 1,4-бутандиол.
б) Восстановление производных карбоновых кислот.
В лабораторной практике диолы удобно получать восстановлением дикарбоновых кислот и их производных, особенно эфиров. Для восстановления используют ряд способов. В их числе восстановление алкоголятом натрия, LiAlH4, а также каталитическое гидрирование с использованием в качестве катализатора хромита меди, реже никелевых и кобальтовых катализаторов.
в) Другие реакции гидрирования.
Длинноцепочечные α, ω-диолы получают восстановлением бифункциональных или циклических соединений, например, лактонов. Например, гександиол можно синтезировать гидрированием капролактона, 2,5-оксиметилтетрагидрофурана, 5-оксиметилфурфурола и т. д. Пентадиол-1,5 образуется вместе с другими продуктами при гидрировании различных производных фурана, фурфурола и фурилового спирта.
2. Другие методы синтеза.
γ-Диолы и другие высшие диолы, гидроксильные группы которых ведут себя независимо, можно получать любыми способами, применяющимися для синтеза спиртов. Наиболее распространенные общие методы – это омыление дигалогенидов или гидролиз соответствующих простых эфиров.
2.4.4. Химические свойства гликолей
На химические свойства гликолей влияет взаимное расположение гидроксильных групп. За исключением взаимодействия гидроксильных групп диолов друг с другом, в остальном для гликолей характерны те же реакции, что и для спиртов:
1. Образованием алкоголятов с металлическим натрием;
2. Образование моно - и дизамещенных сложных эфиров с карбоновыми кислотами и хлорангидридами кислот;
3. Окисление (Сu, t), приводящее для первичных гидроксильных групп к альдегидам, вторичных – кетонам;
4. Образование хлоргидринов и бромгидринов при действии HCl или HBr (лучше PCl5 или SOCl2);
5. Дегидратация гликолей.
Этиленгликоль, бутандиол-1,4 и пентандиол-1,5 дегидратируются в присутствии сильных кислот с образованием циклических эфиров – 1,4-диоксана, тетрагидрофурана и шестичленного циклического эфира соответственно, а пропиленгликоль, гександиол-1,6 и высшие представители гликолей дегидратируются под действием кислых катализаторов при высоких Т с образованием линейных олигомерных простых полиэфиров.
6. Альдегиды в кислой среде реагируют с 1,2- и 1,3-гликолями с образованием пяти и шестичленных циклических ацеталей соответственно:
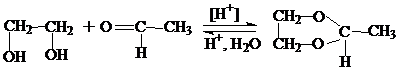
7. Диолы в инертной среде взаимодействуют с изоционатами с образованием уретанов:
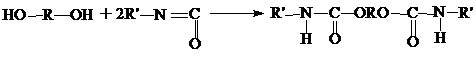
2.4.5. Получение и свойства бисхлорформиатов
Получение. Единственным общим методом синтеза хлорформиата является взаимодействие гидроксилсодержащих соединений с фосгеном:
![]()
Для α, β-гликолей параллельно идет побочная реакция образования циклических пяти - шестичленных карбонатов, от которых бисхлорформиаты очищают многократной промывкой водой.
Бисхлорформиаты гликолей, содержащих гидроксильные группы, разделенные не менее чем 4-мя атомами углерода, образуются с высоким выходом в значительно более мягких условиях без катализатора (третичные амины для α, β- гликолей).
Химические свойства. Хлорформиатная группа вступает в типичные реакции хлорангидридов кислот, но активность у них при этом меньше и поэтому в отсутствии катализаторов гидролизируется водой с очень низкой скоростью. Продуктами гидролиза хлорформиатов является спирт, СО2 и НСl.
Хлорформиаты гладко реагируют со спиртами с образованием карбонатов:

Хлорформиаты реагируют с аминами с образованием уретанов:
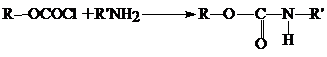
2.4.6. Поликонденсация гликолей
Гликоли представляют собой значительный интерес как исходные вещества в синтезе сложных и простых полиэфиров, полиацеталей и полиуретанов. В промышленном масштабе производятся только сложные полиэфиры и полиуретаны; простые полиэфиры и полиацетали получают в промышленности не из гликолей, а из других мономеров.
Сложные полиэфиры
Сложные полиэфиры – это наиболее важный класс конденсационных полимеров на основе гликолей. Среди них выделяются ненасыщенные полиэфиры (ПЭ), волокнообразующие ПЭ, поликарбонаты и олигомерные ПЭ.
Волокнообразующие ПЭ получают из линейных α, ω-диолов и линейных дикарбоновых кислот, хотя из-за низкой теплостойкости и малой гидролитической стойкости из них находят практическое применение. Этиленгликоль – единственный линейный гликоль, на основе которой получены ПЭ-ные волокна с высокими физико-механическими показателями. Для придания полиэфиру большей теплостойкости и высокой гидролитической стойкости в паре с этиленгликолем применяется ароматическая, главным образом терефталевая кислота.
Поликарбонаты можно получать разными способами, но наиболее предпочтительным является реакция поликонденсации бисхлорформиата и гликоля. Поликонденсация идет легко при нагревании реакционной смеси в вакууме:
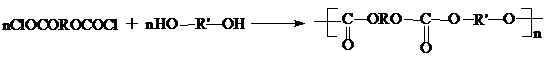
Другими способами получения поликарбонатов на основе гликолей является реакция эфирного обмена с диалкилкарбонатами или взаимодействие с эквимолекулярным количеством фосгена.
Полиуретаны (ПУ)
В промышленности ПУ получают реакцией диизоцианатов с гликолями:
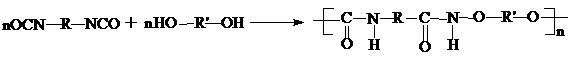
При этом конденсация изоцианатов и полимеров с концевыми гидроксильными группами имеет значительно больше промышленное значение, чем прямая конденсация их с мономерными диолами.
Простые полиэфиры
При дегидратации первичных гликолей за исключением некоторых (см. выше) получаются олигомерные простые эфиры. Однако ценные по свойствам простые полиэфиры получают не прямой дегидратацией, а например, полимеризацией циклических эфиров с раскрытием цикла.
Поликонденсация бисхлорформиата
Полиуретаны
Из 2-х способов получения полиуретанов реакциями диизоционатов с гликолями или бисхлорформиата с диаминами предпочитают второй путь. Это обусловлено тем, что во-первых, бисхлорформиаты (БХФ) получают намного легче, чем диизоцианаты, во-вторых, на основе БХФ значительно проще синтезировать высокомолекулярные полимеры методом межфазной поликонденсации.
К числу ПУ, которые легко образуются из БХФ, но не получаются через диизоцианаты относятся полимеры на основе БХФ и вторичных диаминов, например, пиперазина. ПУ на основе пиперазина обладают высокой теплостойкостью.
Реакции поликонденсации с участием БХФ проводят межфазным способом, когда БХФ растворяют в не смешивающемся с водой органическом растворителе, а диамин, например, в воде. Реакцию поликонденсации проводят при интесивном перемешивании для ускорения реакции и повышения выхода полимера.
Поликарбонаты (ПК). (см. выше)
ПК легко образуется при поликонденсации БХФ и многоатомных спиртов или ароматических диолов. Однако промышленное значение в основном имеют только чисто ароматические поликарбонаты.
2.5. Ароматические дикарбоновые кислоты
Из ароматических дикарбоновых кислот наиболее важны три изомерные бензолдикарбоновые кислоты, причем эти три кислоты и производятся в промышленном масштабе. о-Изомер известен под названием фталевая кислота, п-изомер – терефталевая кислота и м-изомер – изофталевая кислота. В настоящее время находят применение и ряд других ароматических дикарбоновых кислот, что связано с большей доступностью исходных веществ для их синтеза.
2.5.1. Получение ароматических дикарбоновых кислот
Фталевая кислота
Единственным важным способом синтеза ароматических дикарбоновых кислот является окисление алкилароматических соединений. Поэтому при синтезе той или иной дикарбоновой кислоты вопрос заключается в определении наиболее удобного способа проведения реакции и её режима.
1. Фталевую кислоту получают каталитическим окислением воздухом нафталина и о-ксилола через промежуточную стадию образования фталевого ангидрида.
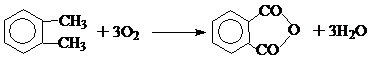
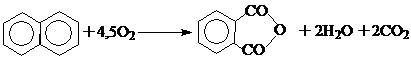
Окисление проводят в паровой фазе на ванадиевых катализаторах (обычно V2О5 на различных носителях) при Т=350 0С и выше.
На второй стадии гидролизом фталевого ангидрида в кипящей воде получают фталевую кислоту:
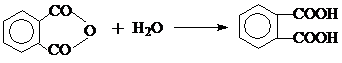
2. При Т=450 0С и использовании в качестве катализатора V2О5 можно получить фталевую кислоту прямым окислением нафталина кислородом воздуха.
Терефталевая кислота
1. Терефталевую кислоту можно получить окислением различных паразамещенных производных бензола. Промышленное производство т. к. базируется на жидкофазном окислении п-ксилола кислородом воздуха в среде карбоновой кислоты (УК) в присутствии ацетата кобальта как катализатора:
![]()
2. Прекрасным окислителем для окисления алкилароматических соединений является водный раствор бихромата натрия. При Т=280-290 0С под давлением окислением п-ксилола получают т. к.
3. Окисления п-ксилола в т. к. также можно производить в присутствии сильных окислителей, нaпример, HNO3, NO2 в присутствии ацетата кобальта как катализатора, двуокисью серы под давлением и т. д.
Изофталевая кислота
Изофталевая кислота образуется из м-ксилола и других мета - дизамещенных производных бензола с помощью тех же способов, которые используют в синтезе терефталевой кислоты из п-ксилола или других п - замещенных производных бензола, например, п-этилбензол, п-изо-пропилбензол, п-хлорметилтолуол, диацетилбензол, п-цианоацетофеноно, п-толилкарбинол и т. д.
4,4’ - дифенилдикарбоновая кислота
Из других ароматических дикарбоновых кислот наибольшее распространение в синтезе полимеров находят 4,4’ – дифенилдикарбоновая кислота, 4,4’ – дифенилсульфонкарбоновая кислота, 2,6-нафталиндикарбоновая кислота и 2,6 - пиридиндикарбоновая кислота.
1. Окисление 4,4’- дитолила.
Окисление проводят бихроматом калия в водном растворе серной кислоты при 275 0С в автоклаве:
![]()
2. Окисление 4,4’-диацетилдифенила (4,4’-ДАДФ).
Реакцию осуществляют двухстадийным способом по следующей схеме:
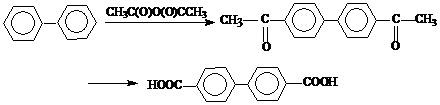
Окисление 4,4’-ДАДФ проводят в присутствии гипохлорита.
3. Окисление 4,4’-бис-(хлорметил)дифенила (4,4’- ДХМДФ).
Реакция также является 2-хстадийным с хлорметилированием дифенила на первой стадии и окислением образующегося ДХМДФ бихроматом калия.
4. 4,4’- дифенилсульфондикарбоновая кислота.
Получают обычно окислением ди-п-толилсульфона разными способами.
1. Окисление ди-п-толилсульфона хромовой кислотой.
Окисление проводят хромовым ангидридом в присутствии конц. Серной кислоты при Т=100-106 0С
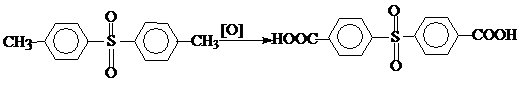
2. Аутоокисление (окисление кислородом воздуха).
Окисление проводят в присутствии ацетата кобальта (III) в качестве катализатора и ацетальдегида в качестве активатора реакции в растворе при пропускании через раствор кислорода при Т=90-95 0С.
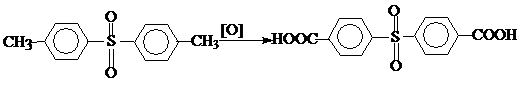
5. 2,6-нафталиндикарбоновая кислота (НДК).
Получают 2,6-НДК в 2 стадии из нафталевого ангидрида. На 1-ой стадии проводят обработку нафталевого ангидрида едким калия с образованием дикалиевой соли 1,8-нафталиндикарбоновой кислоты. На 2-ой стадии в присутствии безводного хлористого кадмия при давлении 30 атм. и Т=400-430 0С в автоклаве происходит перегруппировка дикалиевой соли 1,8-нафталиндикарбоновой кислоты в соль 2,6-нафталиндикарбоновой кислоты, обработкой которого конц. НСl получают 2,6-нафталиндикарбоновую кислоту:
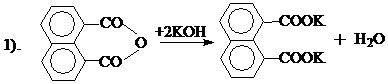
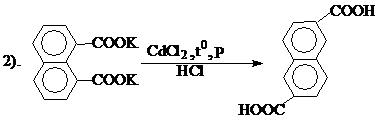
Физические свойства.
Все указанные ароматические дикарбоновые кислоты являются в основном бесцветными кристаллическими соединениями. Константы диссоциации для о-, м - и п-бензилдикарбоновых кислот равны:
Ароматические дикарбоновые кислоты | К1 | К2 | Кукс. |
о- | 1,123*10-3 | 3,5*10-6 | 1,5*10-5 |
м- | 2,4*10-4 | 2,5*10-5 | |
п- | 2,5*10-4 | 3,5*10-5 |
т. е. даже у вторичных карбоновых групп м-, п - терефталевой кислот кислые свойства более выражены, чем у уксусной кислоты.
2.5.2. Химические свойства ароматических дикарбоновых кислот
Ароматические дикарбоновые кислоты обладают всеми общими свойствами алифатических дикарбоновых кислот и в том, что касается поведения карбонильной группы, мало отличаются от карбоновых кислот алифатического ряда.
2.5.3. Получение и свойства хлорангидридов ароматических дикарбоновых кислот
Получение
1. Хлорангидриды ароматических кислот синтезируют обычными способами, исходя из самих кислот и SOCl2 или PCl5. При использовании PCl5 реакцию в начале ведут при комнатной температуре, а заканчивают при нагревании. Реакция идет более гладко в среде таких растворителей как бензол и СНСl3.
При использовании хлористого тионила часто в качестве катализатора добавляют наибольшее количество пиридина, амидов (особенно ДМФА). Побочными продуктами при использовании SOCl2 являются исключительно газообразные вещества, а образующийся хлорангидрид, легче поддается очистке.
2. Хлорангидриды кислот получают также прямым хлорированием ароматических альдегидов при высоких температурах.
Поликонденсация хлорангидридов карбоновых кислот
Интерес к хлорангидридам ароматических дикарбоновых кислот как к мономерам обусловлен их высокой реакционной способностью, проявляющиеся в энергичном взаимодействии с активными атомами водорода (аминами, спиртами) в присутствии акцептора протонов. Реакцию проводят с использованием межфазной конденсации хлорангидрида дикарбоновой кислоты в несмешивающемся с водой органическом растворителе и водного раствора диамина или диола. В межфазной поликонденсации применяются алифатические первичные и вторичные диамины или бисфенолы в воде их динатриевых солей. Вследствие низкой реакционной способности не удаётся получить высокомолекулярные полимеры на основе ароматических диаминов и алифатических диолов.
Полимеры на основе хлорангидрида терефталевой и изофталевой кислоты и алифатических гликолей получают в безводной среде в расплаве.
2.6. Ароматические диамины
Интерес к ароматическим диаминам как к мономерам для получения линейных полимеров обусловлен наличием комплекса ценных свойств у ВМС, содержащих только ароматические циклы. К этим свойствам относятся в первую очередь высокая термическая и термоокислительная устойчивость, намного превышающая достижимую для алифатических ПА, а также высокие модули упругости, обусловленные большей жесткостью цепей ароматических полимеров по сравнению с гибкими макромолекулами алифатических полимеров.
Для получения ароматических полимеров наибольшее применение находят о-, м - и п- фенилендиамин, бензидин, 4,4’- диаминодифенилметан, 4,4’- диаминодифенилоксид и некоторые из так называемых упорядоченных диаминов.
2.6.1. Получение ароматических диаминов
1. о-фенилендиамин.
а) Получают восстановлением о-нитроанилина цинковой пылью и щелочью (или сульфидом натрия) в этаноле при кипении:
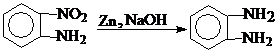
или восстановлением сульфидом натрия.
б) Второй способ заключается в обработке о-дихлорбензола или о-хлоранилина аммиаком под давлением при Т=150 0С
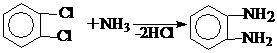
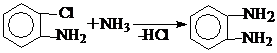
2. м-фенилендиамин.
а) Получают восстановлением м-динитробензола железом в конц. соляной кислоте при нагревании до кипения
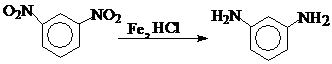
б) большое применение находит также метод непрерывного жидкофазного гидрирования м-динитробензола при умеренных температурах и интенсивном перемешивании. Предпочтительным катализатором восстановления является Pd/C. В качестве катализатора гидрирования используют также никель Ренея.
3. п-фенилендиамин.
а) Получают восстановлением п-нитроанилина – продукта аммонолиза п-хлорнитробензола – железом и соляной кислотой:
![]()
б) другой способ восстановления предполагает использование H2SO4, перегретого пара и специальной проточной аппаратуры, что приводит к образованию продукта высокой степени чистоты.
4. Бензидин (4,4’-диаминодифенил)
Единственным способом получения бензидина является хорошо известная бензидиновая перегруппировка. Бензидиновая перегруппировка является последовательным 2-х стадийным процессом с восстановлением нитробензола на 1-ой стадии до гидразобензола, который на 2-ой стадии перегруппировывается в бензидин:
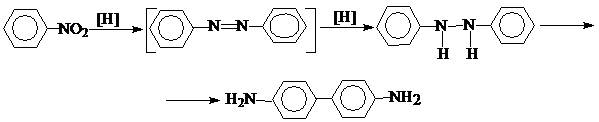
Восстановление нитробензола в гидразобензол протекает через промежуточную стадию восстановления с образованием азобензола. В качестве восстановителей нитробензола в гидразобензол используют цинк и щелочь или железо и воду. Перегруппировка гидразобензола в бензидин осуществляется в разб. HCl (или H2SO4) и приводит непосредственно к получению его дихлоргидрата (или сульфата).
5. 4,4’- диаминодифенилметан.
а) Получают конденсацией амина с формальдегидом в присутствии каталитических количеств сильных кислот, напримпер, НСl:
![]()
б) Следующий способ состоит в восстановлении 4,4’-динитродифенилметана Zn и HCl или последовательно фенилгидразином и гидразином.
в) Диамин также образуется и при декарбоксилировании 4,4’-диаминодифенилуксусной кислоты хлористым водородом при Т=180-200 0С:
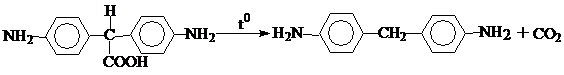
6. 4,4’-диаминодифенилоксид.
а) Восстановление 4,4’-динитродифенилоксида проводят никелем Ренея при 75 0С и Р=3,5 кг/см3:
![]()
Исходный 4,4’-динитродифенилоксид получают в чистейшем виде реакцией п-галоиднитробензола с п-нитрофенолятом щелочных металлов:
![]()
б) Другой предпочтительный метод получения диамина это аммонолиз соответствующего дибромсоединения:
![]()
7. «Упорядоченные» диамины.
Существует ряд диаминов, уникальных в том отношении, что в их молекулах содержатся амидные звенья или гетероциклы. Эти диамины легко реагируют с соответствующими бифункциональными мономерами с образованием большого числа конденсационных полимеров, получивших название «упорядоченные сополимеры». Упорядоченные диамины, используемые для синтеза таких сополимеров, обычно имеют симметричную структуру. Наиболее перспективными из таких диаминов считаются:
N, N’-м-фенилен-бис-(м-аминобензамид):
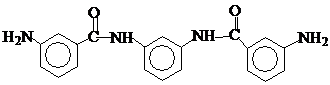
N, N’-бис-(3-аминофенил)изофталамид:
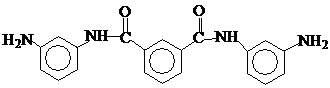
2,5-ьис—(п-аминофенил)-1,3,4-оксадиазол:
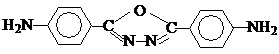
Основными способами получения первых 2-х диаминов является восстановление соответствующих динитросоединений, которые получаются реакцией ароматических диаминов с нитроарилхлоридами или нитроариламинами и ароматическими хлорангидридами:
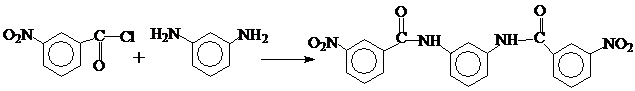
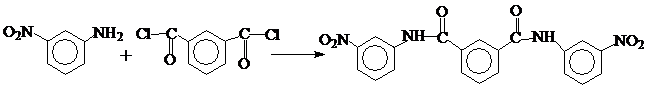
Синтез 2,5-бис-(4-аминофенил)-1,3,4-оксодиазола осуществляют по следующей схеме:
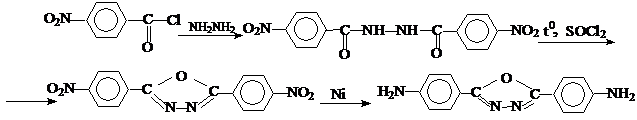
2.6.2. Химические свойства ароматических диаминов
Особняком среди ароматических диаминов стоит о-фенилендиамин в связи с его способностью легко образовывать гетероциклы.
1. Так при диазотировании он дает внутреннее диазоаминосоединение – бензотриазол:
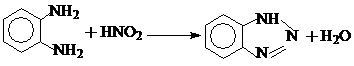
2. Нагревание с карбоновыми кислотами приводит к гетероциклическим амидинам – бензимидазолам:

3. Реакция с α-дикетонами дает хиноксалины:
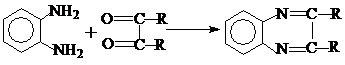
4. Взаимодействием с SO2 получают пиазтиол:
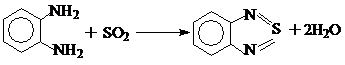
Общие химические свойства ароматических диаминов.
В том, что касается поведения аминогрупп ароматических диаминов, они во многом схожее с реакциями аминогруппы алифатических диаминов.
Это: 1). Образование солей с минеральными кислотами;
2). Реакции ацилирования карбоновыми кислотами их хлорангидридами и ангидридами;
3). Взаимодействие с азотистой кислотой с образованием динитрозопроизводных.
Основные свойства ароматических диаминов выражены значительно слабее, чем у алифатических диаминов, причем наибольшей основностью обладает п-фенилендиамин.
2.6.3. Полимеры на основе ароматических диаминов
Ароматические диамины высокой степени чистоты могут быть использованы для получения линейных высокомолекулярных полиамидов, полиуретанов, полимочевин и полиимидов.
Синтез полиамидов.
Ароматические ПА образуются в условиях низкотемпературной поликонденсации в растворе или на границе раздела фаз. В качестве растворителя используется N, N-диметилацетамид или N-метилпирролидон, в качестве катализатора используют LiCl. В качестве сомономеров используются дихлорангидриды кислот:
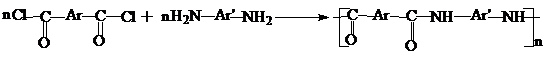
Ароматические ПА могут быть получены также межфазной поликонденсацией при условии, что используемый диамин растворим водной фазе или смачивается ею, а образующийся полимер растворим в органической фазе или набухает в ней.
Высокомолекулярные упорядоченные сополимеры, также как и полимеры на основе бензидина этим методом обычно не получается.
Синтез полиимидов.
Первой стадией получения полиимидов является низкотемпературная поликонденсация (15-75 0С) в среде ДМАА с образованием полиамидокислот. При Т=75 0С наблюдается уменьшение молекулярных весов амидокислот. Путем подбора концентраций мономеров получают обычно 10%-ые растворы полиамидокислот, если раствор при этом является очень вязкой, её разбавляют до 5-7%-ной концентрации. Растворы полимеров хранят в сухих запаянных бутылях при -15 0С. Логарифмическая вязкость таких растворов (0,5%-ных) находятся в пределах 1,5-3,0.
В дальнейшем термической обработкой полиамидокислот получают полиимиды:

Синтез полимочевин.
ПМ получают взаимодействием ароматических диаминов с фосгеном или диизоцианатами. Реакция поликонденсации ароматических диаминов с диизоцианатами проводят в среде апротонных диполярных растворителей при не высоких температурах:

2.7. Бисфенолы
Бисфенолами называются органические соединения, содержащие 2 гидроксильные группы, непосредственно связанные с ароматическим ядром. Из них наибольшее применение находят м-диоксибензол (резорцин), п - диоксибензол (гидрохинон) и ряд более сложных бисфенолов, которые будут рассмотрены ниже.
2.7.1. Получение бисфенолов
1. 2,2-бис-(4-оксифенил)пропан – (диан, бисфенол А).
Все способы получения диана на сегодняшний день основаны на реакции взаимодействия ацетона с фенолом с использованием различных катализаторов.
Разработаны непрерывные в процессе, основанные на катализе HCl в присутствии меркаптанов или без них. Роль меркаптанов заключается в ускорении кислотно-каталитической реакции кетона с фенолом. С этой целью также могут быть использованы и меркаптоалифатические кислоты.
Наиболее хорошим катализатором в непрерывном процессе является нерастворимая сильнокислотная катионообменная смола, например, сополимер стирола и дивинилбензола.
Наилучшим способом получения диана считается конденсация ацетона с большим избытком фенола в присутствии безводного HCl при Т=35-40 0С.
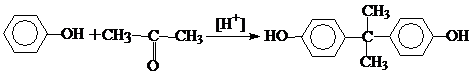
2. 1,1-бис-(4-оксифенол)циклогексан (Бисфенол С).
В основе получения бисфенола С лежит реакция взаимодействия фенола и циклогексанона в присутствии кислых (HCl, H2SO4) и щелочных катализаторов, образование бисфенола С по этим методам идет очень легко:

3. Бис-(4-оксифенил)метан (Бисфенол F).
Основным способом получения бисфенол F является реакция взаимодействия формальдегида с большим избытком (5-кратным) фенола в присутствии конц. НСl:
![]()
4. Фенолфталеин.
Фенолфталеин обычно получают только 1-им способом, а именно взаимодействием фенола с фталевым ангидридом:

В качестве катализатора используют серную кислоту, хлорид цинка, смесь хлорида цинка с серной кислотой и др.
5. 4,4’-диоксибензофенон.
а) щелочное плавление фенолфталеина

б) гидролиз 4,4’-дихлорбензофенона проводят в присутствии меди как катализатора
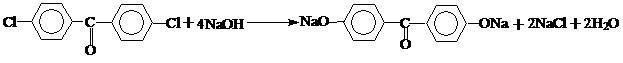
в) следующим способом получения диоксибензофенона является реакция анизолхлорида и анизола, катализируемая иодом с последующим деметилированием образующегося 4,4’-диметоксибензофенона солянокислым пиридином:
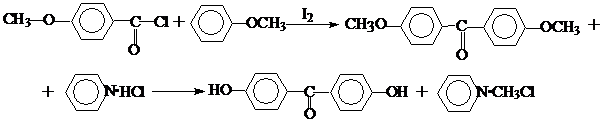
6. 4,4’-диоксидифенилсульфон (Бисфенол S)
а). Гидролиз 4,4’-дихлордифенилсульфона осуществляет щелочью в присутствии окиси меди:
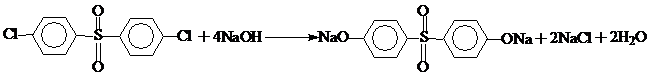 2,4’-дихлордифенилсульфон получают сульфированием хлорбензола. Сульфирование осуществляют смесью серного ангидрида с избытком диэтилсульфата с промежуточным образованием диэтилпиросульфата:
2,4’-дихлордифенилсульфон получают сульфированием хлорбензола. Сульфирование осуществляют смесью серного ангидрида с избытком диэтилсульфата с промежуточным образованием диэтилпиросульфата:
![]()
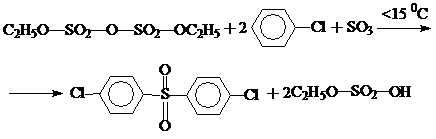
б) вторым способом получения бисоксифенильных соединений является синтез бисфенолов, содержащих серу в более низком валентном состоянии и последующее их окисление.
7. 4,4’-диоксидифенилсулифид и 4,4-диоксидифенилсульфоксил можно получить реакцией фенола с хлористым тионилом
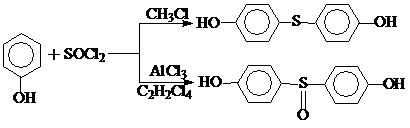
Окисление сульфида осуществляют над бензойной кислотой в СНСl3, а сульфоксид перекисью водорода в уксусной кислоте.
2.7.2. Химические свойства бисфенолов
1. Образование фенолятов.
С щелочами бисфенолы образуют феноляты.
2. С алкилгалогенидами в присутствии акцептора галогенводорода (К2СО3) бисфенолы образуют простые эфиры, которые также образуются при алкилировании фенолятов
![]()
3. Образование сложных эфиров не может быть достигнуто взаимодействием их с кислотами, а только ацелированием их ангидридами или галогенангидридами кислот.
4. Замещение гидроксила на хлор при действии хлорирующих агентов протекает гораздо труднее, чем для спиртов и с плохим выходом.
2.7.3. Полимеры на основе бисфенолов
Эпоксидные полимеры.
Э. п. получают по следующей схеме:
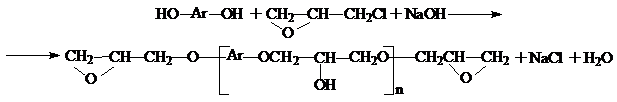
Величина n зависит от количества эпихлоргидрина и при большом избытке приближается к нулю. При уменьшении количества эпихлоргидрина n возрастает, причем, ещё более ВМ полимеры можно получить обработкой данной смолы бисфенолом. Промышленностью выпускаются эпоксидные полимеры с n≤15. Для получения эпоксидных полимеров в основном используется бисфенол А.
Эпоксидные полимеры являются не чем иным, как реакционными преполимерами, конечные изделия из которых получают превращением их в сшитые полимеры путем обработки аминами или ангидридами реагирующими с эпоксидными группами, или этерификации гидроксильных групп жирными кислотами.
Поликарбонаты (ПК).
Получают конденсацией бисфенолов с фосгеном или дифенилкарбонатом:
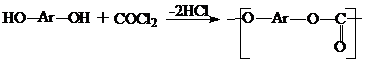
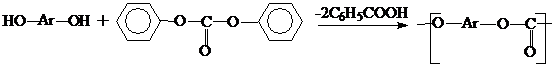
ПК отличаются высокой ударной вязкостью, высокими диэлектрическими характеристиками, прозрачностью, но недостаточной огнестойкостью, но их горючесть можно снизить использованием в качестве бисфенола производных диана – тетрахлордиана. Следует отметить, что и в случае ПК наибольшее применение в качестве бисфенола для их получения находит бисфенол А (диан).
Простые ароматические полиэфиры.
Их получают по 1-ой из следующих 2-х схем:
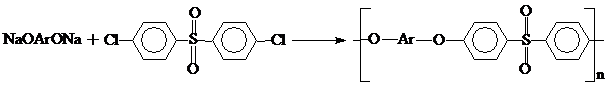
Реакцию проводят в полярных апротонных растворителях, главным образом в ДМСО, при Т<160 0С.
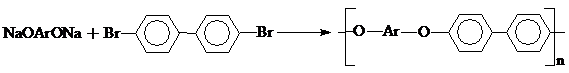
При использовании, как в данном случае, неактивированных ароматических дигалогенидов реакцию ведут в присутствии соли одновалентной меди как катализатора в более жестких условиях. Полиэфир на основе диана и 4,4’- дихлордифенилсульфона известен под названием «полисульфон», представляет собой жесткий прочный термопласт, устойчивый к агрессивным средам с хорошими электрическими характеристиками, прекрасной огнестойкостью.
2.8. Диангидриды тетракарбоновых кислот
2.8.1. Получение диангидродов тетракарбоновых кислот
1. Пирромелитовый ангидрид.
Пиромеллитовый диангидрид - тетрафункциональный мономер, привлекающий наибольшее внимание. Промышленный способ его получения базируется на окислении дурола в присутствии V2О5 в качестве катализатора, который легко гидролизируется в пирромелитовую кислоту.
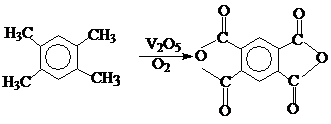
2. Диангидрид 3,3’,4,4’-бензофенонтетракарбоновой кислоты.
Получают конденсацией 2-х молей о-ксилола с молью ацетальдегида до бензофенонтетракарбоновой кислоты, дегидратация которого приводит к диангидриду:
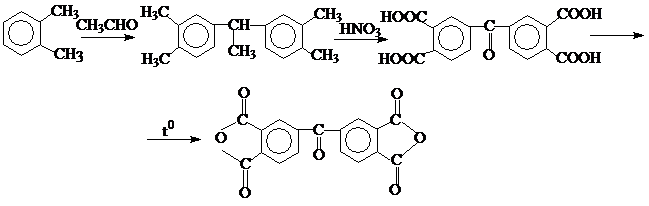
3. Диангидрид 3,3’,4,4’-дифенилтетракарбоновой кислоты.
а). 1-ый способ включает диазотирование о-аминотолуола и последующую обработку продукта реакции цианидом меди. Образующийся при этом 4,4’-дициано-3,3’-диметилдифенил подвергают гидролизу и окислению, приводящему к тетракарбоновой кислоте, которая при нагревании дает диангидрид:
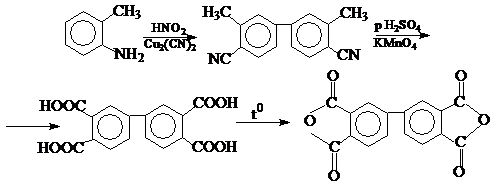
б). Удобный метод получения диангидрида базируется на использовании диметил-4-иодфталата с полученным в присутствии порошкообразной меди тетраметилового эфира 3,3’,4,4’-дифенилтетракарбоновой кислоты. Гидролиз эфира КОН и обработка тетракарбоновой кислоты избытком ацетилхлорида приводит к диангидриду:

4. Диангидрид 1,4,5,8-нафталинтетракарбоновой кислоты (НТКК).
Наиболее удобный способ получения НТКК – окисление пирена в присутствии V2О5 смесью бихромата натрия и серной кислоты:
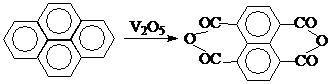
5. Диангидрид 3,3’,4,4’-дифенилсульфонтетракарбоновой кислоты.
Реакция взаимодействия о-ксилола с серной кислотой или п-толуолсульфокислотой приводит к 3,3’,4,4’-тетраметилдифенилсульфону. Его окисление азотной кислотой приводит к 3,3’,4,4’-дифенилсульфонтетракарбоновой кислоте, которая при нагревании с уксусным ангидридом легко превращается в диангидрид:
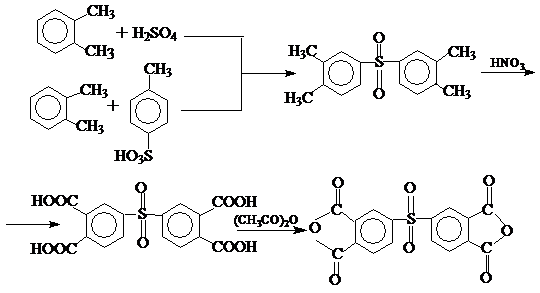
Как диангидрид, так и тетракарбоновая кислота используется в реакциях с диамином.
2.8.2. Химические свойства диангидридов тетракарбоновых кислот
1. При нагревании со спиртами диангидрид присоединяет 2 молекулы спирта с образованием кислых эфиров, которые могут быть превращены в полные эфиры обычной этерификацией в присутствии минеральных кислот:

2. При действии аммиака на диангидриды могут получаться 2 продукта: амидокислоты и имиды. Действие водного раствора аммиака приводит к амидокислотам, а пропускание аммиака над нагретым диангидридом к имидам:

В свою очередь нагревание амидокислот приводит к имидам.
3. Гидролиз. Гидролиз ангидридов приводит к тетракарбоновым кислотам.
Полиимиды
Процесс получения полиимидов из диангидридов и ароматических диаминов 2-хстадийный, с получением полиамидокислоты в растворе (обычно ДМФА) в эквимолекулярных количествах. Полиамидокислоты при н. у. неустойчивы и подвергаются гидролизу при хранении. Поэтому сразу после получения ПАК проводят формование её циклизацией (имидизацией). Обычно эту стадию проводят в инертной среде путем термообработки ПАК при Т>300 0С. В процессе циклизации удаляется остаточный растворитель, а полимер становится неплавким и нерастворимым материалом.
Литература
1. , Сливинский химии и технологии мономеров. Учебное пособие. М.: Наука: МАИК Наука/Интерпериодика, 2002, 696 с.
2. Мономеры и высокомолекулярные соединения. Под ред. , Воронеж, 1974, 99 с.
3. Химия мономеров. М: Изд-во иностранной литературы, 1960, 735 с.
4. , Таланов элементоорганических мономеров и полимеров. Колос, 2011,440 с.
5. Киреев соединения, : Высшая Школа, 2013, 602 с.
6. , , Кашаева в химию полимеров: Учебное пособие. М.: Высшая школа, 2005, 368 с.
7. Тагер -химия полимеров, М., Научный мир, 2007.
8. Химия и физика высокомолекулярных соединений. Учебное пособие. Антонова-, Ильина -во: Московского государ. Открытого унита, 2008 (www. *****).
9. Черный мономеров и сырья для нефтехимического синтеза. Научная монография. 1973.
10. Коршак . Часть 2. М: Изд-во иностранной литературы, 1953, 273 с. Сб. статей.
11. Химия и технология мономеров. Сб. научн. трудов. Отв. ред. . М., ВНИПИМ, 1984, 92 с.
12. Мономеры для термостойких полимеров. Сб. научн. трудов. ДСП-М НИИ ТЭХИМ, 1990, 123 с.
13. Мономеры для поликонденсации. Сб. научн. трудов. ДСП-М НИИ ТЭХИМ, 1989, 196 с.
14. Полимерные реагенты и катализаторы. Пер. с англ. /Под ред. Ферда. М.: Химия, 1991, 256 с.
15. , Савастьянов мономеры и полимеры на их основе. М.: Химия, 1988, 384 с.
16. Шаов образования макромолекул. Конспект лекций.//Учебное пособие. Нальчик, КБГУ, 2006, 83 с.
17. Энциклопедия полимеров, М. Изд. БСЭ, т. т.
18. Мардыкян полимеров. Минск, Изд-во БГУ, 1971, 215 с.
19. , Васнев процессы и полимеры. М.: Наука, 2000, 372 с.
20. Практикум по ВМС. Под ред. . М.: Химия, 1985, 223 с.
Заключение
Курс рассматривает классификацию мономерных веществ для полимеров. Описаны основные способы и методы синтеза исходных мономеров для полимеров. Изложены основные теоретические и технологические особенности получения мономеров полимеризационного и поликондесационного характера. Показано влияние различных факторов (температура, давление, катализатор) на процессы получения мономеров полимеризационного характера. При этом основным сырьем для синтеза мономеров являются природные источники - нефть, газ, уголь и т. д.
Следует отметить, что в пособии рассмотрены наряду с широко используемыми мономерами полимеризационного и поликонденсационного характера и другие мономерные вещества, которые могут быть использованы для получения специальных полимерных материалов.
Несомненно, материалы конспекта вызавят определенный интерес и будут полезны для бакалавров, магистров, аспирантов и специалистов, занимающихся химией высокомолекулярных соединений.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



