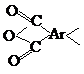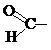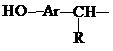На практике используют 3 вида ПВХ:
- винилпласты – жесткие материалы на основе ПВХ, содержащие стабилизирующие добавки и смазывающие вещества, которые выпускаются в виде листов, труб и пленок;
-пластикаты – мягкие материалы на основе стабилизированного и пластифицированного ПВХ, количество пластификатора в которых может достигать 50%. Введение пластификатора увеличивает эластичность и морозостойкость ПВХ (-50 0С). Пластикаты выпускаются в виде гранул, пленок, шлангов.
- пластизоли – это дисперсии эмульсионного ПВХ в жидких пластификаторах – в качестве которых используют диалкилфталаты, сложные эфиры адипиновой, себациновой, фосфорной кислот. Количество пластификаторов составляет от 30 до 80%. Пластизоли используют для получения искусственной кожи, клинки.
ПТФЭ – политетрафторэтилен (тефлон); ПВДФ – поливинилиденфторид.
1.3.Стирол
1.3.1. Получение стирола
Получение стирола сводится к осуществлению следующих реакций:
![]()
Алкилирование бензола этиленом большей частью проводится при атм. давлении, без механического перемешивания, при 90 0С в присутствии безводного хлористого алюминия как катализатора. Расход AlCl3 2,5г на 100г этилбензола.
Другой способ алкилирования бензола состоит в проведении реакции с этиленом в присутствии фосфорной кислоты, нанесенный на кизельгур. Температура реакции не должна превышать 275 0С, т. к. катализатор быстро покрывается коксом. Давление реакции при 63 атм. Соотношение бензол : этилен - 4:1.
Вторую реакцию осуществляют с использованием различных катализаторов при разных условиях.
1. Один из катализаторов дегидрирования состоит в основном из окиси цинка (76-86%) с добавками окиси алюминия (2,3-8%), окиси кальция (4,7-5,1%), окиси магния (0-5%), сульфата калия (2-3%) и хромата калия (2-3%). Пары этилбензола с водяным паром (1/0,8-1/2) подвергают дегидрированию в колонне при Т=6000С.
2. Другим катализатором дегидрирования являются катализаторы N 1707 и N 105, применяемые для дегидрирования бутанов в бутадиены. Дегидрирование также проводится в присутствии водяного пара, который предотвращает коксообразование и одновременно служит для подачи необходимого для реакции тепла. Дегидрирование проводят при Т=625 0С, время пребывания на катализаторе 0,5 сек, выход при однократном проходе 37%.
3. Третий способ по реакции:
![]()
Физические свойства
Стирол – жидкость бесцветная, Ткип=145 0С, Тпл=-30,6 0С и d=0,9021 г/см3.
1.3.2. Химические свойства стирола
Наличие активной олефиновой связи в боковой цепи стирола – главное направление атак на эту цепь
![]()
![]()
Стирол легче, чем олефины, присоединяет спирты:

Однако при нитровании стирола наряду с главным продуктом этой реакции – ω-нитростиролом образуются оба продукта в ядро о- и п - стиролы;



что свидетельствует об электроннооднородном характере виниловой группы.
1. Реакция Дильса-Альдера

Стирол может функционировать в реакции Дильса-Альдера и как диенофил, и как диен. При этом как диеновый компонент он проявляет себя только в реакциях с активным диенофилами (см. выше). При взаимодействии стирола с малеиновым ангидридом на 1-ой стадии образуется промежуточный аддукт циклоприсоединения, который на заключительной стадии претерпевает 2-ое циклоприсоединение по Дильсу-Альдеру и «еновую» реакцию.
1.3.3. Полимеризация стирола и его сополимеры
Атактический ПС получают радикальной полимеризацией стирола в присутствии пероксидных или азосоединений в качестве инициаторов. В промышленности полимеризацию осуществляют в массе, в эмульсии (в воде), реже в суспензии. ММ= тыс. наибольшую ММ и лучший комплекс прочностных характеристик имеет эмульсионный ПС. Марки ПС, полученного полимеризацией в массе, имеют обозначение ПСМ, суспензионные – ПСС, эмульсионные – ПСЭ. Выпускается стабилизированным в виде гранул или порошка.
Сополимеры стирола
1. Ударопрочный полистирол (УПС) – продукт привитой сополимеризации стирола с бутадиеновым или бутадиенстирольным каучуком. Процесс сополимеризации с каучуком проводят в растворе стирола в присутствии пероксидных инициаторов. Молекулярная масса равна 70-100 тыс. При этом одновременно проходят гомополимеризация стирола и привитая сополимеризация стирола с каучуком. Доля сополимера около 15%. Марочный ассортимент определяется способом получения и назначением УПС. При полимеризации в массе буквенное обозначение марки – УПМ, при суспензионной – УПС.
УПС можно считать композиционным, содержащим матрицу жесткого полистирола (ММ=70-100 тыс.) с частицами каучука размером 1-5 мкм, окруженными тонким слоем привитого сополимера.
2. Бутадиен-стирольные каучуки – статистические сополимеры бутадиена и стирола (СКС) или α-метилстирола (СКМС) с содержанием последних 21-25%. На 50% и более бутадиен присоединяется в трансконфигурации, остальное в конфигурации 1,4-цис и 1,2. Получают СКС в основном методом эмульсионной сополимеризации при 50 или 5 0С. Каучуки с содержанием стирола 21-25% обозначаются как CRC-30 или СКМС-30. Выпускаются каучуки с 8-10% стирола (CRC-10) с повышенной морозостойкостью или с 40-50% стирола (CRC-50) с повышенной жесткостью. ММ (СКС)=150-400тыс. Применяются как каучуки общего назначения.
1.4. Акрилонитрил
Акрилонитрил – прозрачная жидкость с удушливым запахом, кипящая при Т=77,3 0С. Он быстро полимеризуется, но может быть стабилизирован добавлением олеата меди, диоксидифенила и других ингибиторов.
1.4.1. Получение акрилонитрила
1. Промышленное производство.
Сырьем для производства акрилонитрила является жидкая окись этилена и синильная кислота, процесс проводят в водной среде в присутствии диэтиламина и NаОН как катализатор. Реакция протекает в 2 стадии:


Дегитратацию образующегося нитрила оксипропановой кислоты проводят каталитически в жидкой фазе при 200-280 0С или в газовой фазе над активной окисью алюминия. Выход акрилонитрила после отделения от воды и перегонки на 2-ой стадии 75-78%. Выход этиленциангидрина на 1-ой стадии достигает 90%.
2. Присоединение синильной кислоты к ацетилену (метод Курца)
![]()
Процесс получения акрилонитрила по этому методу протекает гладко. Работу ведут в присутствии раствора хлористой меди (I) – Сu2Cl2 и хлорида аммония, слабо подкисленного соляной кислотой, соотношение Сu2Cl2:NH4Cl=1:0,8; рН=3,5. При температуре реакции 75 0С промышленный выход достигает 85%.
3. Окисление 1-аминопропена-2 (аллиламина). Катализатор карбид кремния, на который нанесен 1% серебра.
![]()
Процесс примечателен тем, что в этом случае отпадает необходимость использования синильной кислоты.
4. Действие цианидов щелочных металлов на этиленхлоргидрин.

1.4.2. Химические свойства акрилонитрила
Акрилонитрил – соединение, обладающее высокой реакционной способностью, которое присоединяется ко всем соединениям, имеющим подвижный атом водорода. Иначе говоря способность цианогруппы активировать кратную углерод-углеродную связь делает акрилонитрил активным соединением по отношению к нуклеофильным атакам. Именно благодаря этому акрилонитрил легко присоединяет в щелочной среде самые разнообразные нуклеофилы – спирты, тиолы, аминосоединения и т. д. Эти реакции называются реакциями цианоэтилирования.




2. Акрилонитрил легко вступает в реакцию Дильса-Альдера в качестве диенофила:

3. Восстановление акрилонитрила. При восстановлении акрилонитрила на свинцовом катоде в присутствии в качестве восстановителя LiAlH4 образуется аллиламины:
![]()
![]()
4. Гидролиз акрилонитрила:

1.4.3. Полимеризация акрилонитрила и его сополимеры
1. Полиакрилонитрил получают радикальной полимеризацией акрилонитрила в присутствии пероксидных или азоинициаторов в атмосфере азота. Полимеризацию проводят в водной эмульсии и редко в массе. Выпускают в виде белого порошка или лаков. Молекулярная масса равна 35-100тыс. Полиакрилонитрил (ПАН) – жесткоцепной неплавкий полимер с плотностью равной г/м3. При Т=220-230 0С ПАН разлагается с выделением большого количества газообразных продуктов (в основном аммиак), при Т=270 0С выделяется НСN. Используется в основном для изготовления волокон из раствора.
Сополимеры акрилонитрила.
Значительно чаще акрилонитрил используется для сополимеризации с бутадиеном и бутадиенстирольным каучуком для получения эластомеров.
1. Бутадиен-нитрильные каучуки – статистические сополимеры бутадиена с акрилонитрилом. Бутадиен присоединяется преимущественно в положении 1,4-транс, содержание 1,2-структуры не превышает 10%.

Получают эмульсионной полимеризацией. Марочный ассортимент синтетического каучука нитрильного (СКН) определяется содержанием акрилонитрилов, которое в разных сортах составляет 17-20, 27-30, 36-40, иногда до 50%, а соответствующие марки каучука СКН-18, СКН-26. СКН-40, СКН-50. ММ=200-300тыс. применяются как каучуки спецназначения.
2. АБС-пластики – продукт привитой сополимеризации стирола с акрилонитрилом и бутадиеновым или бутадиенстирольным каучуком. Процесс сополимеризации мономеров с каучуком проводят в эмульсии в присутствии пероксидных инициаторов. Одновременно протекает сополимеризация стирола с акрилонитрилом. В конечном продукте содержится 65% стирола, 20% акрилонитрила и 15% каучука.
Глава 2. Мономеры для поликонденсации
Поликонденсация, наряду с полимеризацией является одним из методов синтеза полимеров и представляет собой ступенчатый процесс. Как и в цепных процессах образования макромолекулы, строение и реакционная способность мономеров играет решающую роль для реакций поликонденсации. При этом основными в поликонденсационных процессах являются понятия реакционного центра, функциональной группы и функциональности.
Реакционным центром называют активную часть молекулы (обычно один атом), непосредственно участвующую в химическом взаимодействии.
Функциональной группой называют часть молекулы мономера, определяющую его принадлежность к тому или иному классу соединений и имеющую характерную реакционную способность. Функциональная группа определяет поведение мономера в химических реакциях. Так, в функциональных группах – NH2 и ОН реакционными центрами являются атомы водорода. В принципе в зависимости от условий и в разных реакциях одна и та же функциональная группа может иметь различные реакционные центры. Так, при нейтрализации реакционным центром в группе – СООН является атом водорода, а при реакции со спиртом – атом кислорода группы – ОН.
Важной характеристикой мономеров является их функциональное число реакционных центров (или функциональной группы) в одной молекуле. От значения функциональности зависит возможность образования линейных, разветвленных или трехмерных макромолекул. При поликонденсации бифункциональных мономеров образуются линейные цепи, если же один или оба исходных мономера не может отражать его истинной функциональности в конкретных условиях процесса, различают возможную, практическую и относительную функциональности мономера. Возможная функциональность Фв – это общее число активных групп в молекуле мономера, для данного соединения эта величина постоянная, определяемая его химическим строением. Практическая функциональность Фпр – число функциональных групп, способных вступать в реакции в данных условиях (Т, концентрация, наличие катализатора). Эта величина может менятся в зависимости от условий процесса и от строения мономера. Отношение Фв/Фпр называют онтосительной функциональностью Фотн.
Формирование функциональной группы может происходить и в процессе синтеза аолимера методом поликонденсации, как в случае образования фенолформальдегидных полимеров из фенола и формальдегида, которые с точки зрения функциональности непригодны для синтеза полимеров как малофункциональными соединениями.
2.1. Классификация мономеров. Сомономеры.
Гомо - и гетерополиконденсация
Применяемые для синтеза методом поликонденсации мономеры разделяют на 2 группы: мономеры для гомополиконденсации и мономеры для гетерополиконденсации.
Основные группы поликонденсационных мономеров
Отличительный признак | Мономеры для | |||
гомополиконденсации | гетерополиконденсации | |||
Тип А-А | Тип А-В | Тип А-А | Тип А-В | |
Возможность взаимодействия между реакционными центрами одной молекулы мономеров | да | да | нет | нет |
Строение реакционных центров молекулы мономера | одинаковое | разное | одинаковое | Разное |
Мономеры | Гликоль, силоксандиолы | Оксикислоты, аминокислоты | Диамины, дикарбоновые кислоты | аминоспирты |
Мономеры для поликонденсации – это вещества, содержащие в молекуле одинаковые или различные функциональные группы, способные к взаимодействию друг с другом, например:
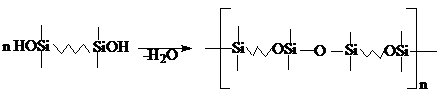
Для гетерополиконденсации используют мономеры, в отдельности не способные к образованию полимеров, но образующие их при взаимодействии друг с другом, например:
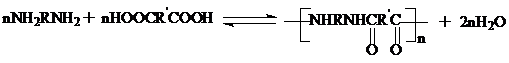
Мономеры для гетерополиконденсации часто называют сомономерами.
Примеры функциональных групп в мономерах и типы полимеров, образующие при поликонденсации
Функиональные группы | Низкомолекулярный продукт реакции | Образующаяся связь | Тип образующегося полимера | |
первая | вторая | |||
-ОН | -COOH | H2O |
| Сложный полиэфир |
-ОН | ROOC- | ROH | То же | То же |
-ОН | -OH | H2O | -О- | Простой полиэфир |
-OH | -Cl | HCl | То же | То же |
-NH2 | HOOC- | H2O |
| Полиамид |
-NH2 |
| HCl | То же | То же |
-NH2 |
| HCl |
| Полиуретан |
-NH2 | Cl- | HCl | -NH- | Полиамин |
-NH2 | O=C=N- | Нет |
| Полимочевина |
-OH | O=C=N- | Нет |
| Полиуретан |
-ONa | Cl-ArSO2- | NaCl |
| Ароматический полисульфон |
-R-Cl | NaS- | NaCl | -R-S- | Полисульфид |
-SH | H2C=CH- | Нет | -CH2CH2S- | Полисульфид |
|
| H2O |
| Полисилоксан |
-NH2 |
| нет |
| полиамидокислота |
-NH2 |
| H2O | -N=CH- | полиазометин |
|
| H2O |
| Фенолформальдегидный полимер |
2.2. Алифатические дикарбоновые кислоты

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |