Кислоты, в которых 2 карбоновые группы разделены из шести или более углеродных атомов (n>5) в большинстве случаев не обладают какими либо специфическими свойствами – в этих случаях свойства карбоновых групп более или менее независимы друг от друга. Если же карбоксильные группы расположены ближе одна к другой, то возможности их взаимодействия увеличиваются. С точки зрения особенности химических свойств интерес представляет прежде всего кислоты такого типа.
кислота | формула | Тпл | Константа диссоциации в воде при 25 0С | Константа диссоциации уксусной кислоты | |
К1 | К2 | ||||
Щавелевая | НООС-СООН | 189,0 | 5,9×10-2 | 6,4×10-5 | 1,5×10-5 |
Малоновая | НООС-СН2-СООН | 135,6 | 1,49×10-3 | 2,03×10-6 | - |
Янтарная | НООС-(СН2)2-СООН | 185,0 | 6,89×10-5 | 2,47×10-6 | - |
Глутаровая | НООС-(СН2)3-СООН | 97,5 | 4,55×10-5 | 3,89×10-6 | - |
Адипиновая | НООС-(СН2)4-СООН | 153,0 | 3,71×10-5 | 3,87×10-6 | - |
Пимелиновая | НООС-(СН2)5-СООН | 103,0 | 3,09×10-5 | 3,77×10-6 | - |
пробковая | НООС-(СН2)6-СООН | 140,0 | 2,99×10-5 | 2,5×10-6 | - |
Можно ожидать, что индуктивный эффект одной карбоновой группы приведет к увеличению кислотных свойств другой, и в соответствии с ожидаемым (из таблицы) результатом очевидно, что сила дикарбоновых кислот (на основании первой константы диссоциации К1) выше, чем сила уксусной кислоты и уменьшается при увеличении расстояния между карбоксильными группами. Вторая константа диссоциации К2 меньше чем Кукс, по той причине, что отрыв протона оказывается более трудным из-за электростатического притяжения к расположенному поблизости карбоксилат – аниону.
Температуры плавления в гомологическом ряду двухосновных кислот выше у кислот с четным числом углеродных атомов, чем у кислот с нечетным числом, при этом с удлинением углеродной цепи разница постепенно уменьшается.
2Основные методы получения алифатических
дикарбоновых кислот
а) Щавелевая кислота
1. в промышленности её получают из оксалата натрия, которую в свою очередь получают нагреванием формиата натрия в щелочной среде:
![]()
2. Окисление этиленгликоля
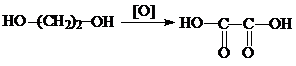
3. Гидролиз дициана. При гидролизе водой в кислой среде дициана образуется щавелевая кислота
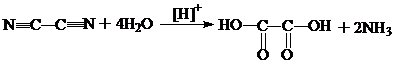
б) Малоновая кислота
Её получают в промышленных масшабах через её мононитрил цианоуксусную кислоту, обработкой на 1-ой стадии цианидом натрия с последующим гидролизом в кислой среде:
![]()
![]()
в) Янтарная кислота
Синтез её может быть осуществлен несколькими способами.
1. Промышленный способ получения состоит в гидрировании малеиновой кислоты (цис) или фумаровой кислоты над платиновым или никелевым катализатором:
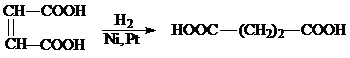
2. Янтарную кислоту можно получить из дихлорэтана обработкой её на 1-ой стадии цианидом натрия и гидролизом в кислой среде образующегося динитрила:
![]()
![]()
3. Синтез Конрада
Синтез Конрада состоит в получении янтарной кислоты через натриймалоновый эфир:

При действии на натриймалоновый эфир моногалойдных производных этилового эфира уксусной кислоты с последующими стадиями гидролиза и декарбоксилирования получают янтарную кислоту.
г) Дикарбоновые кислоты с числом метиленовых групп > 3-х.
Дикарбоновые кислоты с числом метиленовых групп > 3-х получают с использованием ряда общих способов.
1. Наиболее обычным способом синтеза таких карбоновых кислот является окисление циклических кетонов, например:
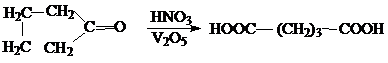
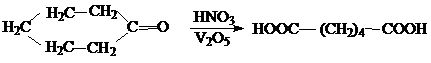
2. Для четных и нечетных членов ряда дикарбоновых кислот существуют разные способы получения с использованием тетрахлоралканов:
четные члены ряда:
![]()
![]()
Нечетные члены ряда
![]()
![]()
![]()
Требуемые тетрахлоралканы получают реакцией этилена с четыреххлористым углеродом по реакции теломеризации, которая заключается в присоединении ССl4 и ССl3Br к олефинам:
![]()
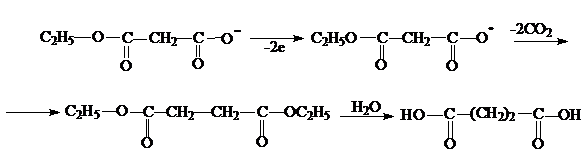
3. Кислоты с четным числом углеродных атомов также могут быть получены по реакции Кольбе, электролизом солей эфиров низших двухосновных килот:
2.2.2. Химические свойства алифатических дикарбоновых кислот
а). Щавелевая кислота.
Щавелевая кислота одна из самых сильных карбоновых кислот, далеко превосходящая по силе свои гомологи. Кристаллизуется с 2-мя молекулами воды с образованием гидрата с tпл=101,5 0С.
1). Нагревание.
При нагревании до 160-180 0С щавелевая кислота декарбоксилируется:
![]()
2) Щавелевая кислота легко окисляется сильными окислителями, например, КМnO4 в кислой среде, давая СО2 и Н2О.
3) При нагревании с Н2SO4 происходит разложение щавелевой кислоты на СО, СО2 и Н2О.
б). Малоновая килота.
Малоновая кислота также особенностями, резко отличающих её от других членов ряда.
1). Нагревание.
При нагревании до 140-180 0С малоновая кислота гладко декарбоксилируется, превращаясь в уксусную кислоту с выделением СО2:
![]()
2). Взаимодествие с галогенами.
Водороды метиленового звена в м. к. находятся в α-положении по отношению к 2-м карбоксилам, обладают более высокой подвижностью, чем в одноосновных кислотах. При взаимодействии галогенов с малоновой кислотой в зависимости от условий процесса замещение может происходить так одного, так и обоих атом водорода.
3). Взаимодействие с альдегидами.
Малоновая кислота легко вступает в реакции конденсации с альдегидами в присутствии основных катализаторов. При этом в зависимости от условий и соотношения реагентов с молекулой альдегида реагирует одна или две молекулы кислоты:
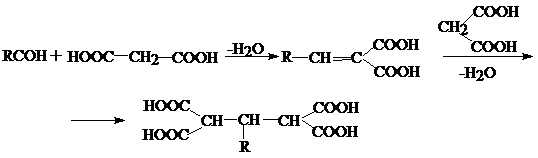
Очевидно, что этот путь может быть использован также для синтеза двухосновных кислот и для синтеза одноосновных непредельных кислот.
4). Обезвоживание над Р2О5.
При этом образуется недоокись углерода:
![]()
Которую легко можно перевести в малоновую кислоту или её эфир действием соответственно воды и спиртов.
5). Синтез этилового эфира малоновой килоты (малоновый эфир).
![]()
При действии на этиловый эфир малоновой кислоты металлического натрия один, а при избытке натрия и оба метиленовых водорода замещаются на натрий, с образованием натриймалонового эфира (динатриймалонового эфира), который находит широкое применение в органическом синтезе. Так при действии на него галоидных алкилов или других галоидопроизводных происходит замещение натрия на алкил или другой радикал, связанный с галоидом. Так, можно получать гомологи и разнообразно замещенные малоновые эфиры, а после их гидролиза - кислоты (синтез Конрада). Так, в частности, синтез Конрада является важным способом синтеза двухосновных карбоновых кислот с числом метиленовых групп ≥2 (синтез янтарной кислоты и выше). Например, синтез глутаровой кислоты и других двухосновных кислот:
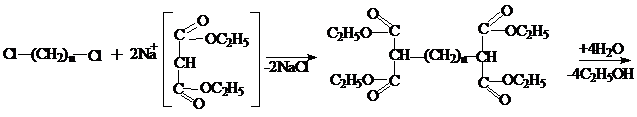
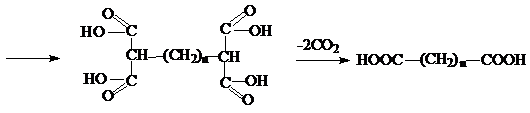
в) Янтарная кислота.
Янтарная кислота отличается от предыдущих членов ряда образованием циклических ангидридов и имидов. При длительном нагревании или при обезвоживании уксусным ангидридом из янтарной кислоты образуется янтарный ангидрид:
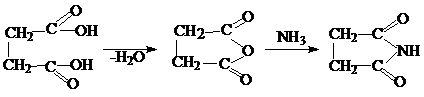 (сукциимид)
(сукциимид)
г) Глутаровая кислота.
Она также образует циклический ангидрид:
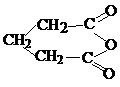
д) Дикарбоновые кислоты с числом метиленовых групп > 3 не образуют циклических ангидридов. Путем каталитической реакции над окисью тория или марганца двухосновные кислоты могут быть превращены в 5- или 6-членные алициклические кетоны:
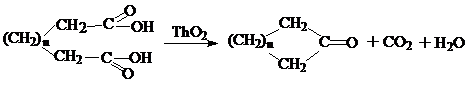
Общие химические реакции дикарбоновых кислот.
Для двухосновных дикарбоновых кислот в принципе характерными являются все химические реакции, присущие карбоксильной группе одноосновных кислот. Это:
1. реакции со щелочами;
2. этерефикации в кислой среде;
3. получение хлорангидридов при действии хлорирующих агентов: РСl5, PCl3, SOCl2, SO2Cl2, COCl2;
4. реакции с аммиаком (аминами); и т. д.
2.2.3. Получение непредельных одноосновных
карбоновых кислот
Из таких кислот простейшими и важнейшими, имеющими большое техническое значение, является акриловая кислота: СН2=СН-СООН и α-метакриловая (или метакриловая кислота): СН2=С(СН3)-СООН. При этом принято проводить аналогию между такими сопряженными системами и системами типа С=С-С=С. Например, и для тех и других характерны как 1,2-так и 1,4-присоединение.
Получение
а) акриловую кислоту можно получать разными способами:
1. Из этиленхлоргидрина или окиси этилена обработкой их цианидом калия или цианистой кислотой соответственно с последующим гидролизом образующегося нитрила β-оксипропионовой кислоты и одновременной дегидратацией этого нитрила конц. Н2SO4:
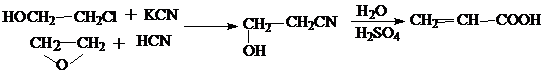
2. Гидролизом акрилонитрила в присутствии Н2SO4:
![]()
3. Обработкой ацетилена моноокисью углерода и с водой в присутствии в качестве катализатора тетракарбониланикеля.
![]()
4. Присоединением фосгена к этилену в присутствии AlCl3:
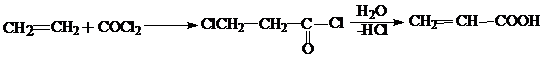
б) метакриловую кислоту обычно синтезируют из ацетона и синильной кислоты по следующей схеме:
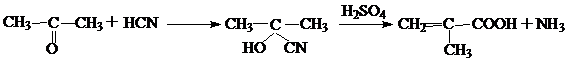
В полимерной промышленности применение в основном находит не сама метакриловая кислота, а её метиловый эфир – метилметакрилат, которую получают из ацетона, циангидрина и метанола в присутствии серной кислоты:
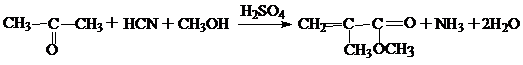
2.2.4. Физические и химические свойства непредельных карбоновых кислот
При комнатной температуре акриловая кислота и метакриловая кислота являются жидкостями с Тпл=12,3 0С и 16 0С соответственно. Константа диссоциации в воде при 25 0С – 5,6∙10-5 и 2,03∙10-5 соответственно.
1. Непредельные кислоты легко присоединяют по двойной углерод - углеродной связи молекулу воды в кислой среде, галойдводороды и аммиак. Присоединение при этом проходит против правила Марковникова, что легко объясняется влиянием электроноакцепторной карбонильной группы:
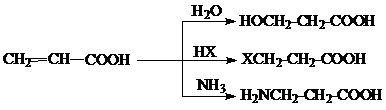
2. К числу наиболее важных реакций непредельных кислот и их производных (например, эфиров) является присоединение ацетоуксусного и малонового эфиров в сильнощелочной среде (реакция Михаэля):

3. Реакция Дильса – Альдера:
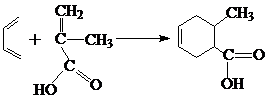
Аналогично реагируют эфиры акриловой и метакриловой кислот. Реакции протекают при комнатной температуре или легком нагревании.
2.2.5. Полимеризация непредельных карбоновых кислот
Полимеризацию акриловой кислоты и метакриловой кислоты осуществляют в промышленных условиях в присутствии перекиси бензоила или водорастворимых перекисных соединений эмульсионным или суспензионным методом.
Полиметилметакрилат (ПММА) получают радикальной полимеризацией метилметакрилата в присутствии перекисных катализаторов. Молекулярная масса (ММ) синтезированного ПММА – 20-30 тыс. полимеризацией в массе в присутствии небольших количеств пластификатора (фталаты, фосфаты) (5-15%) получают органические стекла, содержащие также остаточный мономер.
Пластификатор добавляется для уменьшения хрупкости. Органические стекла имеют ММ≤600 тыс. ПММА – атактический аморфный полимер с высокой степенью разветвленности, плотностью (1,18-1,2) и Тст=100-110 0С, что обусловлено значительным межмолекулярным взаимодействием.
В нормальных условиях ПММА является материалом общетехнического назначения. Основные его достоинства: высокая прозрачность в том числе и для УФ - и ИК-лучей и достаточно высокие прочностные характеристики; используется для изготовления светотехнических изделий, стекла (например авиационного).
2.3. Алифатические и алициклические диамины
Из различных алифатических диаминов в синтезе поликонденсационных полимеров наибольшее распространение получили нормальные α,ω – диамины, алициклические диамины, ксилилендиамин и пиперазин.
2.3.1. Получение алифатических диаминов.
α, ω - нормальные диамины
1. Восстановление динитрилов
При восстановлении нормальных алифатических α, ω – динитрилов легко образуются соответствующие диамины:
![]()
Восстановление можно проводить с применением химических реагентов, например гидридов металлов, и в частности литийалюминийагидрида или натрием в спирте.
Обычно восстановление проводят используя в качестве катализаторов гидрирования Ni, Pt, Pd при повышенных t и Р (промышленный способ производства).
2. Аммонолиз дигалогенсодержащих соединений.
Алифатические диамины можно получать реакцией соответствующих дигалогенов с аммиаком. Из алкилгалогенов наиболее реакционноспособны алкилйодиды, а наименее алкилхлориды, но из соображений экономии в промышленности наиболее часто используют алкилхлориды:
![]()
Для уменьшения роли побочных реакций берут избыток аммиака. Реакцию проводят при Т>100 0С при повышенном давлении. Диамины при этом получаются в виде хлоргидратов и для выделения их в виде свободного основания проводят нейтрализацию сильными щелочами.
Для ускорения реакций можно использовать различные катализаторы, например Аl, MgO.
3. Аминирование гликолей.
Реакцию проводят при нагревании под давлением до высоких температур (>200 0С) в присутствии в качестве катализатора никеля:
![]()
К хорошим результатам приводит и использование в качестве катализатора рутения на угле за исключением этиленгликоля, бутандиола-1,4 и пентандиола-1,5 из-за склонности их к образованию циклических соединений.
4. Гофмановское разложение диамидов.
При реакции алифатических диамидов с гипобромитом натрия (NaOH+Br2) образуются α, ω- алифатические диамины с числом углеродных атомов, меньше чем у исходного диамида на 2:
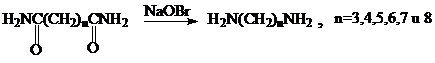
5. Реакция Шмидта.
Алифатические диамины легко получают из соответствующих дикарбоновых кислот, содержащих на 2 атома углерода больше, чем требуемый диамин. Реакцию осуществляют путем взаимодействия азометоводородной кислоты, образующийся при действии H2SO4 на азид натрия, с дикарбоновой кислотой:
![]()
При получении диаминов по реакции Шмидта выходы выше, чем по реакции Гофмана, но реакция Шмидта используют значительно реже в связи с опасностью работы с аммиаком (токсичность и взрывоопасность).
6. Синтез по Габриэлю
Алифатические диамины образуются с очень хорошим выходом в результате реакции фталимида калия гидролизом промежуточного алкилдиамина:
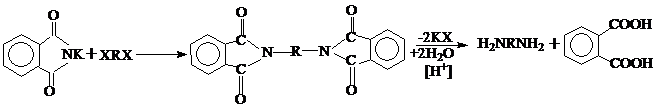
2.3.2. Получение алициклических диаминов
Основным способом получения алициклических диаминов, а именно 1,3 и 1,4-диаминоциклогексанов, метилдиаминоциклогексанов и бис-(n-аминоциклогексил)метана является гидрирование соответствующих ароматических соединений в присутствии в качестве катализатора двуокиси рутения под давлением при высоких температурах (>200 0С). При этом гидрирование аминозамещенных производных бензола, как правило, протекает намного труднее, чем гидрирование незамещенного ядра.
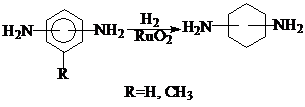
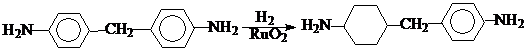
В качестве исходных веществ для получения диаминоциклогексанов можно использовать соответствующие динитробензолы или нитроанилины. Причем гидрирование можно осуществлять прямо в одну стадию в присутствии в качестве катализатора RuO2 или Ru/C.
Так, предпочтительным методом получения 1,3-диаминоциклогексана и 1,4-диаминоциклогексана является гидрирование м-нитробензола и п-нитроанилина соответственно.
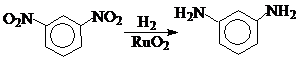
![]()
1-метил-2,4- и 1-метил-2,6-диаминоциклогексан можно получить в результате нитрования толуола (образуется смесь 2,4- и 2,6-динитробензола, суспензионным гидрированием которых, получают толуилендиамины и соответственно метилдиаминоциклоны)
м - и п - Ксилилендиамин и их получение
Т. к. м - и п - ксилилендиамины в своем составе имеют бензольные ядра, их иногда относят к ряду ароматических диаминов.
Продукты коксохимической и нефтехимической промышленности м - и п - ксилилендиамины – выделяют из смеси о-, п - и м-изомеров. Существует два способа получения ксилилендиаминов.
1. Получение из изофталевой и терефталевой кислот.
Способ синтеза ксилилендиаминов из изофталевой кислоты или терефталевой кислоты одинаково хорошо применим для получения м-ксилилендиамина и п-ксилилендиамина или их смеси; все зависит от того какая кислота используется в качестве исходного соединения. Процесс является двухстадийным с образованием на первой стадии соответствующих фталонитрилов, восстановлением которых получают ксилилендиамины гидрированием:
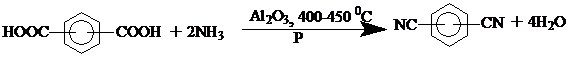
На 2-ой стадии проводят гидрирование фталонитрилов при Т=100-160 0С и Р=140-350 атм. в присутствии никеля.
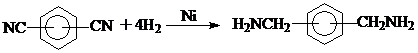
2. Окислительный аммонолиз.
О. а. представляет собой общий способ синтеза ароматических нитрилов из соответствующих алкилбензолов. Он заключается в газофазной реакции алкилзамещенных бензолов, в данном случае м - и п-ксилолов с аммиаком и кислородом в присутствии катализатора при повышенных температурах. а. представляет собой смесь ванадата аммония, окиси мышьяка, сульфата калия и воды в качестве растворителя.
Пиперазин и их получение
Пиперазин и его алкилзамещенные гомологи представляют собой циклические вторичные диамины. Т. к. по своей структуре они сильно отличаются от алифатических и алициклических диаминов, общие методы их синтеза не применимы для получения пиперазина. Из пиперазинов наибольшее применение находят сам пиперазин, 2-метилпиперазин, 2,5- и 2,6-диметилпиперазины.
Пиперазин
1. Получают взаимодействием моноэтаноламина с водородом и аммиаком, пропуская реакционную смесь через неподвижный слой катализатора из сплава никеля и хрома при Т=220-230 0С и Р=200 атм.:
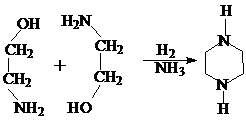
2. Пиперазин можно получить димеризацией этиленимина
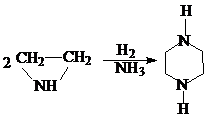
2-метилпиперазин
Получают циклизацией Т-(2-окипропил)этилдиамина в присутствии катализатора гидрирования – дегидрирования
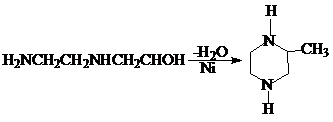
При этом существует непрерывный процесс синтеза 2-МП при повышенном давлении периодический процесс при нормальном давлении.
2,5-диметилпиперазин.
Широкое применение как способ получения 2,5-ДМП находит только реакция бимолекулярного циклоаминирования изопропаноламина:
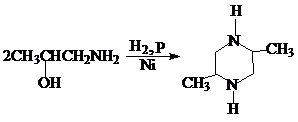
Реакция циклизации проводится под давлением водорода в присутствии никеля как катализатор.
2,6-диметилпиперазиин
Получают конденсацией диизопропаноламина с аммиаком в присутствии никелевого или кобальтового катализатора при Т=170-200 0С под давлением водорода при двухкратном избытке NH3.
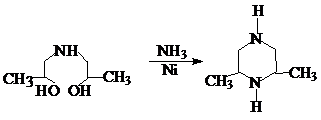
Химические свойства алифатических и алициклических
диаминов
1. Диамины как основания образуют соли даже со столь слабыми кислотами, как угольная, сероводород и синильная:
![]()
2. Алифатические диамины ацилируются карбоновыми кислотами, ангидридами кислот, хлорангидридами кислот, сложными эфирами:
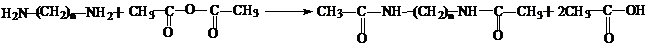
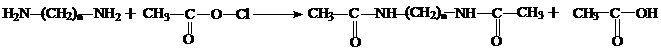
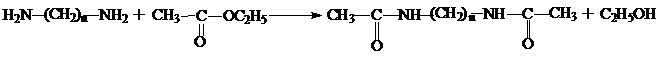
3. Диамины с 2-мя атомами водорода у азота (первичные) реагируют с азотистой кислотой, превращая их в спирты:
![]()
Пиперазины реагируют иначе, когда происходит нитрование по азоту с образованием 1,4-динитропиперпазина:
![]()
4. Первичные диамины при нагревании с хлороформом в спиртовой щелочи образуют диизонитрилы:
![]()
Изонитрилы в отличие от нитрилов ядовиты и имеют неприятный запах. Поэтому реакция их образования – чувствительная качественная реакция, как на первичные амины, так и диамины.
5. С хлористым тионилом первичные диамины образуют сульфин-имины:
![]()
2.3.4. Полимеры на основе алифатических и алициклических
диаминов
Поликонденсация в расплаве является промышленным методом получения полиамидов. Процесс проводят нагреванием стехиометрических количеств диамина и карбоновой кислоты выше Тпл образующегося полиамида. Эта Т обычно выше 200 0С. молекулярный вес регулируют изменением продолжительности реакции. В качестве катализаторов обычно применяют окислы и карбонаты щелочных металлов. Полученные таким образом полиамиды (ПА) пригодны для изготовления пленок и волокон формованием из расплава или раствора.
Другим способом синтеза полиамида является межфазная поликонденсация. Полимер получают на границе раздела 2-х растворов реакций хлорангидрида дикарбоновой кислоты в растворе не смешивающегося с водой органического растворителя с раствором диамина в воде. В качестве акцептора выделяющегося НСl применяются гидроксиды и карбонаты щелочных металлов. В отличии от поликонденсации в расплаве межфазную поликонденсацию проводят в открытой аппаратуре при температуре <40 0С. реакция заканчивается обычно за несколько минут.
Термин «найлон», первоначально введенный фирмой Дю Pont для изготовления полиамида на основе гексаметилендиамина и адипиновой кислоты (другое название ПА-6,6) в настоящее время относят ко всем синтетическим полиамидам с волокнообразующими свойствами, получающимися поликондесацией диаминов и дикарбоновых кислот (ПА-6,6, ПА-6,себациновая кислота), гомополиконденсацией м-аминокарбоновых кислот (ПА-7,9,11) и полиамида, образующихся полимеризацией циклических амидов – лактамов (ПА-3,4,5,6,8,12).
Промышленное значение имеют также ПА на основе ксилилендиамина и дикарбоновых кислот, у которых модули упругости выше, чем у обычных найлонов. ПА на основе пиперазина и себациновой кислоты обладает жесткостью и водостойкостью. Волокна ПА из бис-(п-аминоциклогексил)метана и дикарбоновых кислот с 8-12 атомами углерода похоже на шелк.
2.4. Диолы и бисхлорформиаты
2.4.1. Получение α-диолов
Среди различных α – диолов лишь две привлекают большой интерес как мономеры. Первый из них этиленгликоль, который выпускается в большом масштабе, чем все другие гликоли, вместе взятые, второй – пропиленгликоль, на долю которого приходится большая часть производства других гликолей.
1. Хотя известны различные методы получения указанных гликолей, единственным важным методом получения является гидролиз соответствующих эпоксидов, которые можно легко получить дегидрохлорированием галогенгидринов или окислением олефинов:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



