Рис. 3. Реограми плину дослідних зразків
Введення даної речовини до складу препарату дозволить спростити технологію виробництва, підвищить антимікробну дію препарату та споживчі характеристики лікарського засобу.
Дослідження фармакологічної активності засобів, що володіють вираженою протизапальною активністю передбачає вивчення здатності препарату протидіяти запальним процесам. Дослідження протизапальної активності мазей проводили на моделі термічного запалення стопи у мишей. До складу модельних зразків мазі на макрогольній основі (таблиця 6) крім диференційної кількості ГЕКЯ та п’ятикратної кількості розчинника – етанолу 70%, було додано 5% бензокаїну.
Для проведення експерименту тварини були сформовані у групи по 6 тварин у кожній: перша – контрольна патологія, друга – дослідна група, якій на обпечену лапу наносили «Зразок №1», третя – дослідна група, якій на лапу наносили «Зразок №2», четвертій групі на лапу наносили «Зразок №3» та п’ятій – «Зразок №4».
Таблиця 6
Склад дослідних зразків, г
Інгредієнти* | Зразок №1 | Зразок №2 | Зразок №3 | Зразок №4 |
ГЕКЯ | 0,50 | 0,75 | 1,00 | 2,00 |
Етанол 70% | 2,50 | 3,75 | 5,00 | 10,00 |
Бензокаїн | 5,00 | 5,00 | 5,00 | 5,00 |
Макрогол-400 | 73,60 | 72,40 | 71,20 | 66,40 |
Макрогол-1500 | 18,40 | 18,10 | 17,80 | 16,60 |
* Склад наведений на 100,00 г препарату
Результати експерименту наведені в табл. 7.
Згідно отриманих даних (табл. 7) можна зробити висновок, що максимальну протизапальну дію матиме мазь, до складу якої включено 1% ГЕКЯ.
Таблиця 7
Вплив концентрації ГЕКЯ на протизапальну активність
Групи тварин | n | Різниця між стопами в масі, мг | Протизапальна активність, % |
Контрольна патологія | 6 | 57,33±5,31 | - |
Зразок № 1 | 6 | 50,67±5,26 | 11,62 |
Зразок №2 | 6 | 48,17±6,52 | 15,98 |
Зразок № 3 | 6 | 24,50±4,31* | 57,26 |
Зразок № 4 | 6 | 34,40±6,42* | 39,40 |
Примітка. n =5, р£0,05 – відхилення показника достовірне в порівнянні з контролем.
Ефективну концентрацію анестезуючої речовини визначали за методикою на моделі анестезії ока кроля. За даними досліджень при підвищенні концентрації бензокаїну від 1 до 5 % швидкість появи анестезії та термін її існування значно підвищується. Але, слід відзначити, що підвищення концентрації анестетика вище за 5% не призводить до значного покращення анестезуючої дії препарату, але може призвести до негативного впливу на організм людини завдяки високої концентрації в препараті. Тому, ефективною концентрацією бензокаїну в складі розроблюваного препарату слід вважати 5%.
Таким чином, на підставі проведених досліджень пропонується склад мазі під умовною назвою «Фраксид»:
Густий екстракт кори ясеня 1,00 г
Бензокаїн 5,00 г
Спирт 70% 5,00 г
Макрогол 400 71,20 г
Макрогол 1500 17,80 г
100,00 г
Одним з головних питань в розробці нових лікарських засобів є підбір оптимальних режимів промислового виробництва препарату з урахуванням температури та часу ведення процесу, параметрів роботи обладнання, черговістю введення речовин, що входять до складу препарату та ін. Першочерговим питанням стало дослідження з визначення граничної температури ведення процесу виробництва препарату. Дослідження проводили за допомогою термогравіметричного аналізу речовин: ГЕКЯ, бензокаїну, основи. Також проводилося термогравіметричне дослідження суміші всіх діючих речовин з основою в рівних частинах, задля визначення відповідності теплових ефектів окремих речовин тепловому ефекту суміші.
Згідно отриманим даним критичною температурою для компонентів є 90 оС. При цій температурі відбувається втрата маси ГЕКЯ. Таким чином, на підставі проведених термогравіметричних досліджень можна стверджувати про можливість проведення процесів приготування мазі при стандартних температурах виробництва (до 70оС).
До складу мазі «Фраксид» входить дві діючи речовини – ГЕКЯ та бензокаїн. Першочерговість введення кожної з них повинно бути обґрунтовано та нести під собою мету отримання препарату з оптимальними споживчими властивостями.
В зв’язку з цим, нами було виготовлено зразки мазі за трьома технологіями, та визначено реологічні якості цих дослідних зразків за допомогою моделюємого реологічного оптимуму намазуваємості та реологічного оптимуму консистенції.
За першою технологією бензокаїн розчиняли в рівній кількості спирту етилового 70%. Після повного розчинення бензокаїну отриману суміш вводили до відваженої наважки ГЕКЯ Після повного розчинення ГЕКЯ в суміші бензокаїну та спирту етилового, концентрат діючих речовин вводили при температурі 50 оС в попередньо виготовлену макрогольну основу та гомогенізували.
За другою технологією ГЕКЯ розчиняли в спирті етиловому 70%. Після повного розчинення ГЕКЯ в отриману суміш вводили бензокаїн. Після повного розчинення бензокаїну в суміші ГЕКЯ та спирту етилового, концентрат діючих речовин вводили при температурі 50 оС в попередньо виготовлену макрогольну основу та гомогенізували.
За третьою технологією ГЕКЯ та бензокаїн розчиняли в спирті етиловому 70%. Надалі концентрат діючих речовин вводили при температурі 50 оС в попередньо виготовлену макрогольну основу та гомогенізували.
Отримані препарати за різними технологіями виробництва закладали на зберігання при температурі 15-25 оС на 10 днів, після чого визначали їх структурно-механічні властивості. Дані досліджень наведені на рисунках 4 та 5.
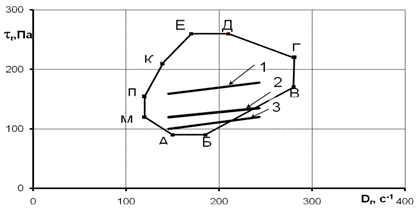
Рис. 4 Обмежені реограми плину для зразків № 1-3
Обмежена реограма плину зразку №1, на відміну від прямих зразків №2 та №3 займає майже центральне місце на площі АБВГДКЛМ (рисунок 4).
Згідно даних рисунку 5, найбільшу петлю гістерезису та максимальне влучання в модельований оптимум консистенції має також зразок №1. Проаналізувавши дані рисунків 4 та 5 можна зробити висновок, що кращі структурно-механічні властивості має зразок, виготовлений за першою технологією.
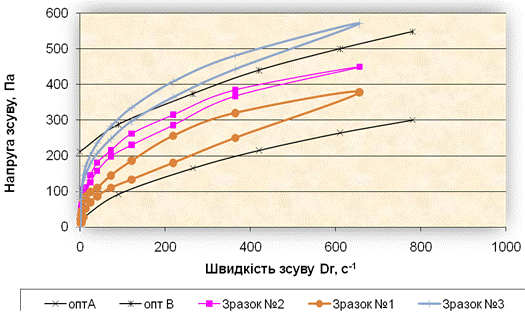
Рис. 5. Реограми плину для зразків № 1-3
На підставі проведених досліджень нами було розроблено технологію виробництва мазі «Фраксид» за наступною схемою (рисунок 6).
У четвертому розділі «Розробка методик аналізу та фізико-хімічні дослідження мазі «Фраксид»» наведені результати ідентифікації та кількісного визначення діючих речовин у препараті, досліджено його стабільність та фармако-технологічні властивості. Дослідження виконані на кафедрі фармацевтичної хімії НФаУ під керівництвом доцента
Важливим аспектом впровадження нових лікарських засобів є розробка методик якісного та кількісного визначення складових препарату. У відповідності до ДФУ мазі на макрогольній основі повинні контролюватися за такими показниками: опис, ідентифікація, однорідність, маса вмісту контейнера, мікробіологічна чистота та кількісне визначення.
Одним з головних показників якості препарату є стабільність його фізико-хімічних, фармакологічних та споживчих властивостей. Нами було проведено дослідження препарату розфасованого в туби алюмінієві та банки з жовтогарячого скла протягом 2 років при різних температурних режимах (15,0-25,0 оС та 8,0-15,0 оС). Кожні шість місяців препарат аналізували за такими показниками як ідентифікація, кількісне визначення бензокаїну, суми гідроксикоричних кислот (метод спектрофотометрії), рН водного розчину, визначали органолептичні показники мазі та мікробіологічну чистоту. Експериментально доведена стабільність препарату протягом 24 місяців зберігання. Отримані дані досліджень представлено в таблиці 8. Всі показники, що зазначені в таблиці були використані при розробці МКЯ на препарат.
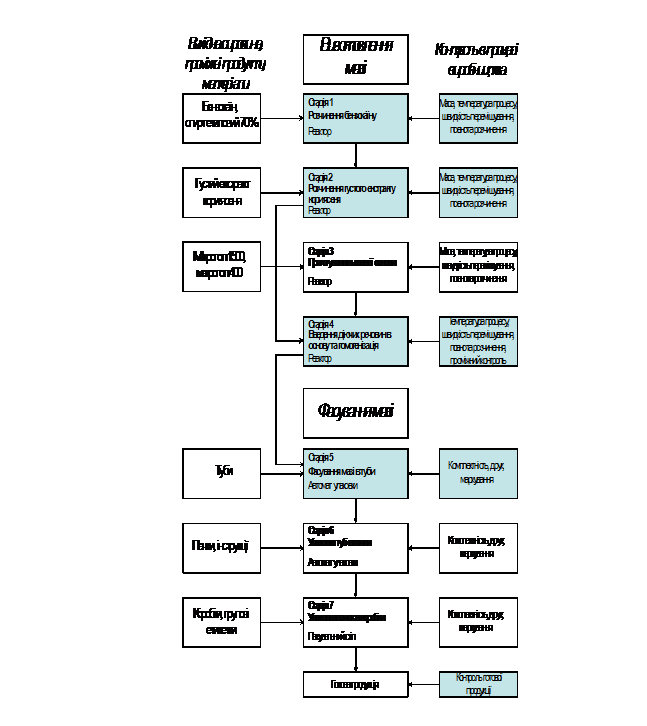
Рис. 6. Технологічна схема виробництва мазі «Фраксид»
На підставі отриманих результатів розроблено рекомендації щодо вибору температури зберігання та матеріалу первинного пакування – туби алюмінієві. За ступенем мікробної контамінації, визначення якого проводили на кафедрі біотехнології НФаУ під керівництвом доцента Стрілець О. П., препарат відповідає вимогам ДФУ для препаратів місцевого призначення. В препараті не виявлені бактерії родин Enterobacteriaceae, Staphylococcus aureus, Pseudomonas aeruginosa. Загальна кількість бактерій в 1 г препарату не перевищила 10, грибів - 25.
У п’ятому розділі «Вивчення фармакологічних властивостей мазі „Фраксид”» наведено результати фармакологічних досліджень, які виконані на базі ЦНДЛ НФаУ під керівництвом професора Яковлевої і доклінічні дослідження дозволили встановити, що мазь проявляє виражену протизапальну, місцевоанестезуючу та антимікробну активність. Препарат належить до відносно нешкідливих, а при вивчення хронічної токсичності субхронічному досліді в умовнотерапевтичній дозі було доведено про відсутність будь-якого токсичного впливу мазі "Фраксид" на життєво важливі органи і системи піддослідних тварин.
ЗАГАЛЬНІ ВИСНОВКИ
1. Розроблено науково обґрунтований склад, раціональну технологію та методи контролю якості мазі для лікування ран на І фазі ранового процесу з густим екстрактом кори ясеня (ГЕКЯ).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


