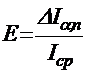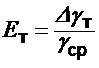Таблица 2.
№ опыта | εi рад/с2 |
MiН•м |
Iiкг•м2 | Icр кг•м2 | ΔIi кг•м2 | (ΔIi)2 (кг×м2 )2 |
Sкг•м2 | ΔIα,n кг•м2 |
| ctg α кг•м2 |
1 | ||||||||||
2 | ||||||||||
3 | ||||||||||
4 | ||||||||||
5 |
Лабораторная работа № 2
Определение отношения теплоемкостей 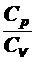 воздуха
воздуха
по методу Клемана – Дезорма
Приборы и принадлежности: Прибор Клемана - Дезорма, нагнетатель воздуха.
Цель работы: Определение отношения теплоемкостей 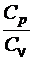 воздуха и сравнение полученного значения с теоретическим.
воздуха и сравнение полученного значения с теоретическим.
1. Теория метода.
Согласно молекулярно-кинетической теории молярные теплоемкости идеального газа при постоянном давлении Cp и постоянном объеме Сv зависят только от числа степеней свободы молекулы и выражаются формулами:
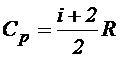
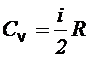
где i - число степеней свободы молекул газа (для одноатомного газа i=3, для двухатомного газа i=5, для многоатомного газа i=6); R - универсальная газовая постоянная.
Отношение этих теплоемкостей равно:
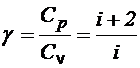 (1)
(1)
Безразмерная величина g, которая называется показателем адиабаты или коэффициентом Пуассона, является важной характеристикой газа. В частности, она входит в уравнение Пуассона для адиабатического процесса:
![]() (2)
(2)
процесса, который происходит без теплообмена с окружающей средой. Практически все быстро протекающие процессы близки к адиабатическому.
Метод экспериментального нахождения значения g, предложенный Клеманом и Дезормом, основан на последовательном переводе газа из состояния 1 в состояние 2 путем адиабатического расширения, а затем из состояния 2 в состояние 3 путем изохорного нагрева (рис.1). Эти процессы на диаграмме p – Т представлены кривыми 1 - 2 и 2 – 3 соответственно.
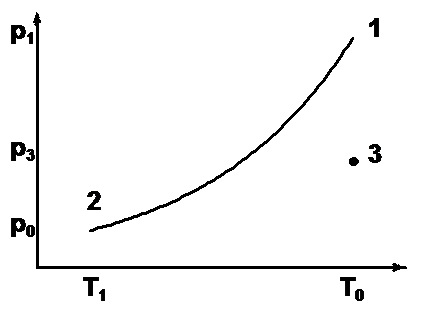
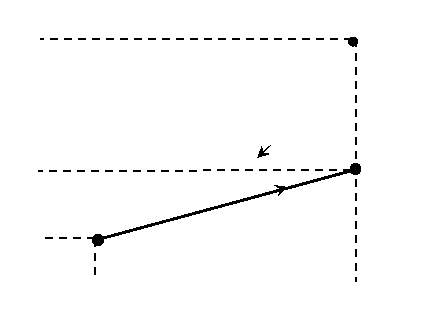

Рис.1. Графики газовых процессов в методе определения
отношения ![]() .
.
В сосуд при комнатной температуре Т0 нагнетается некоторое количество воздуха, в результате чего в сосуде установится давление р1, которое будет превышать атмосферное давление р0 на величину, равную Dр1 . Таким образом, начальное состояние воздуха 1 характеризуется параметрами Т0 и р1 (рис.1).
Если теперь быстро открыть и закрыть сосуд с воздухом, произойдет адиабатическое расширение воздуха (процесс 1 – 2), в результате которого воздух охладится, а его давление уравняется с атмосферным. Таким образом, состояние 2 будет характеризоваться новыми параметрами Т1 и р0 .
Через некоторое время воздух, находясь в закрытом сосуде, нагреется вследствие теплообмена с окружающей средой и перейдет из состояния 2 в состояние 3 (изохорный процесс) с параметрами Т0 и р3 . Давление р3 будет превышать атмосферное давление р0 на величину, равную Dр3 .
Используя уравнение Пуассона (2) и уравнение Менделеева-
Клапейрона p×V = (m/M)×R×T, получим следующее соотношение между параметрами состояния воздуха 1 и 2 (рис.1):
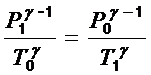 (3)
(3)
Отсюда: 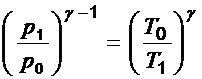 (4)
(4)
Применяя закон Шарля для изохорного процесса, запишем следующее соотношение между параметрами состояния воздуха 2 и 3:
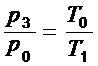 (5)
(5)
Из равенств (4) и (5) следует:
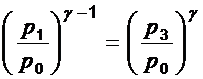 (6)
(6)
После логарифмирования уравнения (6) получим выражение для определения значения g :
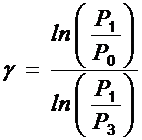 (7)
(7)
Принимая во внимание, что р1 = р0 + Dр1 , а р3 = р0 + Dр3 , формула (7) примет следующий вид:
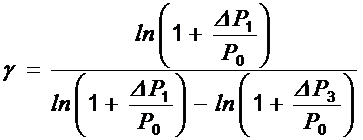 (8)
(8)
Величины Dр1/р0 и Dр3/р0 много меньше единицы. Тогда, используя приближенную формулу ln(1+x)=x, справедливую для малых значений х, получим:
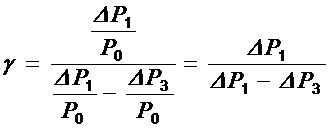 (9)
(9)
В данной лабораторной работе избыточные давления воздуха в сосуде Dр1 и Dр3 измеряются манометром (U- образной трубкой, заполненной подкрашенной водой) как разность уровней воды в его коленах. Заменяя Dр1 и Dр3 соответственно на r×g×h1 и r×g×h3 и сокращая на r×g, получим простую рабочую формулу для вычисления значения g для воздуха:
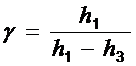 (10)
(10)
Таким образом, для определения отношения теплоемкостей воздуха 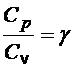 достаточно осуществить процесс 1 – 2 – 3 (рис.1) и при этом измерить только показания U- образного манометра в состояниях воздуха 1 и 3.
достаточно осуществить процесс 1 – 2 – 3 (рис.1) и при этом измерить только показания U- образного манометра в состояниях воздуха 1 и 3.
2. Устройство установки.
Установка Клемана – Дезорма (рис.2) состоит из стеклянного сосуда, в верхней части которого находится трехходовой кран, нагнетателя воздуха и водяного манометра. При определенных позициях крана можно соединить сосуд с окружающей атмосферой или нагнетателем воздуха, а также можно герметизировать сосуд. Манометр представляет собой U- образную трубку, заполненную подкрашенной водой, и шкалу с делениями, по которой проводится отсчет перепада давлений воздуха в сосуде.

Рис.2. Установка Клемана-Дезорма.
3. Порядок выполнения работы и обработки результатов измерений.
1. Повернуть кран в положение, при котором сосуд соединен с нагнетателем воздуха.
2. Накачать в баллон воздух так, чтобы на манометре установилась разность давлений 15-20 см.
3. Выждать 1-2 минуты, чтобы давление воздуха в баллоне полностью установилось.
4. Определить по шкале манометра разность уровней столба жидкости в обоих коленах h1 и занести это показание в табл.1.
5. Выполнить адиабатическое расширение воздуха. Для этого следует быстро открыть кран (при этом сосуд будет соединен с окружающей атмосферой) и тотчас же закрыть его.
6. Выждать 1-2 мин., необходимых для изохорного нагрева газа в сосуде до комнатной температуры, после чего определить по шкале манометра разность уровней столба жидкости в обоих коленах h3. Показание занести в табл.1.
7. Опыт (пункты 1-6) повторить 5-8 раз.
Таблица 1.
№ | h1 см | h3 см | γi | γср | Δγi | (Δγi)2 | S | Δga,n | Δgт |
|
1 | ||||||||||
2 | ||||||||||
… | ||||||||||
… | ||||||||||
9 |
8. Для каждого опыта рассчитать значение gi по формуле (10).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |