9. Вычислить среднее арифметическое значение коэффициента Пуассона γср (результат занести в табл.1).
10. Найти абсолютные погрешности Δγi для всех опытов (данные занести в табл.1).
11. Возвести в квадрат все значения Δγi (данные занести в табл.1).
12. Вычислить среднюю квадратичную погрешность среднего арифметического значения коэффициента Пуассона по формуле:
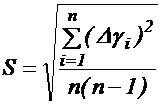
13. По табл.1 (стр.6) найти значение коэффициента Стьюдента ![]() (n - число опытов; a - доверительная вероятность, которую принимаем равной 0,95), после чего вычислить доверительный интервал Dga,n по формуле:
(n - число опытов; a - доверительная вероятность, которую принимаем равной 0,95), после чего вычислить доверительный интервал Dga,n по формуле:
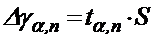
Результат занести в табл.1.
14. После округления величин Dga,n и gср записать окончательный результат измерений в общепринятом виде:
g = gср ± Dga,n
При этом обязательно указать значения α и n.
15. По формуле (1) вычислить теоретическое значение gт , после чего найти абсолютное отклонение (Δgт = gт - γср ) и относительное отклонение (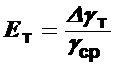 ) экспериментального значения коэффициента Пуассона от теоретического значения (данные занести в табл.1).
) экспериментального значения коэффициента Пуассона от теоретического значения (данные занести в табл.1).
Лабораторная работа
(Компьютерный вариант)
Определение отношения теплоемкостей 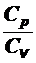 воздуха
воздуха
по методу Клемана – Дезорма
Цель работы: Определение отношения теплоемкостей ![]() воздуха и сравнение полученного значения с теоретическим.
воздуха и сравнение полученного значения с теоретическим.
1. Теория метода.
Согласно молекулярно-кинетической теории молярные теплоемкости идеального газа при постоянном давлении Cp и постоянном объеме Сv зависят только от числа степеней свободы молекулы и выражаются формулами:
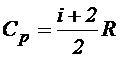
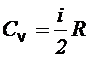
где i - число степеней свободы молекул газа (для одноатомного газа i=3, для двухатомного газа i=5, для многоатомного газа i=6);
R - универсальная газовая постоянная.
Отношение этих теплоемкостей равно:
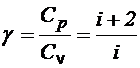 (1)
(1)
Безразмерная величина g, которая называется показателем адиабаты или коэффициентом Пуассона, является важной характеристикой газа. В частности, она входит в уравнение Пуассона для адиабатического процесса:
![]() (2)
(2)
процесса, который происходит без теплообмена с окружающей средой. Практически все быстро протекающие процессы близки к адиабатическому.
Метод экспериментального нахождения значения g, предложенный Клеманом и Дезормом, основан на последовательном переводе газа из состояния 1 в состояние 2 путем адиабатического расширения, а затем из состояния 2 в состояние 3 путем изохорного нагрева (рис.1). Эти процессы на диаграмме p – Т представлены кривыми 1 - 2 и 2 – 3 соответственно.
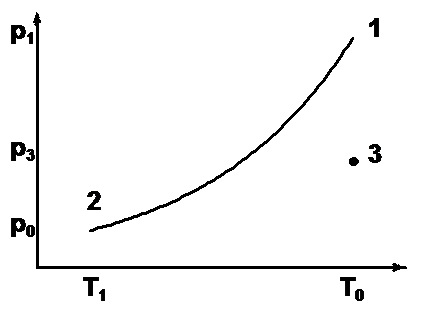
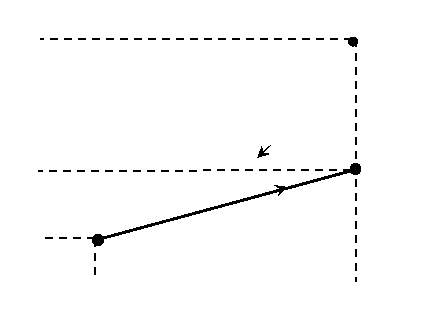

Рис.1. Графики газовых процессов в методе определения
отношения ![]() .
.
В сосуд при комнатной температуре Т0 нагнетается некоторое количество воздуха, в результате чего в сосуде установится давление р1, которое будет превышать атмосферное давление р0 на величину, равную Dр1 . Таким образом, начальное состояние воздуха 1 характеризуется параметрами Т0 и р1 (рис.1).
Если теперь быстро открыть и закрыть сосуд с воздухом, произойдет адиабатическое расширение воздуха (процесс 1 – 2), в результате которого воздух охладится, а его давление уравняется с атмосферным. Таким образом, состояние 2 будет характеризоваться новыми параметрами Т1 и р0 .
Через некоторое время воздух, находясь в закрытом сосуде, нагреется вследствие теплообмена с окружающей средой и перейдет из состояния 2 в состояние 3 (изохорный процесс) с параметрами Т0 и р3 . Давление р3 будет превышать атмосферное давление р0 на величину, равную Dр3 .
Используя уравнение Пуассона (2) и уравнение Менделеева-
Клапейрона p×V = (m/M)×R×T, получим следующее соотношение между параметрами состояния воздуха 1 и 2 (рис.1):
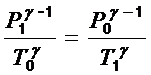 (3)
(3)
Отсюда: 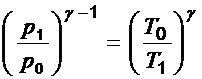 (4)
(4)
Применяя закон Шарля для изохорного процесса, запишем следующее соотношение между параметрами состояния воздуха 2 и 3:
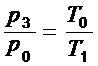 (5)
(5)
Из равенств (4) и (5) следует:
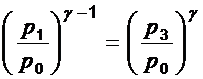 (6)
(6)
После логарифмирования уравнения (6) получим выражение для определения значения g :
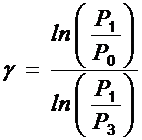 (7)
(7)
Принимая во внимание, что р1 = р0 + Dр1 , а р3 = р0 + Dр3 , формула (7) примет следующий вид:
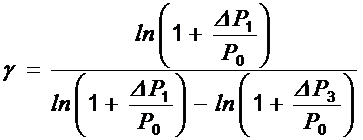 (8)
(8)
Величины Dр1/р0 и Dр3/р0 много меньше единицы. Тогда, используя приближенную формулу ln(1+x)=x, справедливую для малых значений х, получим:
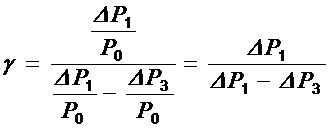 (9)
(9)
В данной лабораторной работе избыточные давления воздуха в сосуде Dр1 и Dр3 измеряются манометром (U- образной трубкой, заполненной подкрашенной водой) как разность уровней воды в его коленах. Заменяя Dр1 и Dр3 соответственно на r×g×h1 и r×g×h3 и сокращая на r×g, получим простую рабочую формулу для вычисления значения g для воздуха:
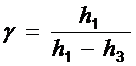 (10)
(10)
Таким образом, для определения отношения теплоемкостей воздуха 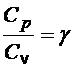 достаточно осуществить процесс 1 – 2 – 3 (рис.1) и при этом измерить только показания U- образного манометра в состояниях воздуха 1 и 3.
достаточно осуществить процесс 1 – 2 – 3 (рис.1) и при этом измерить только показания U- образного манометра в состояниях воздуха 1 и 3.
2. Устройство установки.
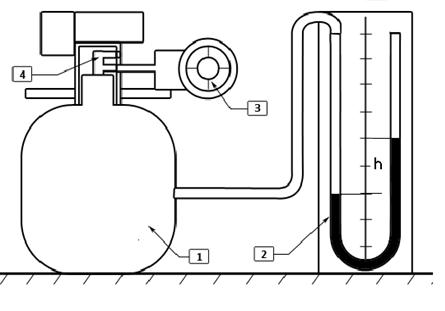
Рис.2. Установка Клемана-Дезорма.
1 – сосуд; 2 – манометр; 3 – микрокомпрессор; 4 – поршень
Прибор состоит из стеклянного сосуда, закрытого поршнем, который может перемещаться с помощью электромагнита, микрокомпрессора для нагнетания воздуха в баллон и манометра, соединенного трубкой с баллоном и предназначенного для измерения давления.
Закачивание воздуха в сосуд проводится с помощью микрокомпрессора, который включается кнопкой, расположенной на нижней панели. Остановка микрокомпрессора происходит автоматически после достижения определенного давления в сосуде.
Выпускание газа из сосуда проводится кнопкой «Напуск». При этом поршень в горловине сосуда с помощью электромагнита переводится в положение, при котором сосуд сообщается с внешней атмосферой. Через 1 секунду поршень автоматически возвращается в прежнее положение, обеспечивая герметизацию сосуда.
Манометр состоит из U образной трубки, заполненной подкрашенной водой, и шкалы с делениями, по которой проводится отсчет перепада давлений.
3. Порядок выполнения работы и обработки результатов измерений.
1. После появления на экране заставки щелкнуть «мышью» по надписи «Эксперимент».
2. Для накачки воздуха в сосуд включить микрокомпрессор, для чего нажать кнопку «Вкл1» на нижней панели под надписью «Микрокомпрессор».
3. После прекращения работы микрокомпрессора через 10-20 с (это время необходимо для охлаждения воздуха в сосуде до комнатной температуры) определить по шкале манометра разность уровней столба жидкости в обоих коленах h1 и занести это показание в табл.1.
4. Выполнить адиабатическое расширение воздуха, для чего следует нажать кнопку «Напуск» на нижней панели. При этом поршень в горловине баллона переместится в положение, при котором отверстия в поршне и баллоне совпадут, т. е. сосуд будет соединен с окружающей атмосферой. Спустя 1 с поршень автоматически вернется в прежнее положение и сосуд загерметизируется.
5. Выждать 10-20 с, необходимых для изохорного нагрева воздуха в сосуде до комнатной температуры, после чего определить по шкале манометра разность уровней столба жидкости в обоих коленах h3. Показание занести в табл.1.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



