Сегодня мы начнём разбирать новый материал с воспоминания основных расчётных формул, которые использовали при вычислениях по химической формуле вещества. Для этого я вам приготовила специальные бланки, где вы внесёте свои ответы в течении 5 минут. Постарайтесь работать самостоятельно, проверяя себя и свою память.
Каждому ученику выдаётся бланк – кластер для внесения ответов. Кластер каждый ученик заполняет сам, а затем 2 минуты обсуждает результаты своей работы с соседним учеником по парте. После этого в течении 6 минут результаты работы обсуждаются совместно с учителем, а учащиеся класса вносят поправки в графу «дополнения, исправления».
Заполните таблицу
вопросы | ответы | дополнения и исправления |
| Запишите обозначения: А) молярная масса Б) количество вещества В) объем газа Г) масса вещества Д) число структурных частиц | А) Б) В) Г) Д) | |
| Составьте формулы для вычисления количества вещества, используя: А) массу вещества Б) объем газа В) число структурных частиц | А) Б) В) | |
3. Укажите числовое значение А) молярного объема Б) числа Авогадро | А) Б) | |
4. Напишите единицы измерения: А) количества вещества Б) молярной массы В) молярного объема | А) Б) В) | |
5.Что означают коэффициенты урав- нений химических реакций в макромире? |
IV. Изложение нового материала. (25мин)
1) Вы уже умеете производить вычисления по химической формуле вещества. А теперь начнём учиться производить вычисления с помощью химического уравнения. Делать это будем на конкретном примере.
Запись на доске и в тетрадях учащихся
Пример: Вычислите массу воды, которая образуется при сжигании 8г водорода.
m(H2O)-? Дано: m(H 2 )=8г M(H2)=2 г/моль M(H2O)=18 г/моль | Решение: 1. Составляем уравнение 8г m-? 2H2 + O2= 2 H2O 2 моль 2 моль |
Находим количество вещества, масса которого известна:
n (H2)= ![]() =
=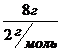 =4моль
=4моль
3. Находим количество вещества, масса которого неизвестна:
n (H2): n (H2O)=2:2; n (H2)= n (H2O); n (H2O)=4 моль
4. Находим неизвестную массу:
m(H2O) =n*M =4 моль*18 г/моль =72г
Ответ: образуется 72г воды.
То, что у вас, ребята, оказалось подчёркнутым, является основными шагами при решении задач, т. е. её план или алгоритм. Ещё раз проговорить алгоритм решения.
2) После разбора типовой задачи учащиеся класса решают аналогичную задачу в тетрадях, получая карточку – задание, составленное по принципу самоконтроля. Это своеобразные карточки, где на одной стороне листа написано условие задачи, а на другой - решение. Таким образом, учащиеся уже самостоятельно проверяют себя, насколько они усвоили материал.
Вариант 5. Какая масса серной кислоты получится при взаимодействии оксида серы VI массой 32г с водой? SO3 + H2O = H2SO4 | Найти: m(H2SO4)-? Дано: m(SО3)=32г M(SО3)= 80 г/моль M(H2SO4)= 98 г/моль | Решение: 1. 32г m-? SO3 + H2O = H2SO4 1 моль 1 моль 2.n (SO3)= 32 г : 80 г/ моль = 0,4 моль по уравнению реакции n (SO3): n (H2SO4)=1:1 n (H2SO4 ) = n (SO3)= 0,4 моль 5. m(H2SO4)= 0,4моль* 98 г/моль=39,2 г Ответ:39,2г |
3) Мы сейчас разобрали задачу, где коэффициенты веществ, используемых при решении, были равны. А как быть, если коэффициенты будут разными?
Запись на доске и в тетрадях учащихся
2А + 3В = А2В3 n (А) : n (В) = 2 : 3 n (А) = 2* n (В) : 3
V. Закрепление изученного материала, сообщение домашнего задания. (5мин)
Итак, сегодня на уроке мы начали выполнять большую и сложную работу по формированию умения производить различные вычисления с использованием уравнения химической реакции.
Вопросы учащимся:
Сколько этапов – шагов в решении подобных задач? На каком этапе решения используется уравнение химической реакции? Что определяют с помощью уравнения химической реакции? Как определить количество вещества, массу которого надо определить?Домашнее задание (заранее написано на доске):
Выучить план решения задач; решить задачу: Найти массу оксида серы IV, который образуется при взаимодействии 4,8г серы с кислородом. S + O2= SO2
Приложение
Урок по химии 8 класс
Химические свойства кислот в свете электролитической диссоциации
Цели урока.
Образовательные:
· актуализировать знания о составе и свойствах кислот;
- продолжить знакомство с основными химическими свойствами кислот в свете электролитической диссоциации.
Развивающие: (совершенствование у учащихся)
- умения составлять уравнения химических реакций с участием кислот в молекулярном и ионном виде; умения предсказывать химические свойства кислот; умения работать с реактивами и оборудованием; умения работать с текстом учебника, выделять главное, анализировать, формулировать выводы;
- навыков аналитической мыслительной деятельности; навыков познавательной деятельности; навыков самоорганизации, самоконтроля и самооценки при выполнении работы.
Воспитательные: (развитие у учащихся навыков)
- аккуратности, внимательности, точности в выполнении работы; настойчивости в достижении цели, в доведении начатого до конца; ответственности к выполнению полученного задания; умения работать в парах.
Оборудование. Реактивы.
Бланки для внесения ответов при составлении кластера, инструктивные карточки для проведения лабораторных опытов, карточки – задания для закрепления полученных знаний, учебники Химия-8 2008, пластины для проведения лабораторных опытов, шпатель, р-р гидроксида натрия, р-р сульфата меди II, р-р соляной кислоты, оксид кальция, р-р азотной кислоты, р-р серной кислоты, р-р карбоната натрия.
Структура урока
по технологии развития критического мышления
Деятельность учителя | Деятельность учащихся | Приёмы и методы |
Стадия вызова | ||
Вызывает уже имеющиеся знания, задаёт вопросы по ранее изученному материалу, обсуждает полученную от учащихся информацию. | Вспоминают, анализируют, систематизируют уже имеющиеся знания по этой теме, демонстрируют свои знания с помощью устной речи. | Составление кластера. Совместное обсуждение полученных результатов. Корректировка записей в кластере. Самопроверка и самооценка за ответы в кластере. Работа ведётся индивидуально и парами. |
Стадия осмысления | ||
Рассказывает содержание нового материала, ведёт записи на доске, поддерживает интерес учащихся к теме. | Слушают объяснение учителя, ведут записи в тетрадях, выполняют лабораторные опыты, работают с текстом учебника. | Записи в тетради, ответы на поставленные вопросы, лабораторная работа, работа с материалом учебника. Работа ведётся индивидуально и парами. |
Стадия рефлексии | ||
Помогает проанализировать изученную информацию, установить причинно - следственные связи между блоками информации. | Соотносят новую информацию с уже имеющимися знаниями. | Выбор из списка формул тех веществ, которые взаимодействуют с кислотами. Самопроверка и самооценка за работу в течение всего урока. Работа ведётся индивидуально. |
Ход урока
I. Организационный момент. (1мин)
· подготовка аудитории к работе
· приветствие
· наличие учащихся
II. Мотивация учебной деятельности (1мин)
Итак, ребята, вы уже познакомились на предыдущих уроках с понятием «кислота» и разобрали вопрос о взаимодействии кислот с металлами. Сегодня мы продолжим знакомство с химическими свойствами кислот и будем учиться составлять уравнения химических реакций с участием кислот в молекулярном и ионном виде.
Сообщение темы урока, постановка познавательных задач для учащихся.
Тема урока записана на доске.
Задачи учащихся:
- запомнить основные химические свойства кислот в свете электролитической диссоциации;
- научиться составлять уравнения химических реакций с участием кислот в молекулярном и ионном виде.
III. Актуализация знаний учащихся. (13мин)
Сегодня мы начнём разбирать новый материал с заполнения кластера, что позволит нам вспомнить основные вопросы по кислотам. Для этого я вам приготовила специальные бланки, где вы внесёте свои ответы в течении 5 минут. Постарайтесь работать самостоятельно, проверяя себя и свою память.
Каждому ученику выдаётся бланк – кластер для внесения ответов. Кластер каждый ученик заполняет сам, а затем 2 минуты обсуждает результаты своей работы с соседним учеником по парте. После этого в течении 5 минут результаты работы обсуждаются совместно с учителем, а учащиеся класса вносят поправки в графу «дополнения, исправления».
Заполните таблицу
вопросы | ответы | дополнения и исправления |
1. На какие ионы диссоциируют кислоты? | ||
2. Почему растворы кислот проявляют одинаковые свойства? | ||
3. Какой цвет приобретает лакмус в растворе кислоты? | ||
4. Закончите возможное уравнение реакции: Zn + HCl à Cu + HCl à | ||
5. При каких условиях реакции между ионами протекают до конца? |
Во время проверки ответов учащиеся ставят себе по 1 баллу за верно выполненное задание. Таким образом, они могут максимально получить 5 баллов.
IV. Изложение нового материала. (25мин)
Итак, продолжаем разбирать основные химические свойства кислот в свете электролитической диссоциации. Когда мы изучали реакции обмена между ионами, то я вам показывала, как происходит взаимодействие между кислотой и щелочью. Напомните себе ещё раз этот материал с помощью текста учебника на странице 205. Когда будете читать материал, отметьте те моменты, которые, на ваш взгляд, требуют комментариев.
В течение 2-х минут ученики работают с учебником, а затем учитель даёт ответы на их вопросы, ещё раз акцентируя внимание на порядке выполнения данного эксперимента.
Кислоты могут взаимодействовать не только со щелочами, но и с нерастворимыми основаниями.
Таким образом, мы переходим с вами к выполнению лабораторных опытов.
Учитель выдаёт учащимся инструктивную карточку и напоминает основные правила работы по технике безопасности. Работа проводится по следующему плану: выполнение опыта, запись уравнения проделанной реакции в молекулярном и ионном виде, определение смысла реакции по записи краткого ионного уравнения. По мере разбора материала учитель сам или с помощью учащихся ведёт записи на доске.
Инструктивная карточка
Исследования химических свойств кислот
Л. о. №1. В ячейку пластины поместите 2 капли гидроксида натрия и 1 каплю сульфата меди II. К полученному осадку добавьте 1 каплю соляной кислоты. Что произошло с осадком? Составьте уравнение реакции между гидроксидом меди II и соляной кислотой в молекулярном и ионном виде.
Л. о. №2. В ячейку пластины поместите шпателем немного оксида кальция и прилейте к нему 2 капли азотной кислоты. Что произошло с оксидом? Составьте уравнение реакции между оксидом кальция и азотной кислотой в молекулярном и ионном виде.
Л. о. №3. В ячейку пластины поместите 1каплю карбоната натрия и 1 каплю серной кислоты. Что произошло при этом? Составьте уравнение реакции между карбонатом натрия и серной кислотой в молекулярном и ионном виде.
После выполнения лабораторной работы учитель просит учеников ответить на вопрос:
С какими классами веществ могут взаимодействовать кислоты?
Вывод по уроку подводим с помощью схемы на 211-ой странице учебника.
V. Закрепление изученного материала, сообщение домашнего задания. (5мин)
Для закрепления полученных знаний учитель предлагает выполнить задание, которое записано на обратной стороне бланка – кластера. Задание выполняют 2 минуты, затем проверяют правильность его выполнения. Во время проверки ответов учащиеся ставят себе по 1 баллу за верно выполненное задание. Таким образом, они могут максимально получить 4 балла.
Вариант 1 | Вариант 2 |
Выберите формулы веществ, с которыми будет взаимодействовать раствор кислоты и реакции протекают до конца соляная кислота + Al, SO2, Fe(OH)2, Aq, K2O, CuSO4, AqNO3. | Выберите формулы веществ, с которыми будет взаимодействовать раствор кислоты и реакции протекают до конца серная кислота + Fe, K2CO3, CO2, Mq(OH)2, BaCl2, Cu, Al2O3. |
В конце урока ученики суммируют свои баллы. Учитель отмечает или оценивает работу тех учеников, которые по ходу урока были активны и набрали 8-9 баллов.
Домашнее задание (заранее написано на доске):
§ 38, выполнить упр. 4 на стр. 214

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




 Найти:
Найти:
