![]()
Для построения боровской теории водородного атома необходимо также привлечь постулат Планка о дискретности состояний гармонического осциллятора, энергия которого равна
![]() ( n – целое число).
( n – целое число).
Из этого постулата вытекает правило квантования круговых орбит: из всех орбит электрона, возможных с точки зрения классической механики, осуществляются только те, для которых момент импульса равен целому кратному постоянной Планка ![]() :
:
![]() (24)
(24)
§ 3. Атом водорода.
Согласно (24) момент импульса электрона, вращающегося со скоростью V, но орбите радиуса r вокруг ядра (![]() ), должен удовлетворять условию
), должен удовлетворять условию
![]()
Запишем также уравнение движения электрона, находящегося под действием кулоновской силы![]() (в системе СГСЕ), вокруг ядра:
(в системе СГСЕ), вокруг ядра:
![]()
Исключив v из этих двух уравнений, получим выражение для радиусов допустимых орбит
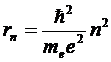 (n – целое число)
(n – целое число)
Радиус первой орбиты электрона в атоме водорода r1 носит название боровского радиуса:
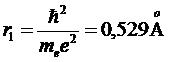
Для скорости электрона получается выражение
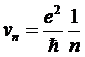
И, наконец, для полной энергии электрона, включающей как кинетическую часть (mev2/2), так и потенциальную (- e2/r), можно получить следующую формулу:
![]() (25)
(25)
Излучение или поглощение энергии атомом водорода по Бору происходит при переходе электрона с одной орбиты на другую. Энергия излучаемого или поглощаемого при этом фотона рассчитывается с помощью второго постулата Бора (см.§2)
![]()
отсюда для волнового вектора ![]() имеем:
имеем:
![]()
Таким образом, 2-ой постулат Бора перешел в обобщенную формулу Бальмера (20) с постоянной Ридбергера, равной
![]() ,
,
численное значение которой согласуется с ее экспериментальным значением (см. гл. 3, §1).
. § 4. Молекулы
а) Уравнение Шредингера для электронов в молекуле. Электронная энергия. Как известно, молекула состоит из ядер и связывающих их электронов. Поскольку ядра имеют массу, в несколько тысяч раз превышающую массу электрона, они движутся гораздо медленнее электронов. Поэтому движение последних в квантовой механике рассматривают в первом приближении как движение в поле неподвижных ядер. Тогда расстояния между ядрами рассматриваются параметры задачи. Решение соответствующего уравнения Шредингера показывает, что энергия электронов Е е квантуется, а ее собственные значения зависят от расстояния между ядрами. Для случая двухатомной молекулы эта зависимость для двух устойчивых состояний молекулы I и П имеет вид, показанный на рис.12б. В обоих случаях энергия имеет минимум при определенных значениях расстояния между ядрами X. Переход из одного устойчивого состояния в другое называют изменением электромагнитной конфигурации. Это приводит, как видно из рис.12б, к изменению кривой зависимости Ее(х)
б) Полная энергия. При заданной электронной конфигурации ядра молекулы могут различным образом колебаться около своих равновесных положений, а сама молекула вращаться относительно центра масс. С этими видами движений тоже связаны запасы энергии: колебательной Ev и вращательной Er. В первом приближении движение электронов, колебания ядер и вращение молекулы считают независимыми. Тогда полную энергию молекула можно записать в виде следующей суммы:
Е=Ее+Еv+Еr (57)
в) Колебательная энергия. При небольших отклонениях от положения равновесия (область вблизи R0 – рис12б) силы, возвращающие атомы обратно в положение равновесия, являются "квазиупругими", то есть подчиняются с достаточно высокой степенью точности закону Гука: F=-kx. Это видно из рис.12,: график в области вблизи Ro имеет вид параболы E=kx2/2(смотри рис.12а),откуда
![]()
Частица, коле6лющаяся под действием квазиупругой силы, называется гармоническим осциллятором. По законам квантовой механики возможные значения ее энергии дискретны, и их величины можно найти из решения соответствующего уравнения Шредингера. Эти значения (собственные значения) таковы:
![]() , (58)
, (58)
где v=0,1,2,3,…-колебательное квантовое число; ![]() - постоянная Планка; ω - циклическая частота колебаний классического гармонического осциллятора
- постоянная Планка; ω - циклическая частота колебаний классического гармонического осциллятора ![]() .Из формулы (58) следует, что расстояние между соседними уровнями энергии одинаковы. Еще раз подчеркнем, что это справедливо лишь для гармонического осциллятора, когда силы квазиупругие, а энергия осциллятора при смещении из положения равновесия Х равна кх2/2 (см. рис.12а). В реальных же молекулах подобный параболический ход потенциальной энергии наблюдается лишь при малых смещениях из положения равновесия (для небольших квантовых чисел V ). При больших смешениях эта зависимость имеет более сложный характер (рис. I2б), и колебания уже не будут гармоническими. Если учесть отклонения от гармоничности, то решение уравнения Шредингера дает следующие значения для уровней энергии:
.Из формулы (58) следует, что расстояние между соседними уровнями энергии одинаковы. Еще раз подчеркнем, что это справедливо лишь для гармонического осциллятора, когда силы квазиупругие, а энергия осциллятора при смещении из положения равновесия Х равна кх2/2 (см. рис.12а). В реальных же молекулах подобный параболический ход потенциальной энергии наблюдается лишь при малых смещениях из положения равновесия (для небольших квантовых чисел V ). При больших смешениях эта зависимость имеет более сложный характер (рис. I2б), и колебания уже не будут гармоническими. Если учесть отклонения от гармоничности, то решение уравнения Шредингера дает следующие значения для уровней энергии:
![]()
где 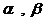 - так называемые коэффициенты ангармоничности. Из этой формулы видно, что для реальных молекул расстояния между колебательными уровнями энергии ухе не одинаковы с увеличением квантового числа V уровни сгущаются и стремятся к некоторому предельному значению. Если энергия колебаний превышает этот предел, то молекула диссоциирует - распадается на составные части.
- так называемые коэффициенты ангармоничности. Из этой формулы видно, что для реальных молекул расстояния между колебательными уровнями энергии ухе не одинаковы с увеличением квантового числа V уровни сгущаются и стремятся к некоторому предельному значению. Если энергия колебаний превышает этот предел, то молекула диссоциирует - распадается на составные части.
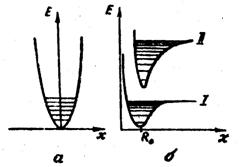 |
Рис.12. Потенциальные кривые и уровни энергии двухатомной молекулы:
а)в приближении гармонического осциллятора (расстояние между уровнями одинаковое);
б)для реальной молекулы с невозбужденным (I) и возбужденным (II) электронными состояниями (уровни сгущаются при приближении у энергии диссоциации)
Отметим, что даже при V =0 энергия колебаний не обращается в ноль, а принимает конечное значение, называемое нулевой энергией, то есть колебания молекул никогда не прекращаются.
Таким образом, расстояния между колебательными уровнями энергии и связанные с ними частоты колебаний молекулы определяются закoнoмepнocтями потенциальной энергии взаимодействия атомов в молекуле. Эта энергия, в свою очередь, зависит от состояния атомных электронов, Если при поглощении фотонов электроны в молекуле переводятся в возбужденное состояние, то это приводит к изменению сил взаимодействия атомов.(см. изменение хода кривой Е(х) на рис.12б. F= - dE/dx) и, следовательно, к изменению системы колебательных уровней энергии и частот колебаний.
г) вращательная энергия. Если, молекула имеет момент инерции I к вращается с угловой скоростью ωr то энергия вращения (Er) равна:
![]() ,
,
где ![]() - момент импульса молекулы. Согласно законам квантовой механики последний может принимать дискретные значения:
- момент импульса молекулы. Согласно законам квантовой механики последний может принимать дискретные значения:
![]() (j=0,1,2,…),
(j=0,1,2,…),
j – квантовое число момента импульса, которое в данном случае называют вращательным квантовым числом. Следовательно,
![]() (59)
(59)
Для вращательного квантового числа имеется правило отбора:
![]()
которое и определяет испускание (или поглощение) молекулой квантов света, связанное с вращательными переходами.
С учетом формул (58), (59) полную энергию молекулы (57) можно записать в следующем виде:
![]() (60)
(60)
д) Спектры изолированных молекул. Спектры поглощения молекул отличаются от спектров атомов прежде всего большей сложностью. Это объясняется тем, что изменение внутренней энергии атомов связано лишь с изменением энергии отдельных электронов, в то время как изменение энергии молекул складывается из изменения энергии трех ее составляющих (см.(60)). - энергии электронов, энергии колебаний атомов внутри молекулы и энергии вращения молекулы как целого.
Согласно правилам квантовой механики все три вида энергия молекулы квантуются, то есть могут принимать лишь определенные дискретные значения (уровни энергии). Получающаяся сложная система уровней всей молекулы схематически показана на рис. 13 (масштаб по шкале энергий не соблюден).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




