6.Контрольные вопросы.
1. Цель исследования молекулярных спектров.
2. Различия между спектроскопией атомов и молекул?
3. Структура уровней энергии молекулы.
4. В чем отличия колебаний молекулы от колебаний гармонического осциллятора?
5. В чем состоит влияние изменения состояния электронов в молек6уле на характеристики колебаний?
6. Какие виды энергии молекулы изменяются при поглощении фотонов в видимой части спектра?
7. С какой целью в работе рассчитываются разности энергии фотонов?
8. Опишите принципиальную схему измерений.
9. Опишите методику определения частоты колебаний и энергии асс6оциации молекул.
Лабораторная работам 342
ОПРЕДЕЛЕНИЕ ПОСТОЯНОЙ РИДБЕРГА ПО СПЕКТРУ АТОМАРНОГО ВОДОРОДА
I. Цель и содержание работа
Целью работы является ознакомление с закономерностями в спектре водорода. Работа состоит в градуировке спектроскопа, определении длин волн четырех спектральных линий серии Бальмера и расчете постоянной Ридберга.
II. Краткая теория работы
1. См. Ч.1, Гл. III, IV (§§ 1, 2)
2. Вывод расчетной формулы
Постоянную Ридберга можно найти о помощью формулы (Ч.1-20), определив экспериментальным путем длины волн в какой-либо серии. Наиболее удобно это сделать в видимой области спектра, то есть для серии Бальмера (Ч.1-21). В настоящей работе определяются длины волн первых четырех наиболее ярких спектральных линий этой серии, для которой I принимает значения: 3(красная линия), 4(голубая), 5(фиолетовая), 6(темно-фиолетовая, слаборазличимая). Таким образом, постоянная Ридберга определяется из четырех независимых измерений по формуле, вытекающей из (Ч.1-20):
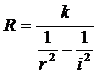 (i=3,4,5,6).
(i=3,4,5,6).
III. Приборы и принадлежности для выполнения работы
Установка, используемая в работе, состоит из монохроматора УМ-2 и двух спектральных ламп - ртутной и водородной, питание которых осуществляется от специальных устройств.
Монохроматор служит в данном случае в качестве спектроскопа, так как выходная щель монохроматора заменена окуляром, что позволяет наблюдать спектр визуально, в частности для определения длин волн линий в спектре водорода. Оптическая схема монохроматора показана на рис. 1: 1 - источник света, 2 - защитное стекло щели, 3 - щель коллиматора, 4 - объектив коллиматора, 5 – диспергирующая призма, 6 - объектив зрительной трубы, 7 - указатель в фокальной плоскости окуляра, 8 - окуляр зрительной трубы. Объектив коллиматора, в фокусе которого находится щель, образует параллельный пучок света и направляет его на призму 5. Призма преобразует этот пучок в систему параллельных пучков, выходящих из диспергирующего элемента под различными углами, зависящими от длины волны. Объектив зрительной трубы фокусирует отдельные параллельные пучки и образует в фокальной плоскости совокупность монохроматических цветных изображений входной щели, которые и представляют собой спектры, наблюдаемые с помощью окуляра.
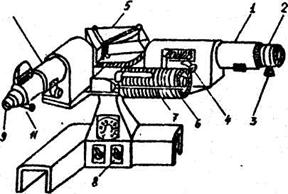
Рис.2. Общий вид монохроматора
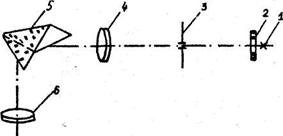
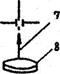
Рис.1
Общий вид монохроматора показан на рис. 2: 1 - коллиматор, 2 - щель, ширина которой регулируется микрометрическим винтом 3. Винт 4 служит для фокусировки изображения спектральных линий. Поворот призмы 5 осуществляется вращением барабана 6. В зависимости от положения призмы в поле зрения попадает тот или иной участок спектра. На барабане нанесена шкала в относительных делениях - градусах поворота самого барабана. Шкала барабана освещается лампочкой 7, включение которой производится тумблером 8. В фокальной плоскости окуляра 9 зрительной трубы 10 находится указаcм. pиc.1 - указа
Спектральные лампы
а) Ртутная лампа. Для того чтобы привести в соответствие деления шкалы барабана с длинами волн, монохроматор необходимо проградуировать. Для градуировки используется газоразрядная
ртутная лампа с линейчатым спектром излучения. Включение лампы производит лаборант.
б) Водородная лампа. В качестве источника света, спектр которого изучается в данной работе, применяется газоразрядная водородная трубка Гейслера. Трубка представляет собой Н-образный стеклянный баллон, заполненный водородом при давлении порядка нескольких мм рт. ст. В колена трубки впаяны электроды, на которые подается переменное напряжение 3000 В. В трубке устанавливается тлеющий разряд. В столбе газового разряда происходит диссоциация молекул водорода, атомы которого, возбуждаясь, излучают характерный для. атомарного водорода спектр.
Понятно, что молекулы водорода также могут возбуждаться и излучать спектр. Этот молекулярный спектр имеет гораздо более сложную структуру (так называемый "полосатый" спектр).
Но интересующие нас 4 линии серии Бальмера гораздо ярче, чем полосы молекулярного спектра, и легко различимы на его фоне.
Водородную лампу также включает лаборант.
IV. Порядок выполнения работы
1. Градуировка монохроматора.
а) Установить против щели монохроматора ртутную лампу и попросить лаборанта ее включить. Вращая винт 4 и перемещая окуляр 9, получить четкое изображение спектральных линий.
б) Поворачивая барабан 6, совместить изображение спектральных линий с указателем и произвести отсчет делений по шкале барабана. Эта операция необходима для всех линий, указанных в таблице, имеющейся на установке. Для правильной градуировки очень важно осуществить отсчет далекий по шкале барабана именно для тех линий, которые изображены на этой таблице и для которых указана длина волны. Данные занести в табл. 1. Для каждой линии отсчет по шкале барабана сделать 3 раза, причем линия к указателю подводится со стороны больших длин волн. Снять показания для 13 линий в спектре ртути.
Таблица 1
№ | спектральные линии | длинна волны нм | деление шкалы барабана | среднее деление шкалы барабана |
1 | 1 2 3 | |||
2 | 1 2 3 | |||
3 | 1 1 2 3 | |||
13 | 1 2 3 |
в) Выключить лампу (выполняется лаборантом).
2. Изучение спектра водорода.
а) Установить против щели монохроматора водородную лампу и обратиться к лаборанту о просьбой включить ее.
б) Вращением барабана 6 совместить с указателем поочередно изображение четырех наиболее ярких линий (красной, голубой, фиолетовой, темно-фиолетовой) и произвести отсчет по шкале барабана. Для каждой линии необходимо сделать отсчет не менее трех
раз, подводя линию к указателю со стороны больших длин волн. Данные занести в табл.2.
в) После окончания сразу же выключить водородную лампу, так как срок ее службы ограничен (выполняется лаборантом).
Таблица 2
№ | спектральная линия | деление шкалы барабана | среднее деление шкалы барабана | длинна волны λ,нм | волновое число k | постоянная Ридберга R |
1 2 3 | красная | |||||
1 2 3 | голубая | |||||
1 2 3 | фиолетовая | |||||
1 2 3 | темно-фиолетовая |
Среднее значение постоянной Ридберга Rcp=…
V. Обработка результатов измерений
1. Построить на миллиметровой бумаге градуировочный график.
График должен быть выполнен очень аккуратно и иметь размер примерно 35x35 см. На график наносить точки, соответствующие средним делениям шкалы барабана.
2: Определить по градуировочному графику длины волн четырех измеренных линий спектра водорода.
3. По формуле (I) вычислить постоянную Ридберга, подставив
соответствующие значения n, i. Найти среднее значение R
4. Оценить погрешность измерения R, используя методику
обработки прямых измерений.
VI. Контрольные вопросы
1. При каких условиях возникают линейчатые спектры?
2. Какова модель атома по теории Резерфорда - Бора?
Сформулируйте постулаты Бора.
3. Выведите на основе теории Бора формулу для энергии электрона на n-ой орбите. Объясните смысл отрицательного значения энергии электрона в атоме.
4. Выведите формулу для константы Ридберга на основе теории Бора.
5. Каковы трудности теории Бора?
6. Объясните устройство монохроматора?
7. Как производится градуировка монохроматора?
8. Что влияет на погрешности измерений в данной работе?
9. Что такое ψ - функция и каков ее статистический смысл?
10. Объясните, как происходит квантование энергии в квантовой механике. Сравните его с квантованием по Бору.
11. Напишите уравнение Шредингера для электрона в атоме водорода. От каких квантовых чисел зависит решение итого уравнения? Каков их смысл?
12. Доказать, что кратность вырождения состояний где электрона в атоме водорода равна n2 .
13. Квант света выбивает электрон из атома водорода, находящегося в нормальном состоянии. С какой скоростью будет двигаться электрон вдали от ядра? Энергия электрона на 1-й боровской орбите равна (по модулю) Е1.
14. В каких пределах должна бить энергия в эВ бомбардирующих электронов, чтобы при возбуждении атома водорода ударами этих электронов спектр водорода имел только одну спектральную линию? Энергия электрона на основном уровне (Е1 = 13,6 эB).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




