ΔН0r, t = f(T) (Рис. 2.1.)
ΔS0r, t = f(T) (Рис. .2.2.)
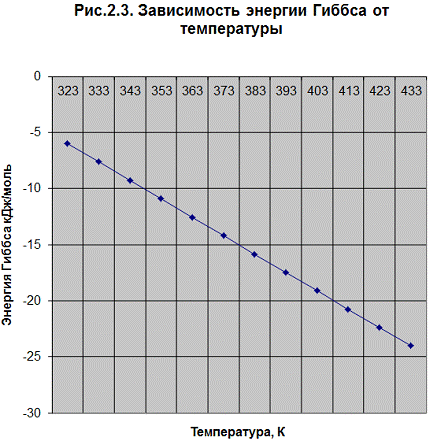
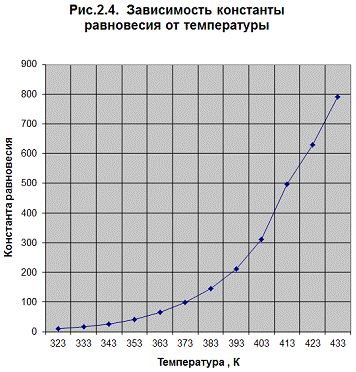
ΔG0r, t = f(T) (Рис. .2.3.)p = f(T) (Рис. 2.4.)
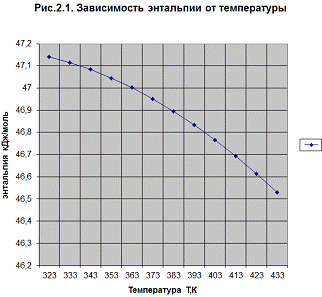
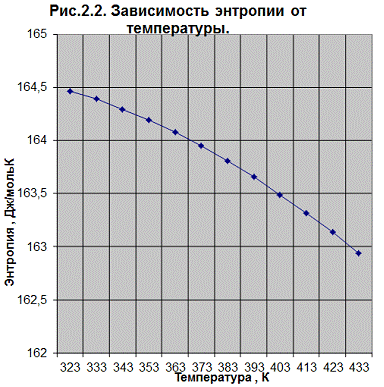
Выводы: Термодинамический расчет показал, что по мере увеличения температуры, тепловой эффект реакции уменьшается. По значению энтальпии (![]() Н0r, t) реакция эндотермическая. Энтропия уменьшается с увеличением температуры. В указанных условиях реакция протекает самопроизвольно, т. к. значения энергии Гиббса отрицательны (
Н0r, t) реакция эндотермическая. Энтропия уменьшается с увеличением температуры. В указанных условиях реакция протекает самопроизвольно, т. к. значения энергии Гиббса отрицательны (![]() G0r. t < 0). Лучше проводить реакцию при повышенных температурах, т. к. минимальное значение
G0r. t < 0). Лучше проводить реакцию при повышенных температурах, т. к. минимальное значение ![]() G0r.433= -24,025, а константа равновесия имеет максимальное значение Кp =791,30 при температуре 433 К.
G0r.433= -24,025, а константа равновесия имеет максимальное значение Кp =791,30 при температуре 433 К.
Так как с увеличением температуры значение константы равновесия увеличивается и равновесие смещается в сторону продуктов реакции, то реакционную смесь нужно нагревать (при этом не стоит забывать об образовании побочных продуктов реакции). Также на смещение равновесия в сторону продуктов реакции влияет уменьшение парциального давления, концентрации спирта и т. д. (по принципу Ле-Шателье). С увеличением температуры увеличивается скорость реакции.
3. Кинетика и механизм реакции получения изобутилена
.1 Механизм реакции и его обоснование
Решение вопроса о механизме образования непредельных углеводородов из спиртов при проведении дегидратации последних в кислой среде осложняется тем, что в условиях реакции получающиеся непредельные углеводороды могут изомеризоваться, превращаясь в более устойчивые структурные или стерические изомеры. При обсуждении вопроса о механизме образования непредельных соединений с точки зрения электронной теории, Ингольд принял во внимание тот факт, что реакции отщепления очень часто сопутствуют реакциям замещения и, следовательно, с большей долей вероятности можно предложить существование аналогичных начальных механизмов процессов [37].
Реакция дегидратации трет-бутилового спирта протекает по механизму Е1, с образованием промежуточного комплекса [26] :
H CH3
| |
(CH3)3C-OH+H+ ↔ (CH3)3 C - O + ↔ CH3-C+- +H2O (I)
| |
H CH3
CH3 CH2
| ||
CH3-C+ ↔ CH − CH3 (II)
| |
CH3 CH3
Реакция отщепления обусловливается изменением состояния связи С-ОН в молекуле в следствии взаимодействия ее с растворителем.
На первой стадии образуется карбианион, а на второй образуется непредельное соединение [37].
Очевидно, что условия, способствующие реакциям замещения должны ускорять также и реакции отщепления (Е1), поскольку в обоих случаях существенной стадией является образование карбониевого иона [43].
3.2 Анализ факторов, влияющих на основную реакцию
.2.1 Влияние строения субстрата
Строение субстрата оказывает значительное влияние на ход реакции, т. к. из субстрата образуется катион, который может влиять на направление реакции. При образовании карбкатиона атом углерода переходит из первичного тетраэдрического состояния в более устойчивое планарное состояние, в котором три метильные группы максимально удалены друг от другой. В ряду от СН3+ до (CН3)3C+ стабильность карбониевого иона возрастает и обусловлена влиянием индуктивных эффектов [37].
При постепенном замещении Н-атомов CН3- группами в метиловом спирте скорость реакции бимолекулярного отщепления падает, а мономолекулярного возрастает.
Таким образом, можно заключить, что строение трет-бутилового спирта способствует протеканию реакции по Е1 механизму, так как подход Н+- частицы к С-атому, при котором происходит процесс отщепления стерически наиболее затруднен. Ионизация же по связи С-ОН в трет-бутаноле, наоборот, требует меньшей затраты энергии, чем в случае изопропанола, и т. д.
Иными словами, чем более разветвленными являются молекулы спирта, тем более «сжатыми» они оказываются при превращении в промежуточную структуру - карбоиневый ион. «Сжатие» уменьшается, если происходит потеря протона, что делает отщепление наиболее предпочтительнее по сравнению с реакцией замещения [43].
Таким образом, можно заключить, что стерические затруднения вызванные наличием трех метильных групп в молекуле трет-бутанола способствует протеканию реакции по механизму отщепления Е1, а не замещения.
3.2.2 Влияние строения атакующей частицы
Атакующая частица Н+, определяет наличие кислотной среды в реакционной смеси, что способствует отщеплению ОН-группы. Отщепление происходит за счет начальной протонизации, приводящей к образованию положительно заряженных частиц (а не нейтральных молекул).
3.2.3 Влияние строения уходящей группы
Скорость реакции протекающей по механизму Е1, зависит от природы покидающей группы. Чем ниже энергия связи этой группы с атомом углерода и чем выше способность покидающей группы давать анион, тем легче должна проходить реакция по Е1 механизму. Энергия связи С-О, равная 314кДж/моль [41], способствует протеканию реакции по механизму Е1. Чем большей основностью обладает уходящая группа, тем в большей степени увеличивается вероятность отрыва водорода и образования олефина. Увеличение объема уходящей группы также приводит к увеличению выхода продуктов отщепления [37].
3.2.4 Влияние растворителя
При диссоциации нейтрального субстарата на ионы переходное состояние более полярно, чем исходный субстрат. Это приводит к тому, что при увеличении диэлектрической проницаемости (полярности) сольватация переходного состояния увеличивается сильнее, и становится больше чем в исходном субстарте. Это приводит к повышению стабильности ионов и увеличению скорости по двухстадийному механизму [43].
При использовании протонных растворителей (Н2О), кроме неспецифичной сольватации наблюдается специфичная сольватация, связанная с образованием водородных связей с уходящей группой. С другой стороны, чтобы увеличить скорость отщепления необходимо уменьшить полярность растворителя. Поэтому в качестве растворителя вместо воды можно использовать этилцеллозольв [1].
Но поскольку вода как растворитель используется в технологических целях, то предполагается ее использование в минимальных количествах для разбавления трет-бутанола.
3.3 Катализ изучаемой реакции
В качестве катализатора предпологается использовать катиониты КУ-2.
Большая часть исследованных реакций дегидратации на ионитах протекает по ионному механизму. На первой стадии трет-бутиловый спирт взаимодействует с ионитом, образуя оксониевый ион ион [40]:
(CН3)3COH +R SO3H → (CН3)3C - O+H2+RSO-3,
который переходит в результате отщепления воды в карбониевый ион:
(CН3)3C-O+H2 → (CН3)3C++H2O
Карбониевый ион может отщепить протон (присоединяющийся затем к катиону) с образованием олифина:
(CН3)3C+ → (CН3)2С=CН2
или же вступить в реакцию со следующей молекулой спирта:
(CН3)3C++(CН3)3COH → (CН3)3 C-О+H-C(CН3)3
с переходом образовавшегося оксониевого иона в простой эфир и отщеплением протона:
(CН3)3C - О+H - C(CН3)3 → (CН3)3С-O-C (CН3)3+Н+
Альтернативным путем превращения карбониевого иона может быть взаимодействие с молекулой олефина, ведущее к образованию полимеров:
(CН3)2С=CН2 → (CН3)2СН−CН =C−(CН3)2
Большое влияние на каталитическую активность ионитов в реакцию дегидратации оказывает их влажность. Это влияние нельзя охватить одной общей закономерностью [40].
Количественная трактовка этого вопроса для реакций, выполняемых в присутствии полимеризационных катионитов, возможна на основе модели Ленгмюра-Хиншельвуда. При таком подходе, изучив резкое снижение скорости выделения изобутилена по мере разложения трет-бутилового спирта на столе дуаэкс-50W, которое авторы исследования объясняют блокировкой и иноктивацией активных групп в выделяющейся водой (реакция1), что затрудняет образование промежуточного комплекса А со спиртом и таким образом мешает течению основных реакции 2:
G+W =GW (1)+ G = AG=C4H8 + H2O (2)
где G - активные группы;
GW - комплекс воды и активных групп;
W - вода;
AG - комплекс спирта спирта и активных групп катализаторов;
А - спирт;
Теоретические расчеты, выполненные на основании этой модели, позволили построить кривую зависимости удельной скорости образования олефина от мольной доли воды в простой разнице фазе (рис. 3.3.1).
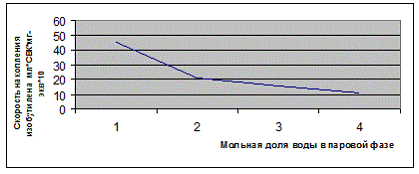
Рис. 3.3.1 Зависимость удельной скорости образования изобутилена при разложении трет-бутанола на катионине дауэке -50х2 от мольной доли воды в парообразной фазе.
Чтобы избежать тормозящего влияние воды на каталитические реакции многие авторы применяли азеотропную отгонку.
Однако же всегда присутствие воды в ионите или реакционной массе оказывает неблагоприятное влияние на кинетику накопления продуктов реакции. Порой в присутствии влаги затрудняется течение нежелательных побочных процессов, усиливаются протонодонорные свойства сульфогрупп или же благодаря набуханию катиониты создаются благоприятные условия для протекания реакции во всем объеме зерна [44]. Зависимость степени набухания катализатора от содержания трет-бутанола (рис. 3.3.2) являются важным технологическим параметром, определющим размер дегидратора [44].
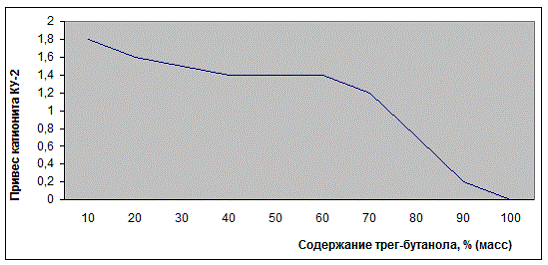
Рис. 3.3.2 Зависимость набухаемости катионита КУ-2 в водных растворах труг-бутанола от его концентрации.
3.4 Кинетическая модель реакции
Изучение кинетических закономерностей процесса дегидратации трет-бутанола, с помощью ионообменных смол и количественная обработка результатов приводится в работах Фриллета, Моувера и Рубина, а также Чаплица, Самохваловой, Тюряева [12].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



